Биполярное расстройство
- 1 year ago
- 0
- 0
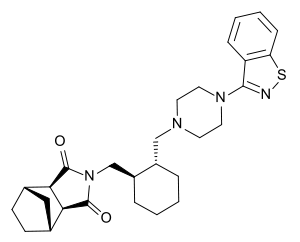
Луразидон (Латуда; DSP-1349M; SM-13496; SMP-13496) — атипичный антипсихотик , одобренный для лечения шизофрении и биполярного расстройства . Луразидон был синтезирован и разработан компаниями Dainippon Sumitomo Pharma и благодаря химическому объединению структуры ядра молекул антипсихотиков ряда «-донов» ( рисперидон , зипрасидон и др.) и антидепрессанта - анксиолитика тандоспирона с целью усиления их антидепрессивных и прокогнитивных свойств за счёт повышения афинности к серотониновым рецепторам 5-HT7 и 5-HT1А типов и исключения из фармакодинамического профиля взаимодействия с нежелательными мишенями, ответственными за развитие целого ряда побочных эффектов . Луразидон был одобрен в США для лечения шизофрении у взрослых и подростков с 13 лет в октябре 2010 года, а также депрессивных эпизодов при биполярном аффективном расстройстве I типа у взрослых и детей с 10 лет в июне 2013 года . В Российской Федерации Латуда зарегистрирована в августе 2016 года и одобрена для лечения шизофрении у взрослых и подростков с 13 лет и депрессии при биполярном аффективном расстройстве I типа у взрослых и детей с 10 лет в монотерапии, а также для адъювантной терапии в сочетании с литием или вальпроатами у взрослых .
Луразидон исследован в обширной клинической программе, включавшей исследования как краткосрочной, так и долгосрочной противорецидивной эффективности при шизофрении и депрессивных эпизодах, обусловленных биполярным аффективным расстройством I типа как в качестве монотерапии, так и в качестве дополнительной терапии с препаратами лития или вальпроевой кислоты (стабилизаторы настроения).
Эффективность луразидона для лечения острого рецидива шизофрении была продемонстрирована в ходе пяти многоцентровых, плацебо -контролируемых, двойных слепых 6-недельных клинических исследований (КИ) в дозах 40-160 мг в сутки. В них основной показатель эффективности определялся как среднее изменение суммы баллов к 6-й неделе терапии, относительно исходного значения по оценке с помощью шкалы позитивных и негативных синдромов () . Статистически значимые отличия от плацебо были зарегистрированы уже на 4-й день терапии . Кроме того, луразидон превосходил плацебо по заранее определённому вторичному показателю эффективности — показателю шкалы общего клинического впечатления о тяжести заболевания () . В двух из пяти краткосрочных исследованиях для оценки чувствительности в одной из параллельных с луразидоном и плацебо групп использовались оланзапин и кветиапин типа XR. Оба препарата продемонстрировали значительное преимущество перед плацебо, но не перед луразидоном, то есть по результатам рандомизированного контролируемого испытания (РКИ) луразидон показал одинаковую эффективность как в сочетании с оланзапином , так и в сочетании с кветиапином XR в терапии острого рецидива психотической симптоматики шизофрении . Кроме того, краткосрочная эффективность луразидона при лечении шизофрении оценивалась в ходе нескольких объединённых анализов данных вышеупомянутых 6-недельных исследований. Так, объединённый анализ пяти РКИ (n = 1029) с использованием пятифакторной модели шкалы PANSS показал, что луразидон в фиксированных дозах 40-160 мг в сутки статистически достоверно улучшал к 6-й неделе терапии как общий балл шкалы PANSS (p < 0,001; величина эффекта — 0,45), так и показатели позитивной, негативной симптоматики шизофрении, нарушения мышления, агрессивности / возбуждения , а также депрессии / тревоги .
Симптомы депрессии широко распространены при шизофрении, и их наличие может ухудшить клинические результаты. В ходе краткосрочных исследований применялась шкала Монтгомери-Асберг для оценки депрессии (). Объединённый анализ четырёх рандомизированных плацебо-контролируемых 6-недельных КИ у пациентов с шизофренией (n = 1330) показал, что луразидон является эффективным антидепрессантом у пациентов с депрессивными симптомами, ассоциированными с шизофренией: лечение луразидоном приводило к статистически достоверному улучшению депрессивной симптоматики в сравнении с плацебо. Среднее изменение балла шкалы MADRS составило −2,8 в группе луразидона и −1,4 в группе плацебо (p < 0,001; величина эффекта — 0,24) .
Долгосрочная эффективность препарата изучалась в двойном-слепом РКИ , где луразидон продемонстрировал более высокие показатели ремиссии и меньший риск в сравнении с кветиапином XR . Оценка вероятности госпитализации по к 12 месяцу была статистически достоверно ниже у пациентов в группе луразидона (9,8 %) в сравнении с группой кветиапина XR (23,1 %; p < 0,05). 12 месяцев лечения луразидоном было связано с 56,7 % сокращением риска госпитализации в сравнении с кветиапином XR. Отмечалось статистически достоверно большее изменение общего балла PANSS (-34,6; p < 0,01 от исходного уровня острой фазы исследования и −5,0; p < 0,01 от исходного уровня расширенной 12-месячной фазы) и субшкалы позитивных симптомов PANSS (-12,3; p < 0,01 от исходного уровня острой фазы исследования и −1,5; p < 0,01 от исходного уровня расширенной 12-месячной фазы) в группе луразидона в сравнении с группой кветиапина XR. Помимо этого, было обнаружено и статистически достоверное превосходство луразидона над кветиапином XR по оценке изменений по шкале MADRS от исходного уровня острой фазы РКИ до финальной оценки по завершении расширенной 12-месячной фазы (-6,0 против −3,8; p < 0,05) .
Кроме клинического состояния, чрезвычайно важным при длительной поддерживающей терапии шизофрении является уровень социального функционирования , и оказывающий на него наибольшее влияние когнитивный статус пациентов. В одном из двойных слепых рандомизированных клинических исследований было показано, что изменение композитного индекса, полученного при проведении компьютеризированной нейрокогнитивной батареи тестов , оказалось статистически значимо лучше при использовании луразидона в дозе 160 мг в сравнении как с группой плацебо (p = 0,038), так и с группой кветиапина XR (p = 0,018). В расширенной 12-месячной фазе этого исследования изменение композитного индекса по сравнению с его первоначальным значением было также более выражено для объединённой группы луразидона в сравнении с группой кветиапина XR как на 19-й (p = 0,05), так и на 32-й неделях терапии (p = 0,008). В проведённом ретроспективном анализе этого исследования улучшение когнитивного функционирования по композитному нейрокогнитивному Z-баллу было достоверно выше в группе пациентов, получавших луразидон в финальной дозе 120 мг в сутки (p = 0,02) и 160 мг в сутки (p = 0,05) .
Луразидон также может быть эффективен при лечении шизофрении у подростков с 13 лет. Так, в двойном слепом плацебо-контролируемом РКИ луразидон в дозах 40 и 80 мг в сутки показал статистически достоверное и клинически значимое улучшение позитивной, негативной, когнитивной и аффективной симптоматик шизофрении по шкале PANSS, по сравнению с плацебо . Кроме того, на основании двухлетнего открытого расширенного исследования при более длительном лечении продолжает наблюдаться постоянное улучшение состояния пациентов . Луразидон хорошо переносится и имеет минимальное влияние на аппетит, массу тела и метаболические параметры. Это особенно важно при лечении подростков, в связи с их эндокринной неустойчивостью и особой повышенной чувствительностью к метаболическим ПЭ при применении АП .
В рандомизированном двойном слепом плацебо-контролируемом исследовании монотерапии с применением луразидона депрессии в рамках БАР I типа пациенты получали лечение луразидоном (20-60 мг в сутки [n = 166] или 80-120 мг в сутки [n = 169]) или плацебо (n = 170) в течение 6 недель. Оценка проводилась по шкалам MADRS и CGI-BP. Луразидон значительно снижал средние общие баллы по шкале MADRS на 6-й неделе как в группе 20-60 мг в сутки (-15,4; величина эффекта = 0,51), так и в группе 80-120 мг в сутки (-15,4; величина эффекта = 0,51) по сравнению с плацебо (-10,7). Точно так же лечение луразидоном привело к значительно большему снижению тяжести депрессии по шкале CGI-BP как для группы 20-60 мг в сутки (-1,8; величина эффекта = 0,61), так и для группы 80-120 мг в сутки (-1,7; величина эффекта = 0,50) по сравнению с плацебо (-1,1). Обе группы луразидона также продемонстрировали значительное улучшение симптомов тревоги. Частота прекращения приёма из-за побочных эффектов была аналогичной в группах 20-60 мг в сутки (6,6 %), 80-120 мг в сутки (5,9 %) и плацебо (6,5 %) .
В одном исследовании оценивали эффективность луразидона, в качестве дополнительной терапии литием или вальпроатом при биполярной депрессии I типа. Пациенты были рандомизированы в группу луразидона (N = 183) или плацебо (N = 165), добавленным к терапевтическим уровням лития или вальпроата. Динамика депрессивной симптоматики оценивалась по шкалам MADRS и CGI-BP. Лечение луразидоном значительно снизило средний общий балл по шкале MADRS на 6-й неделе по сравнению с группой плацебо (-17,1 против −13,5; величина эффекта = 0,34). Точно так же лечение луразидоном привело к значительно большему снижению тяжести депрессии по шкале CGI-BP по сравнению с плацебо (-1,96 против −1,51; величина эффекта = 0,36), а также к значительному улучшению симптомов тревоги. Частота прекращения лечения из-за побочных эффектов составила 6,0 % и 7,9 % в группах луразидона и плацебо, соответственно .
В недавнем исследовании пациенты в возрасте 10-17 лет с биполярной депрессией I типа, завершившие 6-недельное двойное слепое исследование луразидона по сравнению с плацебо, имели право на участие в двухлетнем расширенном открытом исследовании, в котором пациенты продолжали принимать луразидон в гибких дозах (20-80 мг в сутки) или переходили с плацебо на луразидон. Показатели эффективности включали пересмотренную шкалу оценки детской депрессии (CDRS-R) и Шкалу общего клинического впечатления и тяжести биполярной депрессии (CGI-BP-S). Функционирование оценивалось с использованием шкалы глобальной оценки детей (CGAS), при этом значение более 70 баллов указывало на отсутствие клинически значимого функционального нарушения. Критерии ответа были соблюдены, если пациент достиг 50 % снижения балльной оценки от исходного уровня в двойной-слепой фазе по общему баллу CDRS-R: критерии ремиссии были соблюдены, если пациент достиг общего балла CDRS-R = 28 и общего балла YMRS = 8 и CGI-BP-S = 3, и пациент считался соответствующим критериям выздоровления, если он достиг ремиссии с показателем CGAS > 70. Кроме того, также был проанализирован более строгий результат — устойчивая ремиссия, которая требовала, чтобы пациент соответствовал критериям ремиссии в течение 24 недель подряд. В общей сложности 306 пациентов завершили двойное-слепое 6-недельное исследование и вошли в расширенное открытое исследование; 195 (63,7 %) пациентов завершили курс лечения в течение одного года, а 168 (54,9 %) пациентов завершили курс лечения в течение двух лет. Процент ответчиков на начало открытой фазы, в конце первого года и в конце второго года открытой фазы составлял: 51,0 %, 88,4 % и 91,1 % соответственно; частота ремиссии составила 24,3 %, 61,3 % и 75,6 % соответственно. Устойчивая ремиссия была достигнута у 37,2 % пациентов через год и 57 % пациентов через два года. Таким образом, у детей и подростков с биполярной депрессией при лечении луразидоном до 2 лет наблюдалось неуклонное улучшение депрессивных симптомов, что приводило к прогрессивно более высокому уровню ответа, ремиссии, выздоровления и более строго рассчитанному результату устойчивой ремиссии .
Наиболее частыми побочными действиями луразидона в клинических испытаниях являлись тошнота , сонливость , экстрапирамидные расстройства ( акатизия , паркинсонизм , дистония ), тревога и ажитация , бессонница , седация , головная боль , головокружение , рвота . Акатизия и сонливость являются дозозависимыми побочными эффектами . Наблюдалось также повышение уровня глюкозы натощак . По другим данным, клинически значимого изменения уровня глюкозы и липидов не наблюдалось .
Луразидон, по-видимому, может вызывать такие общие для различных антипсихотиков побочные действия, как ортостатическая гипотензия и обмороки , злокачественный нейролептический синдром , поздняя дискинезия , увеличение веса и метаболические нарушения , гиперпролактинемия и связанные с ней расстройства (нарушения репродуктивной функции , снижение плотности костной ткани и др.) .
Поскольку для луразидона характерно низкое или очень низкое связывание с такими «нежелательными» рецепторными мишенями, как H1 гистаминовые рецепторы , 5-HT2C серотониновые рецепторы , М-холинергические, α1 адренорецепторы, D1 и D4 дофаминовые рецепторы , при его приёме маловероятно развитие таких побочных эффектов, как дневная сонливость, ортостатическая гипотензия и тахикардия , Повышение аппетита , прибавка массы тела, метаболические нарушения , снижение либидо , импотенция , антихолинергические эффекты ( парез аккомодации глаз , запоры , задержка мочи, сухость во рту, нарушения памяти и когнитивных функций) .
Луразидон обладает благоприятным профилем побочных эффектов с минимальным влиянием на массу тела и метаболический профиль. Так, в 12-месячном исследовании безопасности и переносимости луразидона с рисперидоном в качестве активного контроля отмечалось увеличение медианы глюкозы натощак при применении рисперидона, но не луразидона (медиана изменений уровня глюкозы (мг/дл, LOCF) для луразидона −0,5; для рисперидона 3,0; p = 0,005) . Помимо этого, отмечалось сокращение средней массы тела (-0,97 ± 5,06 кг) и индекса массы тела (ИМТ) (-0.33 ± 1,71 кг/м 2 ) у пациентов, получавших луразидон, тогда как у пациентов, получавших рисперидон, эти показатели выросли (1,47 ± 5,03 кг и 0,53 ± 1,76 кг/м 2 соответственно); эта разница оказалась статистически достоверной для обоих показателей (P < 0,001 для каждого) . В расширенной открытой фазе КИ с гибким дозированием (40-120 мг в сутки) лечение луразидоном было эффективным и в целом хорошо переносилось в течение 6 месяцев у пациентов, завершивших 6-недельное лечение луразидоном, оланзапином или плацебо; пациенты, изначально получавшие плацебо или луразидон испытывали небольшое повышение веса и минимальные изменения метаболических параметров в течение последующего лечения в открытой фазе в течение 6 месяцев, тогда как у пациентов, изначально набравших вес на оланзапине, наблюдалось сокращение массы тела и улучшение уровня липидов после переключения на луразидон .
Способность повышать уровень пролактина зависит, главным образом, от способности антипсихотика проникать через ГЭБ , что определяет антипсихотическую дозу, применяемую в клинике. Низкая способность проникать через ГЭБ определяет более высокие концентрации антипсихотика на периферии . Поскольку гипофиз находится не за ГЭБ, он подвергается воздействию циркулирующих уровней антипсихотика в крови . Ввиду высокой липофильности луразидон хорошо проникает через ГЭБ .
Для оценки долгосрочной безопасности луразидона у пациентов с шизофренией был проведён анализ двойного слепого сравнительного с рисперидоном исследования. Клинически стабильные взрослые амбулаторные пациенты с шизофренией были рандомизированы в соотношении 2:1 на 12 месяцев двойного слепого лечения с гибкими дозами луразидона (40-120 мг) или рисперидона (2-6 мг) один раз в сутки. Анализ уровней пролактина для пациентов мужского и женского пола показал стойкое повышение уровня пролактина для пациентов, рандомизированных в группы рисперидона, и практически отсутствие изменений для пациентов, получавших луразидон. Медианное изменение пролактина от исходного уровня у пациентов женского пола к 6 неделе терапии в группе рисперидона составило 40 нг/мл (нанограмм на миллилитр), а в группе луразидона — 0,9 нг/мл, а к концу 12 месяца — 28,4 нг/мл и 0,1 нг/мл соответственно. Таким образом, показано стойкое повышение уровня пролактина у пациентов, рандомизированных в группу рисперидона , и практически полное отсутствие изменений у пациентов, получавших луразидон .
Поскольку дневная сонливость является значительным фактором риска несоблюдения режима лечения, ухудшения когнитивных функций , профессиональной состоятельности и качества жизни, для систематической оценки этого неблагоприятного эффекта использовалась проверенная Шкала сонливости Эпворта. Лечение луразидоном в дозах 80 и 160 мг в сутки не было связано с увеличением сонливости по шкале Эпворта (улучшение уровня бодрствования), тогда как лечение кветиапином было связано со значительным увеличением дневной сонливости . Согласно инструкции по медицинскому применению сонливость наблюдается примерно у 10 % пациентов, что связано с сонливостью, наблюдаемой у некоторых пациентов в первые часы после приёма препарата, поэтому рекомендуемый режим дозирования предусматривает однократный вечерний приём препарата с последним приёмом пищи .
В программе клинических исследований луразидона не наблюдалось нежелательных явлений, связанных с удлинением интервала QT . У пациентов в рамках исследований не сообщалось об удлинении интервала QT свыше 500 м/сек, не отмечалось случаев аритмии , желудочковой тахикардии , фибрилляции или трепетания желудочков, у пациентов, получавших луразидон во всех краткосрочных и долгосрочных исследованиях . В специально проведённом исследовании влиянии луразидона на интервал QT с участием 73 пациентов c шизофренией или шизоаффективным расстройством, получавших луразидон 120 мг в сутки или 600 мг в сутки, ни один из пациентов не продемонстрировал удлинение интервала QT на >60 мсек от исходного уровня или продолжительности интервала QT > 480 мсек .
Луразидон метаболизируется главным образом в печени через систему цитохрома CYP3A4 , и его совместный приём с препаратами, которые являются сильными ингибиторами CYP3A4 (например, кетоконазол ) или сильными индукторами (например, рифампицин ), противопоказан .
Луразидон — это селективный антагонист дофаминовых и моноаминовых рецепторов, обладающий высоким сродством к D2 дофаминовым и 5-HT2А и 5-HT7 серотониновым рецепторам (степень сродства 0,994, 0,47 и 0,495 нМ, соответственно) . Среди атипичных антипсихотиков луразидон имеет самый высокий аффинитет к 5-HT7 рецепторам . Луразидон также блокирует α2С и α2А адренорецепторы (степень сродства 10,8 и 40,7 нМ, соответственно), обладает частичным агонизмом к 5-HT1А серотониновым рецепторам со степенью сродства 6,38 нМ. Луразидон клинически значимо не связывается с H1 гистаминовыми и мускариновыми рецепторами .
Антипсихотическое и нормотимическое действие луразидона, как и других антипсихотиков связано с блокадой D2 рецепторов дофамина. При этом луразидон обладает очень высокой селективностью именно к D2 подтипу дофаминовых рецепторов, не связываясь в применяемых дозах с D1 и D4 рецепторами . Считается, что отсутствие значимого связывания луразидона с D1 и D4, блокада которых в префронтальной коре приводит к ухудшению когнитивного функционирования, лежит в основе прокогнитивного эффекта луразидона, особенно выраженного у пациентов с шизофренией . В диапазоне однократных доз от 40 до 80 мг луразидон обеспечивает >60 % занятость D2 рецепторов в базальных ганглиях, необходимую для достижения антипсихотического действия . Таким образом, минимальной антипсихотической является доза 40 мг в сутки, а доза в 20 мг в сутки обладает достоверной антидепрессивной эффективностью, по-видимому, за счёт выраженного 5-HT7-антагонизма и парциального 5-HT1А-агонизма .
Теоретические представления о механизме действия луразидона, лежащем в основе его выраженное прокогнитивное, антинегативное и антидепрессивное действие связаны с представлением о его способности повышать уровень дофамина и серотонина в префронтальной коре . Стимуляция 5-HT1А рецепторов на телах тормозных ГАМКергических нейронов префронтальной коры приводит к ингибированию высвобождения ГАМК и ускоряет глутаматергические пирамидные нейроны, проецирующиеся в катехоламинергические ядра ствола мозга. Это повышает возбуждающую глутаматергическую нейротрансмиссию на телах дофаминергических нейронов (VTA), что, в свою очередь приводит к увеличению активности мезокортикального дофаминергического пути, проецирующегося в префронтальную кору . 5-HT7 и 5-HT2А рецепторы — возбуждающие. В коре они также располагаются на телах тех же ГАМКергических нейронов, что и 5-HT1А (тормозные), поэтому блокада 5-HT2А и 5-HT7 рецепторов приводит функционально тем же эффектам, что и стимуляция 5-HT1А рецепторов, и синергически повышает уровень дофамина в префронтальной коре. Таким образом, стимуляция 5-HT1А рецепторов имеет однонаправленное с блокадой 5-HT2А/5-HT7 рецепторов действие . Под действием луразидона быстрой десенситизации подвергаются не только 5-HT1А ауторецепторы на телах серотонинергических нейронов, но также и 5-HT7 рецепторы, расположенные на ГАМКергических нейронах ядер шва, тормозящих активность серотонинергических нейронов. Таким образом, инактивируются оба контура отрицательной обратной связи внутри DRN, что приводит к выраженному дезингибированию серотонинергической нейротрансмиссии .
Луразидон следует принимать с едой. При приёме с порцией пищи не менее 350 ккал биодоступность луразидона увеличивается в 2 раза.
Tmax в крови составляет от 1 до 3 ч. После приёма луразидона с пищей средняя Сmах и AUC увеличивались в 2-3 и 1,5-2 раза соответственно по сравнению со значениями после приёма луразидона натощак.
После приёма внутрь 40 мг луразидона средний кажущийся Vd составлял приблизительно 6000 л. Луразидон значительно (на 99 %) связывается белками плазмы крови.
Луразидон метаболизируется в основном при участии изофермента CYP3А4. Основными путями метаболизма являются окислительное N-деалкилирование, гидроксилирование нонборнанового кольца, S-окисление.
Луразидон метаболизируется с образованием двух активных метаболитов (ID-14283 и ID-14326) и двух неактивных метаболитов (ID-20219 и ID-20220). На долю луразидона и его метаболитов (ID-14283, ID-14326, ID-20219 и ID-20220) приходится приблизительно 11,4; 4,1; 0,4; 24 и 11 % радиоактивности плазмы соответственно. Активный метаболит ID-14283 метаболизируется в основном при участии изофермента CYP3A4. Фармакодинамический эффект обусловлен действием луразидона и его активного метаболита ID-14283 на дофаминовые и серотониновые рецепторы.
В исследованиях in vitro было выявлено, что луразидон не является субстратом изоферментов CYP1A1, CYP1A2, CYP2A6, CYP4A11, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 и CYP2E1.
В исследованиях in vitro луразидон не показал прямой или слабый ингибирующий эффект (прямой или зависимый от времени, 105,9 мкмоль) в отношении изоферментов CYP1А2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4. На основании этих данных не ожидается влияние луразидона на фармакокинетику ЛС, являющихся субстратами изоферментов CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 и CYP2E1.
В исследованиях in vitro было выявлено, что луразидон является субстратом для эффлюксных переносчиков P-gp и BCRP. Луразидон не является субстратом для активного транспорта с помощью транспортных полипептидов органических анионов ОАТР1В1 и ОАТР1В3.
Также исследования in vitro показывают, что луразидон является ингибитором P-gp , BCRP и транспортёров органических катионов первого типа (ОСТ1). Луразидон не оказывает клинически значимый ингибирующий эффект на ОАТР1В1, ОАТР1В3, транспортёры органических катионов второго типа (ОСТ2), транспортёры органических анионов первого (ОАТ1) и третьего типов (ОАТ3), почечные транспортёры МАТЕ1 и МАТЕ2К или экспортирующую помпу желчных кислот (BSEP).
T 1/2 составляет около 20-40 ч. После приёма внутрь луразидона, меченного радиоактивным изотопом, около 67 % дозы выводится кишечником и около 19 % — почками. Моча содержит главным образом метаболиты вследствие минимальной почечной экскреции исходного соединения.
Фармакокинетические параметры луразидона линейны в диапазоне общей суточной дозы от 20 до 160 мг. Равновесная концентрация Css луразидона достигается в течение 7 дней с момента начала терапии.