Interested Article - Сульфат бериллия

- 2021-05-05
- 1
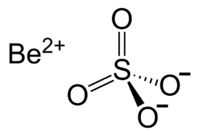
Сульфа́т бери́ллия — химическое соединение с формулой Be SO 4 . Белое твёрдое кристаллическое вещество. Впервые было обнаружено в 1815 году Якобом Берцелиусом .
Применение
Смесь сульфатов бериллия и радия использовалась как источник нейтронов в атомных реакторах. Также очень редко применяются в гомеопатии .
Получение
Сульфат бериллия может быть получен взаимодействием в водном растворе любой соли бериллия с серной кислотой с последующим выпариванием и кристаллизацией продукта реакции. Получаемый гидрат может быть разложен на воду и безводную соль при нагревании до 400 °C .
Химические свойства
- Разлагается при высокой температуре до оксида бериллия :
- С кипящей водой реагирует, образуя осадок основной соли :
- В концентрированном аммиачном растворе образует гидроксид бериллия :
Примечания
- ↑ Для тетрагидрата
- При 30 °C
- Ch. L. Parsons — The Chemistry and Literature of Beryllium S. 33 ff. (1909, London)
- Pradyot Patnaik. Handbook of Inorganic Chemicals . McGraw-Hill, 2002, ISBN 0070494398
- , с. 54.
Литература
- Лидин Р. А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0 .
- 2021-05-05
- 1
![{\displaystyle {\mathsf {BeSO_{4}\ {\xrightarrow[{}]{547-600^{o}C}}\ BeO+SO_{3}}}}](/images/000/799/799150/3.jpg?rand=746506)
![{\displaystyle {\mathsf {2BeSO_{4}+2H_{2}O\ {\xrightarrow[{}]{100^{o}C}}\ Be_{2}SO_{4}(OH)_{2}\downarrow +H_{2}SO_{4}}}}](/images/000/799/799150/4.jpg?rand=149631)
![{\displaystyle {\mathsf {BeSO_{4}+2NH_{3}*H_{2}O\ {\xrightarrow[{}]{}}\ Be(OH)_{2}\downarrow +(NH_{4})_{2}SO_{4}}}}](/images/000/799/799150/5.jpg?rand=523021)