Interested Article - Дифтордихлорметан

- 2021-10-07
- 1
Дифтордихлорметáн (он же дихлордифторметáн , фреóн R 12, фреóн-12, хладóн-12, CFC-12 , арктóн 6, R-12) — органическое вещество , производное метана , полностью замещённый галогеналкан , фреон с формулой C Cl 2 F 2 . При нормальных условиях представляет собой бесцветный негорючий газ, при высокой концентрации имеет лёгкий эфироподобный запах.
Является сильным разрушающим озоновый слой в атмосфере Земли агентом, в связи с чем его производство и использование в 1989 году было запрещено в развитых странах (странах, не подпадающих под действие статьи 5 Монреальского протокола ) .
Получение
Получают взаимодействием четыреххлористого углерода с фтороводородом в присутствии пентахлорида сурьмы в качестве катализатора :
- .
Побочными продуктами этой реакции являются трихлорфторметан ( ), ( ) и тетрафторметан ( ).
Физические свойства
При нормальных условиях представляет собой тяжёлый, примерно в 4 раза тяжелее воздуха, бесцветный газ, со слабым эфирным запахом.
Ниже −29,8 °C при атмосферном давлении сжижается в бесцветную жидкость.
Растворяется в большинстве органических растворителей .
Применение
Используется как холодильный агент и в качестве пропеллента в аэрозольных баллонах .
Влияние на экологию
Дифтордихлорметан обладает высокой озоноразрушающей активностью, образуя озоновые дыры . Поэтому его производство и использование ограничено Монреальским протоколом . К 1994 году был в основном заменён тетрафторэтаном .
Коэффициент возможности истощения озонового слоя (ODP) 0,9 (CCl 3 F = 1). Потенциал глобального потепления (GWP) 8500 ( CO 2 = 1) .
-
 Рост концентрации CFC-12 в атмосфере
Рост концентрации CFC-12 в атмосфере -
 Карта концентраций CFC-12 на уровне моря, 1990 год
Карта концентраций CFC-12 на уровне моря, 1990 год -
 Карта концентраций CFC-12 над океаном, 1990 год
Карта концентраций CFC-12 над океаном, 1990 год -
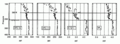 Вертикальные профили концентраций CFC-12, CFC-11, H-1211 и SF6
Вертикальные профили концентраций CFC-12, CFC-11, H-1211 и SF6
Опасность для здоровья
Оказывает раздражающее действие на органы дыхания, снижает сократительную способность миокарда , артериальное давление , нарушает сердечную проводимость, повышает сопротивление лёгочных сосудов, угнетает центральную нервную систему .
Острые отравления обычно связаны как с действием самого вещества, так и продуктов его разложения (при термическом разложении при нагревании выше 150 °C образуется фосген , в присутствии кислорода разлагается с выделением хлороводородной и фтороводородной кислот, карбонилгалогенидов).
При лёгких отравлениях пострадавшие жалуются на головную боль, головокружения, слабость, тошноту , рвоту , иногда повышенную сонливость. Это состояние длится от нескольких часов до 1—2 суток. В более тяжёлых случаях возможны жалобы на раздражение слизистых глаз и верхних дыхательных путей, сухость в носоглотке, ощущение удушья, тремор рук и ног, обморочное состояние, слуховые галлюцинации .
Ингаляционное воздействие приводит к раздражению слизистых поверхностей глаз и верхних дыхательных путей . При попадании на кожу возникают ожоги.
Хронические, подострые и острые отравления наносят необратимый вред здоровью.
Контакт с некоторыми химически активными металлами может привести к взрыву при определённых условиях. (например, при повышенные температуры и/или давления).
Примечания
- ↑ (неопр.) Дата обращения: 21 февраля 2021. 24 октября 2018 года.
- ↑ (неопр.) . Дата обращения: 21 февраля 2021. 3 марта 2021 года.
- name=
- name=
- ↑
- ↑ (англ.) — CRC Press , 1993. — ISBN 978-0-8493-4498-5
- 1:Update on Ozone-Depleting Substances (ODSs) and Other Gases of Interest to the Montreal Protocol // . — Global Ozone Research and Monitoring Project–Report No. 58. — Geneva, Switzerland : World Meteorological Organization, 2018. — P. 1.10. — ISBN 978-1-7329317-1-8 . (неопр.) . Дата обращения: 21 февраля 2021. Архивировано 5 марта 2021 года.
- Гринвуд Н. Н., Эрншоу А. Химия элементов в 2-х т. — М. : Бином. Лаборатория знаний, 2015.
См. также
- 2021-10-07
- 1
 .
.
 ), (
), (
 ) и
) и
 ).
).