Interested Article - Аминокислоты
- 2020-01-11
- 1

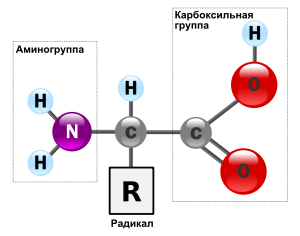
Аминокисло́ты , также аминокарбо́новые кисло́ты , АМК — органические соединения , в молекуле которых одновременно содержатся карбоксильные и аминные группы. Основные химические элементы аминокислот — это углерод (C), водород (H), кислород (O) и азот (N), хотя другие элементы также встречаются в радикале определенных аминокислот. Известны около 500 встречающихся в природе аминокислот (хотя только 21 используется в генетическом коде). Аминокислоты могут рассматриваться как производные карбоновых кислот , в которых один или несколько атомов водорода заменены на аминогруппы.
История
Большинство из около 500 известных аминокислот было открыто после 1953 года, в том числе во время поиска новых антибиотиков в среде микроорганизмов, грибов, семян, растений, фруктов и жидкостях животных. Примерно 240 из них встречаются в природе в свободном виде, а остальные — только как промежуточные элементы обмена веществ .
Открытие аминокислот в составе белков
Жирным шрифтом выделены незаменимые аминокислоты .
| Аминокислота | Аббревиатура | Год | Источник | Впервые выделен |
|---|---|---|---|---|
| Глицин | Gly, G | 1820 | Желатин | А. Браконно |
| Лейцин | Leu, L | 1820 | Мышечные волокна | А. Браконно |
| Тирозин | Tyr, Y | 1848 | Казеин | Ю. фон Либих |
| Серин | Ser, S | 1865 | Шёлк | |
| Глутаминовая кислота | Glu, E | 1866 | Растительные белки | |
| Глутамин | Gln, Q | 1877 | Пшеничная мука | Э. Шулце |
| Аспарагиновая кислота | Asp, D | 1868 | Конглутин, легумин (ростки спаржи ) | |
| Аспарагин | Asn, N | 1806 | Сок спаржи | Л.-Н. Воклен и П. Ж. Робике |
| Фенилаланин | Phe, F | 1881 | Ростки люпина | Э. Шульце , Й. Барбьери |
| Аланин | Ala, A | 1888 | Фиброин шёлка | А. Штреккер , Т. Вейль |
| Лизин | Lys, K | 1889 | Казеин | Э. Дрексель |
| Аргинин | Arg, R | 1895 | Вещество рога | С. Гедин |
| Гистидин | His, H | 1896 | Стурин, гистоны | А. Коссель , С. Гедин |
| Цистеин | Cys, C | 1899 | Вещество рога | К. Мёрнер |
| Валин | Val, V | 1901 | Казеин | Э. Фишер |
| Пролин | Pro, P | 1901 | Казеин | Э. Фишер |
| Гидроксипролин | Hyp, hP | 1902 | Желатин | Э. Фишер |
| Триптофан | Trp, W | 1902 | Казеин | Ф. Хопкинс , Д. Кол |
| Изолейцин | Ile, I | 1904 | Фибрин | Ф. Эрлих |
| Метионин | Met, M | 1922 | Казеин | Д. Мёллер |
| Треонин | Thr, T | 1925 | Белки овса | С. Шрайвер и другие |
| Гидроксилизин | Hyl, hK | 1925 | Белки рыб | С. Шрайвер и другие |
Физические свойства
По физическим свойствам аминокислоты резко отличаются от соответствующих кислот и оснований . Все они кристаллические вещества, лучше растворяются в воде, чем в органических растворителях , имеют достаточно высокие температуры плавления; многие из них имеют сладкий вкус. Эти свойства отчётливо указывают на солеобразный характер этих соединений. Особенности физических и химических свойств аминокислот обусловлены их строением — присутствием одновременно двух противоположных по свойствам функциональных групп: кислотной и основной .
Общие химические свойства
Все аминокислоты — амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы — C O O H , так и основные свойства, обусловленные аминогруппой — N H 2 . Аминокислоты взаимодействуют с кислотами и щелочами :
- N H 2 — C H 2 — C O O H + H Cl → H Cl · N H 2 — C H 2 — C O O H ( Хлороводородная соль глицина )
- N H 2 — C H 2 — C O O H + Na O H → H 2 O + N H 2 — C H 2 — C O O Na (натриевая соль глицина )
Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов , то есть находятся в состоянии внутренних солей.
При определенных условиях могут быть заряжены все три ионогенные группы (нипример у гистидина), тогда они образуют двойные соли . Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов .
Важной особенностью аминокислот является их способность к поликонденсации , приводящей к образованию полиамидов , в том числе пептидов , белков , нейлона , капрона .
Реакция образования пептидов :
- H O O C — C H 2 — N H — H + H O O C — C H 2 — N H 2 → H O O C — C H 2 — N H — C O — C H 2 — N H 2 + H 2 O
Изоэлектрической точкой аминокислоты называют значение pH , при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов .
Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH 3 + , а карбоксигруппа — в виде -COO − . Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот.
Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе .
Получение
Большинство аминокислот можно получить в ходе гидролиза белков или как результат химических реакций:
- C H 3 C O O H + Cl 2 + (катализатор) → C H 2 Cl C O O H + H Cl ; C H 2 Cl C O O H + 2 N H 3 → N H 2 — C H 2 C O O H + N H 4 Cl
Оптическая изомерия
Все входящие в состав живых организмов α-аминокислоты, кроме глицина , содержат асимметрический атом углерода ( треонин и изолейцин содержат два асимметрических атома) и обладают оптической активностью. Почти все встречающиеся в природе α-аминокислоты имеют L-конфигурацию, и только они включаются в состав белков, синтезируемых на рибосомах .
D-аминокислоты в живых организмах
Аспарагиновые остатки в метаболически неактивных структурных белках претерпевают медленную самопроизвольную неферментативную рацемизацию: в белках дентина и эмали зубов L-аспартат переходит в D-форму со скоростью ~0,1 % в год , что может быть использовано для определения возраста млекопитающих. Рацемизация аспартата также отмечена при старении коллагена ; предполагается, что такая рацемизация специфична для аспарагиновой кислоты и протекает за счёт образования сукцинимидного кольца при внутримолекулярном ацилировании атома азота пептидной связи свободной карбоксильной группой аспарагиновой кислоты .
С развитием следового аминокислотного анализа были обнаружены сначала в составе клеточных стенок некоторых бактерий ( 1966 ), а затем — и в тканях высших организмов . Так, D-аспартат и D-метионин предположительно являются нейромедиаторами у млекопитающих .
В состав некоторых пептидов входят D-аминокислоты, образующиеся при посттрансляционной модификации . Например, D- метионин и D- аланин входят в состав опиоидных гептапептидов кожи южноамериканских амфибий филломедуз ( , и ). Наличие D-аминокислот определяет высокую биологическую активность этих пептидов как анальгетиков .
Сходным образом образуются пептидные антибиотики бактериального происхождения, действующие против грамположительных бактерий — низин , субтилин и эпидермин .
Гораздо чаще D-аминокислоты входят в состав пептидов и их производных, образующихся путём в клетках грибов и бактерий. Видимо, в этом случае исходным материалом для синтеза служат также L-аминокислоты, которые изомеризуются одной из субъединиц ферментного комплекса, осуществляющего синтез пептида .
Протеиногенные аминокислоты
В процессе биосинтеза белка в полипептидную цепь включаются 20 α-аминокислот, кодируемых генетическим кодом . Помимо этих аминокислот, называемых протеиногенными , или стандартными , в некоторых белках присутствуют специфические нестандартные аминокислоты , возникающие из стандартных в процессе посттрансляционных модификаций. В последнее время к протеиногенным аминокислотам иногда причисляют трансляционно включаемые селеноцистеин (Sec, U) и пирролизин (Pyl, O) . Это так называемые 21-я и 22-я аминокислоты .
Вопрос, почему именно эти 20 аминокислот стали «избранными», остаётся нерешённым . Не совсем ясно, чем эти аминокислоты оказались предпочтительнее других похожих. Например, ключевым промежуточным метаболитом пути биосинтеза треонина , изолейцина и метионина является α-аминокислота гомосерин. Очевидно, что гомосерин — очень древний метаболит , но для треонина , изолейцина и метионина существуют аминоацил-тРНК-синтетазы , тРНК , а для гомосерина — нет.
Структурные формулы 20 протеиногенных аминокислот обычно приводят в виде так называемой таблицы протеиногенных аминокислот :
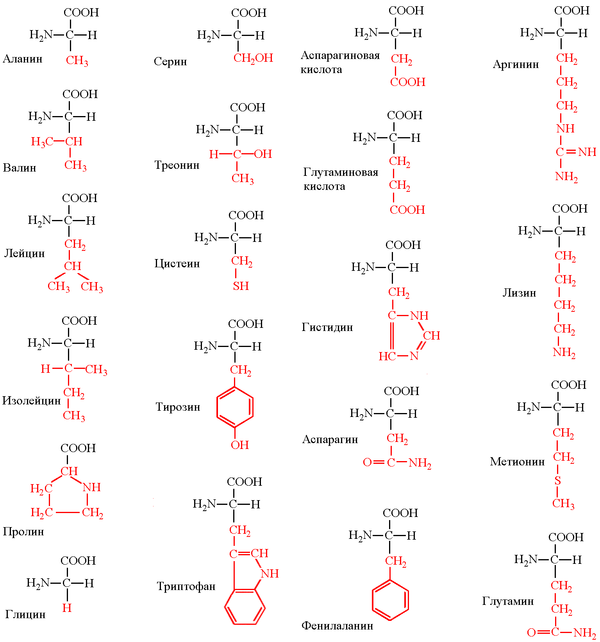
Классификация
| Аминокислота | 3-буквы | 1-буква | Генетический код |
Мнемоническое
правило |
Полярность | Класс по радикалу | Mr |
V
w
(Å 3 ) |
pI | Гидрофобность | Частота в белках (%) |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Глицин | Gly | G | GGU, GGC, GGA, GGG | G lycine | Неполярные | Алифатические | 75,067 | 48 | 6,06 | −0,4 | 7,03 |
| Аланин | Ala | A | GCU, GCC, GCA, GCG | A lanine | Неполярные | Алифатические | 89,094 | 67 | 6,01 | 1,8 | 8,76 |
| Валин | Val | V | GUU, GUC, GUA, GUG | V aline | Неполярные | Алифатические | 117,148 | 105 | 6,00 | 4,2 | 6,73 |
| Изолейцин | Ile | I | AUU, AUC, AUA | I soleucine | Неполярные | Алифатические | 131,175 | 124 | 6,05 | 4,5 | 5,49 |
| Лейцин | Leu | L | UUA, UUG, CUU, CUC, CUA, CUG | L eucine | Неполярные | Алифатические | 131,175 | 124 | 6,01 | 3,8 | 9,68 |
| Пролин | Pro | P | CCU, CCC, CCA, CCG | P roline | Неполярные | Гетероциклические | 115.132 | 90 | 6,30 | −1,6 | 5,02 |
| Серин | Ser | S | UCU, UCC, UCA, UCG, AGU, AGC | S erine | Полярные | Оксимоноаминокарбоновые | 105,093 | 73 | 5,68 | −0,8 | 7,14 |
| Треонин | Thr | T | ACU, ACC, ACA, ACG | T hreonine | Полярные | Оксимоноаминокарбоновые | 119,119 | 93 | 5,60 | −0,7 | 5,53 |
| Цистеин | Cys | C | UGU, UGC | C ysteine | Полярные | Серосодержащие | 121,154 | 86 | 5,05 | 2,5 | 1,38 |
| Метионин | Met | M | AUG | M ethionine | Неполярные | Серосодержащие | 149,208 | 124 | 5,74 | 1,9 | 2,32 |
| Аспарагиновая | Asp | D | GAU, GAC | aspar D ic acid | Полярные | заряженные отрицательно | 133,104 | 91 | 2,85 | −3,5 | 5,49 |
| Аспарагин | Asn | N | AAU, AAC | asparagi N e | Полярные | Амиды | 132,119 | 96 | 5,41 | −3,5 | 3,93 |
| Глутаминовая | Glu | E | GAA, GAG | glu E tamic acid | Полярные | заряженные отрицательно | 147,131 | 109 | 3,15 | −3,5 | 6,32 |
| Глутамин | Gln | Q | CAA, CAG | Q -tamine | Полярные | Амиды | 146,146 | 114 | 5,65 | −3,5 | 3,9 |
| Лизин | Lys | K | AAA, AAG | before L | Полярные | заряженные положительно | 146,189 | 135 | 9,60 | −3,9 | 5,19 |
| Аргинин | Arg | R | CGU, CGC, CGA, CGG, AGA, AGG | a R ginine | Полярные | заряженные положительно | 174.203 | 148 | 10,76 | −4,5 | 5,78 |
| Гистидин | His | H | CAU, CAC | H istidine |
Полярные
заряженные положительно |
Гетероциклические | 155,156 | 118 | 7,60 | −3,2 | 2,26 |
| Фенилаланин | Phe | F | UUU, UUC | F enylalanine | Неполярные | Ароматические | 165,192 | 135 | 5,49 | 2,8 | 3,87 |
| Тирозин | Tyr | Y | UAU, UAC | t Y rosine | Полярные | Ароматические | 181,191 | 141 | 5,64 | −1,3 | 2,91 |
| Триптофан | Trp | W | UGG | t W o rings | Неполярные |
Ароматические,
Гетероциклические |
204,228 | 163 | 5,89 | −0,9 | 6,73 |
По радикалу
- Неполярные: глицин , аланин , валин , изолейцин , лейцин , пролин
- Полярные незаряженные (заряды скомпенсированы) при pH=7: серин , треонин , цистеин , метионин , аспарагин , глутамин
- Ароматические: фенилаланин , триптофан , тирозин
- Полярные заряженные отрицательно при pH=7: аспартат , глутамат
- Полярные заряженные положительно при pH=7: лизин , аргинин , гистидин
По функциональным группам
-
Алифатические
- Моноаминомонокарбоновые: глицин , аланин , валин , изолейцин , лейцин
- Оксимоноаминокарбоновые: серин , треонин
- Моноаминодикарбоновые: аспартат , глутамат , за счёт второй карбоксильной группы несут в растворе отрицательный заряд
- Амиды моноаминодикарбоновых: аспарагин , глутамин
- Диаминомонокарбоновые: лизин , аргинин , несут в растворе положительный заряд
- Серосодержащие: цистеин , метионин
- Ароматические : фенилаланин , тирозин , триптофан ,
- Гетероциклические : триптофан , гистидин , пролин
- : пролин
По классам аминоацил-тРНК-синтетаз
- Класс I: валин , изолейцин , лейцин , цистеин , метионин , глутамат , глутамин , аргинин , тирозин , триптофан
- Класс II: глицин , аланин , пролин , серин , треонин , аспартат , аспарагин , гистидин , фенилаланин
Для аминокислоты лизин существуют аминоацил-тРНК-синтетазы обоих классов.
По путям биосинтеза
Пути биосинтеза протеиногенных аминокислот разноплановы. Одна и та же аминокислота может образовываться разными путями. К тому же совершенно различные пути могут иметь очень похожие этапы. Тем не менее, имеют место и оправданы попытки классифицировать аминокислоты по путям их биосинтеза . Существует представление о следующих биосинтетических семействах аминокислот: аспартата , глутамата , серина , пирувата и пентоз . Не всегда конкретную аминокислоту можно однозначно отнести к определённому семейству; делаются поправки для конкретных организмов и учитывая преобладающий путь. По семействам аминокислоты обычно распределяют следующим образом:
- Семейство аспартата: аспартат , аспарагин , треонин , изолейцин , метионин , лизин .
- Семейство глутамата: глутамат , глутамин , аргинин , пролин .
- Семейство пирувата: аланин , валин , лейцин .
- Семейство серина: серин , цистеин , глицин .
- Семейство пентоз: гистидин , фенилаланин , тирозин , триптофан .
Фенилаланин , тирозин , триптофан иногда выделяют в семейство шикимата .
По способности организма синтезировать из предшественников
Классификация аминокислот на заменимые и незаменимые не лишена недостатков. К примеру, тирозин является заменимой аминокислотой только при условии достаточного поступления фенилаланина. Для больных фенилкетонурией тирозин становится незаменимой аминокислотой. Аргинин синтезируется в организме человека и считается заменимой аминокислотой, но в связи с некоторыми особенностями его метаболизма при определённых физиологических состояниях организма может быть приравнен к незаменимым. Гистидин также синтезируется в организме человека, но не всегда в достаточных количествах, потому должен поступать с пищей.
По характеру катаболизма у животных
Биодеградация аминокислот может идти разными путями.
По характеру продуктов катаболизма у животных протеиногенные аминокислоты делят на три группы:
- Глюкогенные — при распаде дают метаболиты , не повышающие уровень кетоновых тел , способные относительно легко становиться субстратом для глюконеогенеза : пируват , α-кетоглутарат , сукцинил-KoA, фумарат , оксалоацетат
- Кетогенные — распадаются до ацетил-KoA и ацетоацетил-KoA, повышающие уровень кетоновых тел в крови животных и человека и преобразующиеся в первую очередь в липиды
- Глюко-кетогенные — при распаде образуются метаболиты обоих типов
Аминокислоты:
- Глюкогенные: глицин , аланин, валин , пролин , серин , треонин , цистеин , метионин , аспартат , аспарагин , глутамат , глутамин , аргинин , гистидин .
- Кетогенные: лейцин , лизин .
- Глюко-кетогенные (смешанные): изолейцин , фенилаланин, тирозин , триптофан .
«Миллеровские» аминокислоты
«Миллеровские» аминокислоты — обобщенное название аминокислот, получающихся в условиях, близких к эксперименту Стенли Л. Миллера 1953 года . Установлено образование в виде рацемата множества различных аминокислот, в том числе: глицин , аланин, валин , изолейцин , лейцин , пролин , серин , треонин , аспартат , глутамат
Родственные соединения
В медицине ряд веществ, способных выполнять некоторые биологические функции аминокислот, также называют аминокислотами: [ источник не указан 847 дней ]
Применение
Важной особенностью аминокислот является их способность к поликонденсации , приводящей к образованию полиамидов , в том числе пептидов , белков , нейлона , капрона , энанта .
Аминокислоты входят в состав спортивного питания и комбикорма . Аминокислоты применяются в пищевой промышленности в качестве вкусовых добавок , например, натриевая соль глутаминовой кислоты .
Примечания
- ↑ Wagner I., Musso H. New Naturally Occurring Amino Acids (нем.) // Angewandte Chemie International Edition in English : magazin. — 1983. — November ( Bd. 22 , Nr. 11 ). — S. 816—828 . — doi : .
- S. Hansen. . — 2015. 15 июня 2016 года.
- Овчинников Ю. А. «Биоорганическая химия» М:Просвещение, 1987. — 815 с., стр. 25.
- ↑ (англ.) // Wikipedia. — 2019-02-14.
- Карпов В. Л. // Природа . — Наука , 2005. — № 3 . — С. 34—43 . 10 февраля 2018 года.
- ↑ Anton P. Novikov, Alexey V. Safonov, Konstantin E. German, Mikhail S. Grigoriev. (англ.) // CrystEngComm. — 2023-12-01. — ISSN . — doi : .
- Helfman, P M; J L Bada. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1975. — Vol. 72 , no. 8 . — P. 2891—2894 . 4 сентября 2017 года.
- CLOOS P; FLEDELIUS C.: (1 февраля 2000). Дата обращения: 5 сентября 2011. 2 февраля 2012 года.
- J. van Heijenoort. // Glycobiology. — 2001-3. — Т. 11 , вып. 3 . — С. 25R—36R . — ISSN . 20 августа 2018 года.
- Herman Wolosker, Elena Dumin, Livia Balan, Veronika N. Foltyn. // The FEBS journal. — 2008-7. — Т. 275 , вып. 14 . — С. 3514—3526 . — ISSN . — doi : . 15 сентября 2018 года.
- H. Brötz, M. Josten, I. Wiedemann, U. Schneider, F. Götz. // Molecular Microbiology. — 1998-10. — Т. 30 , вып. 2 . — С. 317—327 . — ISSN . 20 августа 2018 года.
- Linda Johansson, Guro Gafvelin, Elias S.J. Arnér. // Biochimica et Biophysica Acta (BBA) - General Subjects. — 2005-10. — Т. 1726 , вып. 1 . — С. 1—13 . — ISSN . — doi : . 5 июля 2018 года.
- Joseph A. Krzycki. // Current Opinion in Microbiology. — 2005-12. — Т. 8 , вып. 6 . — С. 706—712 . — ISSN . — doi : . 20 августа 2018 года.
- Alexandre Ambrogelly, Sotiria Palioura, Dieter Söll. // Nature Chemical Biology. — 2007-1. — Т. 3 , вып. 1 . — С. 29—35 . — ISSN . — doi : . 20 августа 2018 года.
- Andrei S. Rodin, Eörs Szathmáry, Sergei N. Rodin. // Biology Direct. — 2011-02-22. — Т. 6 . — С. 14 . — ISSN . — doi : . 15 июня 2018 года.
- ↑ Cooper, Geoffrey M. . — 3rd ed. — Washington, D.C.: ASM Press, 2004. — xx, 713 pages с. — ISBN 0878932143 , 9780878932146, 0878930760, 9780878930760.
- Р. Б. Соловьев, учитель биологии. от 18 апреля 2018 на Wayback Machine
- ↑ Березов Т.Т., Коровкин Б.Ф. Классификация аминокислот // Биологическая химия. — 3-е изд., перераб. и доп.. — М. : Медицина, 1998. — 704 с. — ISBN 5-225-02709-1 .
- J. Kyte, R. F. Doolittle. // Journal of Molecular Biology. — 1982-05-05. — Т. 157 , вып. 1 . — С. 105—132 . — ISSN . 6 июля 2018 года.
- Lukasz P. Kozlowski. // Nucleic Acids Research. — 2017-01-04. — Т. 45 , вып. D1 . — С. D1112—D1116 . — ISSN . — doi : . 2 июля 2018 года.
- Fumio Sanda, Takeshi Endo. (англ.) // Macromolecular Chemistry and Physics. — Vol. 200 , iss. 12 . — ISSN . — doi : .
- Садовникова М. С., Беликов В. М. Пути применения аминокислот в промышленности. // Успехи химии . 1978. Т. 47. Вып. 2. С. 357―383.
Литература
- / Липкин В. М. , Родионов И. Л. // Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов . — М. : Большая российская энциклопедия, 2004—2017.
- Збарский И. Б. , Симакова Р. А., Будковская Н. Г. // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский . — 3-е изд. — М. : Советская энциклопедия , 1974. — Т. 1 : А — Антибиоз. — 576 с. : ил.
-
Эксперименты Миллера-Юри
и обсуждения:
- Miller S. L. Production of amino acids under possible primitive earth conditions. Science, v. 117, May 15, 1953
- Miller S. L. and H. C. Urey. Organic compound synthesis on the primitive earth. Science, v. 130, July 31, 1959
- Miller Stanley L. and Leslie E. Orgel. The origins of life on the earth. Englewood Cliffs, NJ, Prentice-Hall, 1974.
- Общая биология. Учебник для 9 — 10 классов средней школы. Под ред. Ю. И. Полянского. Изд. 17-е, перераб. — М.: Просвещение, 1987. — 288с.
- Аминокислоты, пептиды, белки. Под ред. Ю. В. Митина
- // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб. , 1890—1907.
Ссылки
- 2020-01-11
- 1