Interested Article - Тиомочевина

- 2021-07-06
- 1
Тиомочевина — CS(NH 2 ) 2 — диамид тиоугольной кислоты, тиокарбамид, белые кристаллы горького вкуса и запахом жареного лука, t пл 180—182 °C (при быстром нагревании; при медленном — разлагается); умеренно растворима в воде, метаноле, пиридине, хорошо — в 50 %-ном водном пиридине.
Тиомочевину применяют в органическом синтезе , для получения лекарственных препаратов (напр., сульфидина ).
Синтез
Тиомочевина может быть получена изомеризацией роданида аммония, этот синтез аналогичен классическому синтезу мочевины из цианата аммония (кислородного аналога роданида) по Вёлеру :
Вместе с тем, в отличие от мочевины, тиомочевина при нагревании находится в равновесии с роданидом аммония : равновесная смесь при температуре 140 °C содержит 28,1 % тиомочевины, при 156 °C — 26,7 %, при 180 °C — 21,8 % .
Подобно синтезу мочевины из аммиака и диоксида углерода, тиомочевина также может быть синтезирована при взаимодействии аммиака и сероуглерода:
Тиомочевину также получают взаимодействием H 2 S или сульфидов аммония либо щелочных металлов с цианамидом кальция CaCN 2 в водных растворах:
Реакционная способность
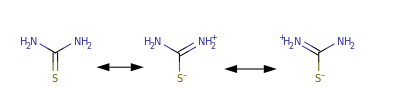
Структура молекулы тиомочевины может быть представлена мезомерными канонической тиоамидной формой и тиоимидными формами, несущими отрицательный заряд на атоме серы и положительный на атомах азота амидинового фрагмента:
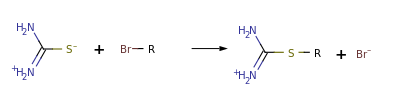
В результате атом серы является сильным нуклеофильным центром и тиомочевина протонируется по атому серы с образованием солей с сильными кислотами. Атаки мягких электрофилов также направляются на атом серы: тиомочевина алкилируется алкилгалогенидами и алкилсульфатами с образованием изотиурониевых солей:
Аналогично протекает реакция тиомочевины с арилдиазониевыми солями.
S-алкилирование тиомочевины также является первой стадией её взаимодействия с эпоксидами , ведущего к образованию (эписульфидов) :
Ацилирование тиомочевины галогенангидридами и ангидридами карбоновых кислот, в зависимости от условий реакции, может протекать как по сере (в мягких условиях), так и по азоту (в жестких условиях).
Альдегиды и кетоны с присоединяются к тиомочевине, образуя гидроксиалкилтиомочевины, которые при отщеплении воды превращаются в N-тиокарбамоилимины:
- H 2 NC(S)NH 2 + R 2 CO H 2 NC(S)NHC(OH)R 2
- H 2 NC(S)NHC(OH)R 2 H 2 NC(S)N=CR 2
Тиомочевина реагирует с бифункциональными электрофилами, образуя гетероциклические соединения. Так, например, с α-галогенкетонами тиомочевина (и её N-замещенные производные)образует 2-аминотиазолы:
при взаимодействии с 1,3-дикарбонильными соединениями - 2-меркаптопиримидины:
Применение
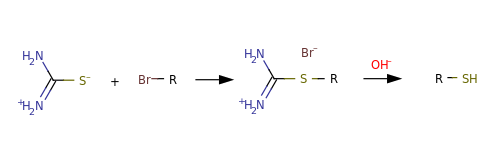
Алкилирование тиомочевины используется алкилирование с образованием алкилтиурониевых солей и их последующим щелочным гидролизом: используется как препаративный метод синтеза алифатических тиолов :
Преимуществом этого метода являются легкая очистка перекристаллизацией тиурониевых солей и достаточно высокие общие выходы тиолов.
Алкилтиурониевые соли также используются для синтеза как гуанидина аммонолизом, так и алкилгуанидинов взаимодействием с аминами в щелочной среде :
- Et-S-C(NH 2 ) 2 + + R-NH 2 R-NHC(=NH)NH 2 + EtSH + H + ,
синтеза алкилсульфонилхлоридов путем окислениея их N-хлорсукцинимидом (NCS) :
- R-S-C(NH 2 ) 2 + Cl - + NCS R-SO 2 Cl ,
Тиомочевина широко используется в синтезе гетероциклических соединений (тиобарбитураты конденсацией с малоновыми эфирами, 2-меркаптопитимидинов при конденсации с ацеталями малонового диальдегида , 2-аминотиазолов конденсацией с α-галогенкетонами ).
Тиомочевина также используется в качестве ингибитора кислотной коррозии сталей .
Примечания
- Тиомочевина // Большая Химическая Энциклопедия
- Zeynizadeh, Behzad; Samal Yeghaneh. Solvent-Free Conversion of Epoxides to Thiiranes by Thiourea/NH4Cl System (англ.) // Phosphorus, Sulfur, and Silicon and the Related Elements : journal. — 2008. — Vol. 183 , no. 9 . — P. 2280—2286 . — doi : .
- от 20 июля 2019 на Wayback Machine DOI: 10.15227/orgsyn.021.0036
- от 20 июля 2019 на Wayback Machine DOI: 10.15227/orgsyn.022.0059
- от 2 июня 2018 на Wayback Machine DOI: 10.15227/orgsyn.091.0116
- от 2 июня 2018 на Wayback Machine DOI: 10.15227/orgsyn.043.0068
- от 2 июня 2018 на Wayback Machine DOI: 10.15227/orgsyn.019.0010
Литература
- О. Я. Нейланд. Органическая химия. — М. : Высшая школа, 1990. — 751 с. — 35 000 экз. — ISBN 5-06-001471-1 .
- 2021-07-06
- 1