Жидкий водород
- 1 year ago
- 0
- 0
| 1 |
Водород
|
|
|
|
| 1s 1 | |
Водоро́д ( химический символ — H , от лат. hydrogenium ) — химический элемент первого периода периодической таблицы химических элементов Д. И. Менделеева , с атомным номером 1.
Одноатомная форма водорода — самое распространённое химическое вещество во Вселенной , составляющее примерно 75 % всей барионной массы. Звёзды, кроме компактных , в основном состоят из водородной плазмы . Самый лёгкий из элементов периодической таблицы.
Три изотопа водорода имеют собственные названия : 1 H — протий , 2 H — дейтерий и 3 H — тритий ( радиоактивен ). Ядро самого распространённого изотопа — протия — состоит из одного только протона и не содержит нейтронов .
При стандартной температуре и давлении водород — бесцветный, не имеющий запаха и вкуса , нетоксичный двухатомный газ (химическая формула — H 2 ), который в смеси с воздухом или кислородом горюч и крайне пожаро- и взрывоопасен . В присутствии других окисляющих газов, например фтора или хлора , водород также взрывоопасен. Поскольку водород охотно формирует ковалентные связи с большинством неметаллов , большая часть водорода на Земле существует в молекулярных соединениях, таких как вода или органические вещества . Водород играет особенно важную роль в кислотно-основных реакциях .
Растворим в этаноле и ряде металлов : железе , никеле , палладии , титане , платине , ниобии .
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в XVI и XVII веках на заре становления химии как науки. Впервые водород получил Парацельс , погружая железные опилки в серную кислоту в XVI веке.
В 1671 году Роберт Бойль подробно описал реакцию между железными опилками и разбавленными кислотами, при которой выделяется газообразный водород .
В 1766 году Генри Кавендиш был первым, кто признал газообразный водород индивидуальным элементом, назвав газ, выделяющийся при реакции металла с кислотой, «горючим воздухом». Он предположил, что «горючий воздух» идентичен гипотетическому веществу, называемому « флогистон », и в 1781 году обнаружил, что при его сгорании образуется вода .
Прямо указывал на выделение водорода и Михаил Ломоносов , но он уже понимал, что это не флогистон .
Французский химик Антуан Лавуазье совместно с инженером Жаном Мёнье , используя специальные газометры, в 1783 году осуществил синтез воды, а затем и её анализ, разложив водяной пар раскалённым железом. Так он установил, что «горючий воздух» входит в состав воды и может быть из неё получен.
Лавуазье дал водороду название hydrogène (от др.-греч. ὕδωρ — вода и γεννάω — рождаю) — «рождающий воду». В 1801 году последователь Лавуазье, академик Василий Севергин , называл его «водотворное вещество», он писал :
Водотворное вещество в соединении с кислотворным составляет воду. Сие можно доказать, как через разрешение, так и через составление.
Русское наименование «водород» предложил химик Михаил Соловьёв в 1824 году — по аналогии с « кислородом » Ломоносова .
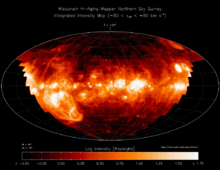
В настоящее время водород — самый распространённый элемент во Вселенной . На его долю приходится около 88,6 % всех атомов (около 11,3 % составляют атомы гелия , доля всех остальных вместе взятых элементов — порядка 0,1 %) . Таким образом, водород — основная составная часть звёзд и межзвёздного газа . Повсеместное возникновение атомарного водорода впервые произошло в эпоху рекомбинации .
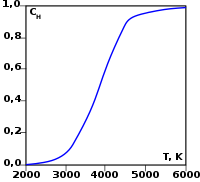
В условиях звёздных температур (например, температура поверхности Солнца ~6000 °C) водород существует в виде плазмы , в межзвёздном пространстве этот элемент существует в виде отдельных молекул , атомов и ионов и может образовывать молекулярные облака, значительно различающиеся по размерам, плотности и температуре.
Массовая доля водорода в земной коре составляет 1 % — это десятый по распространённости элемент. Однако его роль в природе определяется не массой, а числом атомов, доля которых среди остальных элементов составляет 17 % (второе место после кислорода , доля атомов которого равна ~52 %). Поэтому значение водорода в химических процессах, происходящих на Земле , почти так же велико, как и кислорода.
В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях, практически весь водород на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества содержится в атмосфере (0,00005 % по объёму для сухого воздуха ).
Водород входит в состав практически всех органических веществ и присутствует во всех живых клетках, где по числу атомов на водород приходится почти 63 % .
На 2019 год в мире потребляется 75 млн тонн водорода, в основном в нефтепереработке и производстве аммиака . Из них более 3/4 производится из природного газа , для чего расходуется более 205 млрд м 3 газа . Почти все остальное получают из угля. Около 0,1 % (~100 тыс. тонн) вырабатывается электролизом. При производстве водорода в атмосферу поступает ~830 млн тонн CO 2 . Себестоимость водорода, полученного из природного газа, оценивается в 1,5-3 доллара за 1 кг.
В результате данного процесса получается "grey hydrogen", который невозможно применять в топливных элементах, так как примесь CO отравляет катализаторы. Дальше, при его очистке до 10-100 ppm CO, получают "blue hydrogen", но и он отравляет платиновый катализатор.
Дейтероводород получают из тяжёлой воды, которую в настоящее время производят электролитическим обогащением обычной воды. 0,0156 % водорода находится в виде дейтерия.
Перенапряжение выделения H 2 несколько меньше по сравнению с D 2 (хотя зависит от природы материала катода и состава раствора),тяжёлая вода накапливается в электролизере. Применяется каскад электролизёров.
Другие способы получения дейтероводорода: термодиффузия газообразного водорода, диффузия смеси D 2 /H 2 через палладиевый фильтр.
В промышленности реализованы несколько способов очистки водорода из водородосодержащего сырья (так называемый водородсодержащий газ) . Водородсодержащий газ (ВСГ) — это газ с высоким содержанием водорода (10 % и выше). Переход на сжигание водородсодержащих газов — один из способов снижения выбросов углекислого газа в атмосферу.
Стоимость водорода при крупнооптовых поставках колеблется в диапазоне 2—7 USD /кг . В небольших количествах перевозится в стальных баллонах зелёного или тёмно-зелёного цвета.

Водород — самый лёгкий газ: он легче воздуха в 14,5 раз. Поэтому, например, мыльные пузыри , наполненные водородом, на воздухе стремятся вверх . Шары, наполненные водородом, также стремятся вверх. Водород использовался для воздухоплавания, но из-за взрывоопасности от водорода отказались в пользу гелия. Чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа, за счёт чего быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в 7 раз выше теплопроводности воздуха.
Молекула водорода двухатомна — Н 2 . При нормальных условиях это газ без цвета, запаха и вкуса. Плотность 0,08987 г / л ( н. у. ), температура кипения −252,76 °C, удельная теплота сгорания 120,9⋅10 6 Дж / кг , малорастворим в воде — 18,8 мл / л при н.у. Растворимость водорода в воде возрастает с увеличением давления и снижается с увеличением температуры.
Водород хорошо растворим во многих металлах ( Ni , Pt , Pd и др.), особенно в палладии (850 объёмов H 2 на 1 объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре .

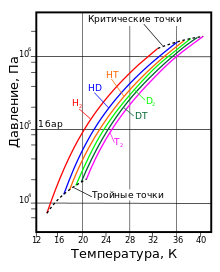
Жидкий водород существует в очень узком интервале температур от −252,76 до −259,2 °C. Это бесцветная жидкость, очень лёгкая ( плотность при −253 °C 0,0708 г / см³ ) и текучая ( вязкость при −253 °C 13,8 сП ). Критические параметры водорода: температура −240,2 °C, давление 12,8 атм , критическая плотность 0,0312 г/см³ и критический объём 66,95—68,9 см³/моль (0,033 м³/кг ). Указанными значениями критических параметров объясняются трудности при ожижении водорода.
В жидком состоянии равновесный водород состоит из 99,79 % пара-Н 2 , 0,21 % орто-Н 2 .
Твёрдый водород , температура плавления −259,2 °C, плотность 0,0807 г/см³ (при −262 °C) — снегоподобная масса, кристаллы гексагональной сингонии , пространственная группа P6/mmc, параметры ячейки a = 0,378 нм и c = 0,6167 нм .
В 1935 году Уингер и Хантингтон высказали предположение о том, что при давлении свыше 250 тысяч атм водород может перейти в металлическое состояние . Получение этого вещества в устойчивом состоянии открывало очень заманчивые перспективы его применения — ведь это был бы сверхлёгкий металл, компонент лёгкого и энергоёмкого ракетного топлива. В 2014 году было установлено, что при давлении порядка 1,5—2,0 млн атм водород начинает поглощать инфракрасное излучение , а это означает, что электронные оболочки молекул водорода поляризуются . Возможно, при ещё более высоких давлениях водород превратится в металл . В 2017 году появилось сообщение о возможном экспериментальном наблюдении перехода водорода в металлическое состояние под высоким давлением .

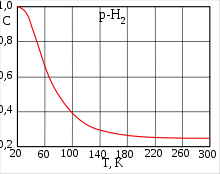
Молекулярный водород существует в двух спиновых формах (модификациях): ортоводород и параводород . Модификации немного различаются по физическим свойствам, оптическим спектрам, также по характеристикам рассеивания нейтронов. В молекуле ортоводорода o -H 2 (англ. о -H 2 ) ( т. пл. −259,10 °C, т. кип. −252,56 °C) спины ядер параллельны, а у параводорода п -H 2 (англ. p -H 2 ) (т. пл. −259,32 °C, т. кип. −252,89 °C) — противоположны друг другу (антипараллельны). Равновесная смесь o -H 2 и п -H 2 при заданной температуре называется равновесным водородом р -H 2 (англ. е -H 2 ) , а смесь 75% орто-водорода и 25% пара-водорода называется нормальным водородом н -H 2 (англ. n -H 2 ).
о- п- кДж
Разделить спиновые изомеры водорода можно адсорбцией на активном угле при температуре жидкого азота . При очень низких температурах равновесие между ортоводородом и параводородом почти нацело сдвинуто в сторону параводорода, так как энергия пара-молекулы немного ниже энергии орто-молекулы. При 80 К соотношение модификаций приблизительно 1:1. Десорбированный с угля параводород при нагревании превращается в ортоводород с образованием равновесной смеси. При комнатной температуре равновесна смесь ортоводорода и параводорода в отношении около 75:25 . Без катализатора взаимное превращение происходит относительно медленно, что даёт возможность изучить свойства обеих модификаций. В условиях разреженной межзвёздной среды характерное время перехода в равновесную смесь очень велико, вплоть до космологических.
Наиболее известны три изотопа водорода: протий 1 H (атомное ядро — протон ), дейтерий 2 Н (ядро состоит из одного протона и одного нейтрона ) и тритий 3 Н (ядро состоит из одного протона и двух нейтронов). Эти изотопы имеют собственные химические символы: протий — H, дейтерий — D, тритий — T.
Протий и дейтерий стабильны. Содержание этих изотопов в природном водороде составляет 99,9885 ± 0,0070 % и 0,0115 ± 0,0070 % соответственно . Оно может незначительно меняться в зависимости от источника и способа получения водорода. Тритий нестабилен, претерпевает бета-распад с периодом 12,32 года , превращаясь в стабильный гелий-3 . Тритий встречается в природе в следовых количествах, образуясь главным образом при взаимодействии космических лучей со стабильными ядрами, при захвате дейтерием тепловых нейтронов и при взаимодействии природного изотопа лития-6 с нейтронами, порождёнными космическими лучами.
Искусственно получены также тяжёлые радиоактивные изотопы водорода с массовыми числами 4—7 и периодами полураспада 10 −21 —10 −23 с .
Природный молекулярный водород состоит из молекул H 2 и HD (дейтероводород) в соотношении 3200:1. Содержание в нём молекул из чистого дейтерия D 2 ещё меньше, отношение концентраций HD и D 2 составляет примерно 6400:1.
Из всех изотопов химических элементов физические свойства изотопов водорода отличаются друг от друга наиболее сильно. Это связано с наибольшим относительным изменением масс атомов .
|
Температура
плавления, K |
Температура
кипения, K |
Тройная
точка |
Критическая
точка |
Плотность,
кг/м³ |
||||
|---|---|---|---|---|---|---|---|---|
| T , K | P , кПа | T , K | P , МПа | жидкий | газ | |||
| H 2 | 13,96 | 20,39 | 13,96 | 7,3 | 32,98 | 1,31 | 70,811 | 1,316 |
| HD | 16,65 | 22,13 | 16,6 | 12,8 | 35,91 | 1,48 | 114,0 | 1,802 |
| HT | 22,92 | 17,63 | 17,7 | 37,13 | 1,57 | 158,62 | 2,31 | |
| D 2 | 18,65 | 23,67 | 18,73 | 17,1 | 38,35 | 1,67 | 162,50 | 2,23 |
| DT | 24.38 | 19,71 | 19,4 | 39,42 | 1,77 | 211,54 | 2,694 | |
| T 2 | 20,63 | 25,04 | 20,62 | 21,6 | 40,44 | 1,85 | 260,17 | 3,136 |
Молекулы чистых протия, дейтерия и трития могут существовать в двух аллотропных модификациях (отличающихся взаимной ориентацией спинов ядер) — орто- и параводород: o -D 2 , p -D 2 , o -T 2 , p -T 2 . Молекулы водорода с другим изотопным составом (HD, HT, DT) не имеют орто- и парамодификаций.
Свойства изотопов водорода представлены в таблице .
| Изотоп | Z | N | Масса, а. е. м. | Период полураспада | Спин | Содержание в природе, % | Тип и энергия распада | |
|---|---|---|---|---|---|---|---|---|
| 1 H | 1 | 0 | 1,007 825 032 07(10) | стабилен | 1 ⁄ 2 + | 99,9885(70) | ||
| 2 H | 1 | 1 | 2,014 101 777 8(4) | стабилен | 1 + | 0,0115(70) | ||
| 3 H | 1 | 2 | 3,016 049 277 7(25) | 12,32(2) года | 1 ⁄ 2 + | β − | 18,591(1) кэВ | |
| 4 H | 1 | 3 | 4,027 81(11) | 1,39(10)⋅10 −22 с | 2 − | -n | 23,48(10) МэВ | |
| 5 H | 1 | 4 | 5,035 31(11) | более 9,1⋅10 −22 с | ( 1 ⁄ 2 + ) | -nn | 21,51(11) МэВ | |
| 6 H | 1 | 5 | 6,044 94(28) | 2,90(70)⋅10 −22 с | 2 − | −3n | 24,27(26) МэВ | |
| 7 H | 1 | 6 | 7,052 75(108) | 2,3(6)⋅10 −23 с | 1 ⁄ 2 + | -nn | 23,03(101) МэВ | |
В круглых скобках приведено среднеквадратическое отклонение значения в единицах последнего разряда соответствующего числа.
Свойства ядра 1 H позволяют широко использовать ЯМР - спектроскопию в анализе органических веществ.
Молекулы водорода достаточно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:
Поэтому окислительная способность водорода проявляется в реакциях с активными металлами, как правило, при повышенных температуре и давлении. При обычных температурах водород реагирует только с очень активными металлами, например, с кальцием , образуя гидрид кальция :
и с единственным неметаллом — фтором , образуя фтороводород :
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например, при освещении:
Записанное уравнение отражает восстановительные свойства водорода.
С галогенами образует галогеноводороды :
С сажей взаимодействует при сильном нагревании:
При взаимодействии с активными металлами водород образует гидриды:
Гидриды — солеобразные, твёрдые вещества, легко гидролизуются
Оксиды металлов (как правило, d-элементов ) восстанавливаются до металлов:
Молекулярный водород широко применяется в органическом синтезе для восстановления органических соединений. Эти процессы называют реакциями гидрирования . Эти реакции проводят в присутствии катализатора при повышенных давлении и температуре. Катализатор может быть как гомогенным (напр., Катализатор Уилкинсона ), так и гетерогенным (напр., никель Ренея , палладий на угле).
Так, в частности, при каталитическом гидрировании ненасыщенных соединений, таких как алкены и алкины , образуются насыщенные соединения — алканы .
На Земле содержание водорода понижено по сравнению с Солнцем, планетами-гигантами и первичными метеоритами, из чего следует, что во время образования Земля была значительно дегазирована: основная масса водорода, как и других летучих элементов, покинула планету во время аккреции или вскоре после неё. [ источник не указан 3866 дней ] Однако точное содержание данного газа в составе геосфер нашей планеты (исключая земную кору ) — астеносферы , мантии , ядра Земли — неизвестно. [ источник не указан 3866 дней ]
Свободный водород H 2 относительно редко встречается в земных газах, но в виде воды он принимает исключительно важное участие в геохимических процессах. Известно содержание водорода в составе вулканических газов, истечение некоторых количеств водорода вдоль разломов в зонах рифтогенеза, выделение этого газа в некоторых угольных месторождениях .
В состав минералов водород может входить в виде иона аммония , гидроксил -иона и воды .
В атмосфере молекулярный водород непрерывно образуется в результате разложения формальдегида, образующегося в цепочке окисления метана или другой органики, солнечным излучением (31—67 гигатонн /год), неполного сгорания различных топлив и биомасс (по 5—25 гигатонн/год), в процессе фиксации азота микроорганизмами из воздуха (3—22 гигатонн/год) .
Имея малую массу, молекулы водорода в составе воздуха обладают высокой тепловой скоростью (она близка ко второй космической скорости) и, попадая в верхние слои атмосферы, могут навсегда улететь в космическое пространство (см. Диссипация атмосфер планет ). Объёмы потерь оцениваются в 3 кг в секунду .

Водород при смеси с воздухом образует взрывоопасную смесь — так называемый гремучий газ . Наибольшую взрывоопасность этот газ имеет при объёмном отношении водорода и кислорода 2:1, или водорода и воздуха приближённо 2:5, так как в воздухе кислорода содержится примерно 21 %. Также водород пожароопасен . Жидкий водород при попадании на кожу может вызвать сильное обморожение .
Считается, что взрывоопасные концентрации водорода с кислородом возникают от 4 % до 96 % объёмных. При смеси с воздухом от 4 % до 75 (74) % по объёму. Такие цифры фигурируют сейчас в большинстве справочников, и ими вполне можно пользоваться для ориентировочных оценок. Однако следует иметь в виду, что более поздние исследования (примерно конец 80-х) выявили, что водород в больших объёмах может быть взрывоопасен и при меньшей концентрации. [ источник не указан 1361 день ] Чем больше объём, тем меньшая концентрация водорода опасна.
Источник этой широко растиражированной ошибки в том, что взрывоопасность исследовалась в лабораториях на малых объёмах. Поскольку реакция водорода с кислородом — это цепная химическая реакция, которая проходит по свободнорадикальному механизму, «гибель» свободных радикалов на стенках (или, скажем, поверхности пылинок) критична для продолжения цепочки. В случаях, когда возможно создание «пограничных» концентраций в больших объёмах (помещения, ангары, цеха), следует иметь в виду, что реально взрывоопасная концентрация может отличаться от 4 % как в большую, так и в меньшую стороны.
Водород сегодня применяется во многих областях. Структура мирового потребления водорода представлена в следующей таблице
| Применение | Доля |
|---|---|
| Производство аммиака | 54 % |
| Нефтепереработка (гидрогенизация ненасыщенных углеводородов и гидросульфирование) и синтез метанола | 35 % |
| Производство полупроводников | 6 % |
| Металлургия и стекольная промышленность | 3 % |
| Пищевая промышленность | 2 % |
Химическая промышленность — это крупнейший потребитель водорода. Более 50 % мирового выпуска водорода идёт на производство аммиака . Ещё около 8 % используется для производства метанола . Из аммиака производят пластмассы, удобрения, взрывчатые вещества и прочее. Метанол является основой для производства некоторых пластмасс.
В нефтепереработке около 37 % мирового выпуска водорода используется в процессах гидрокрекинга и гидроочистки , способствуя увеличению глубины переработки сырой нефти и повышению качества конечных продуктов .
Водород используют и в качестве ракетного топлива . Ввиду крайне узкого диапазона температур (менее 7 кельвинов), при котором водород остаётся жидкостью, на практике чаще используется смесь жидкой и твёрдой фаз.
В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую.
Водород используется в качестве топлива для серийно выпускаемых автомобилей на Водородных топливных элементах : Toyota Mirai , Hyundai Nexo . Американская компания представила линейку коммерческих автомобилей на водороде, а также пикап Nikola Badger с запасом хода 960 км
Компания Alstom в 2018 году запустила в Германии первый коммерческий поезд на топливных элементах Coradia iLint, способный проходить 1000 км на одном резервуаре с водородом. Поезда совершают 100-километровые рейсы со скоростью до 140 километров в час .
В электроэнергетике водород применяется для охлаждения мощных электрических генераторов .
При производстве саломаса (твёрдый жир, производимый из растительных масел ) используется около 2 % мирового выпуска водорода. Саломас является основой для производства маргарина , косметических средств, мыла. Водород зарегистрирован в качестве пищевой добавки под номером E949 .
Водород используется в химических лабораториях в качестве газа-носителя в газовой хроматографии . Такие лаборатории есть на многих предприятиях в пищевой, парфюмерной, металлургической и химической промышленности. Несмотря на горючесть водорода, его использование в такой роли считается достаточно безопасным, поскольку водород используется в незначительных количествах. Эффективность водорода как газа-носителя при этом лучше, чем у гелия, при существенно более низкой стоимости .
Водород используется в метеорологии для заполнения оболочек метеозондов . Водород в этом качестве имеет преимущество перед гелием, так как он дешевле. Ещё более существенно, что водород вырабатывается прямо на метеостанции с помощью простого химического генератора или с помощью электролиза воды. Гелий же должен доставляться на метеостанцию в баллонах, что может быть затруднительно для удалённых мест .
В настоящее время водород в авиации не используется. Когда-то дирижабли и воздушные шары наполняли водородом. Но в 30-х гг. XX в. произошло несколько катастроф , в ходе которых дирижабли взрывались и сгорали. В наше время дирижабли наполняют гелием, несмотря на его существенно более высокую стоимость.
Атомарный водород используется для атомно-водородной сварки . Высокая теплопроводность водорода используется для заполнения сфер гирокомпасов и стеклянных колб филаментных LED-лампочек .