2067: Петля времени
- 1 year ago
- 0
- 0
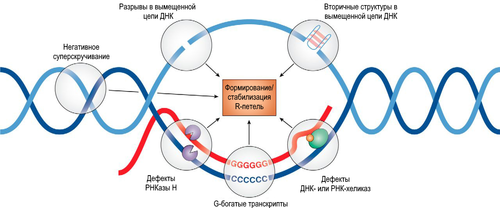

R-петля — особая структурная конформация нуклеиновых кислот , образующаяся при гибридизации РНК с комплементарной нитью двунитевой ДНК , образование дуплекса РНК:ДНК при этом приводит к вытеснению некомплементарной нити ДНК с образованием петли . R-петли часто формируются во время транскрипции , особенно в промоторных областях, когда только что синтезированный транскрипт гибридизуется с матричной цепью ДНК . По некоторым оценкам R-петли могут занимать до 5 % генома у млекопитающих . R-петли играют роль в стабильности генома и хорошо известных функциях, связанных с регуляцией генов , репликацией ДНК, формированием паттерна хроматина , рекомбинацией генов иммуноглобулинов и репарацией двухцепочечных разрывов ДНК .
R-петли были впервые идентифицированы in vitro при помощи электронной микроскопии в 1976 году . В эксперименте in vitro было продемонстрировало образование стабильной гибридных структур РНК с двунитевой ДНК, для разрушения этих структур требовалась деградация РНК при помощи РНКаз. Однако эксперименты по гибридизации in vitro требовали использования 70 % формамида, и поэтому не было доказано, что наблюдаемые структуры встречаются в природе. Тогда было высказано предположение, что при помощи R-петель можно картировать и выявлять последовательности ДНК. Два десятилетия спустя аналогичные гибридные структуры РНК:ДНК были идентифицированы in vivo. В этом исследовании мутантный анализ в Escherichia coli идентифицировал субъединицу ДНК-гиразы В и показал, что сверхэкспрессия эндорибонуклеазы Н ( РНКазы Н ) и топоизомеразы I в качестве ключевых ферментов сбалансированного образования R-петель уменьшает дефекты роста, вызванные накоплением R-петель. С момента этого открытия биологическая роль R-петель в отношении транскрипции / регуляции генов, рекомбинации с переключением классов (CSR)/диверсификации классов антител и стабильности репарации ДНК/генома рассматривалась в большом количестве комплексных исследований .
В ходе исследований были проанализированы крупномасштабные наборы данных о белках, ассоциированных с гибридной петлей, и данные об экспрессии генов из базы данных генома рака. Исследователи предполагают, что РНК:гибридные белки ДНК являются релевантными маркерами и мишенями для терапии рака. Аналогичным образом, различные белки, связанные с регуляцией эпитранскриптома, также способствуют развитию раковых явлений, а METTL3 (m6 A writer) и YTHDF2 (m6 A reader), которые, как было показано, играют роль в биологии R — петли, были связаны с развитием рака в нескольких исследованиях. Роль m6A в биологии R-петли и возможной стабильности генома является очень недавним открытием, и модификации M6a на мРНК имеют несколько функций, включая стабильность мРНК, транспорт и сплайсинг . Таким образом, неизвестно, относится ли биологическая роль модифицированных мРНК M6a к отдельным мРНК или к их гибридизации с ДНК в структурах R-петли. В дополнение к раку, структуры R-петли также были вовлечены в нарушения повторного расширения и многочисленные неврологические заболевания. В мозге происходит динамическое метилирование м6А в мРНК, и механизм, контролирующий это, необходим для точной нейрорегуляции. Опять же, эпитранскриптомика показала, что белки, влияющие на формирование и накопление R-петель, коррелируют с дефектом развития мозга, самообновлением нейрональных стволовых клеток-предшественников и развитием нейронов у мышей. Интересно, что истощение YTHDF2 у мышей приводит к накоплению структур R-петли и очагов yH2AX в коре плода. Формирование, функция и разрешение R-петель в геноме млекопитающих широко изучались в течение последних десятилетий, но некоторые интересные свойства, связанные со стабильностью генома и болезнями, ещё предстоит понять .