Эпигеномика
- 1 year ago
- 0
- 0
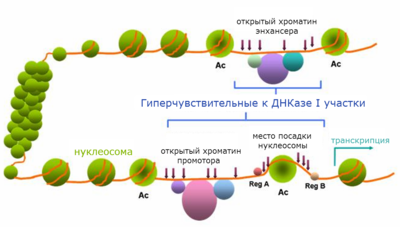
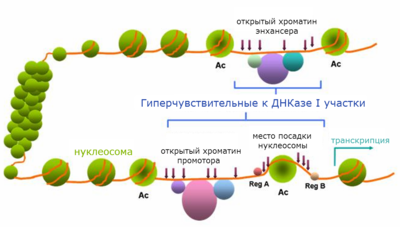
Откры́тый хромати́н ( англ. open chromatin ) — небольшие участки хроматина , свободные от нуклеосом . Посадке нуклеосом, как правило, препятствуют связанные с хроматином белковые факторы, узнающие определённые последовательности ДНК . К числу таких белков относятся транскрипционные факторы , ДНК- или РНК- полимеразы . Открытый хроматин часто совпадает с цис-регуляторными последовательностями , а именно: промоторами , энхансерами , инсуляторами , сайленсерами , участками начала репликации ДНК . Размер открытых участков хроматина обычно составляет несколько сотен пар нуклеотидов , в среднем около 300 п.н .
Открытый хроматин наиболее часто определяют с помощью метода ДНКазной чувствительности. Свободные от нуклеосом участки хроматина предпочтительно атакуются ДНКазой I при обработке ей пермеабилизованных клеток или изолированных ядер . В связи с этим открытый хроматин часто называют гиперчувствительными к ДНКазе I участками , или гиперчувствительными сайтами ( англ. hypersensitive sites ). Вероятность расщепления ДНК нуклеазой в гиперчувствительных сайтах может превосходить среднестатистическую в сотни и даже тысячи раз. Гиперчувствительность к ДНКазе I открытого хроматина следует отличать от повышенной общей ДНКазной чувствительности активно транскрибирующихся генов .
В зависимости от типа белковых факторов, связывание которых с ДНК препятствует посадке нуклеосом, участки хроматина могут быть тканеспецифичными или конститутивными, то есть присутствующими в клетках, дифференцированных по разным путям.
Для картирования областей открытого хроматина используют методы ДНКазной чувствительности ( англ. DNase I hypersensitive ) и изоляции регуляторных элементов с помощью формальдегида англ. formaldehyde-assisted isolation of regulatory elements (FAIRE) . Метод ДНКазной чувствительности не позволяет определить, каким именно регуляторным участком является данная область открытого хроматина .
Ранее анализ результатов метода ДНКазной чувствительности проводился с помощью саузерн-блот гибридизации ( англ. Southern blot ). Это не позволяло проводить анализ большого количества сайтов, а также находить новые сайты гиперчувствительности. Анализ ДНКазной чувствительности можно проводить также с помощью ПЦР в реальном времени (количественной ПЦР). Это значительно проще, чем саузерн-блот гибридизация, но этот метод также имеет ограничение по количеству сайтов для анализа и не может быть использован для полногеномного исследования распределения сайтов чувствительности к ДНКазе I .
Развитие методов высокоэффективного секвенирования ( англ. High-throughput sequencing ) и ДНК-микрочипов ( англ. DNA-microarray ) позволяет картировать области открытого хроматина на всем протяжении генома . Кроме того, сочетание метода ДНКазной чувствительности с методом иммунопреципитации ( англ. Chromatin immunoprecipitation (ChIP) ) с последующим высокоэффективным секвенированием позволяет получать больше информации о связывании конкретных транскрипционных факторов с активными участками хроматина .
Другой способ картирования областей открытого хроматина — проведение иммунопреципитации хроматина ( англ. ChIP ) на антитела к гистонам . При этом области открытого хроматина должны быть мало представлены, так как с ними не связаны нуклеосомы. Метод ДНКазной чувствительности и иммунопреципитация гистонов дают сходные результаты .
В геномах эукариот некодирующие последовательности, участвующие в регуляции экспрессии генов на разных стадиях развития организма или в разных тканях, приобретают особое значение. Открытие и характеристика регуляторных участков становится необходимой для понимания закономерностей в экспрессии генов . Так в геноме человека более 95 % ДНК является некодирующей . В этот класс последовательностей, кроме мусорной ДНК , входят важные регуляторные последовательности: промоторы, энхансеры, сайленсеры, инсуляторы или ( англ. locus control regions (LCR) ). ENCODE консорциум показал, что сайты гиперчувствительности к ДНКазе I, идентифицированные в 1 % генома человека , являются маркерами модификаций гистонов, участков ранней репликации , сайтов начала транскрипции и сайтами связывания транскрипционных факторов . Также открытый хроматин часто связан с активно транскрибируемыми некодирующими РНК .
Кроме некодирующих регуляторных последовательностей, открытый хроматин также ассоциирован с экзонами и интронами активно транскрибируемых генов. Особенно часто такие участки открытого хроматина совпадают первым экзоном и интроном гена . Однако наличие открытого хроматина не является достаточным условием активности гена. Нетранскрибируемые гены, связанные с открытым хроматином, находятся в состоянии «готовности» к транскрипции ( англ. poised state ) . Таким образом, формирование открытого хроматина или перевод в неактивное состояние является важным для регуляции экспрессии генов.
Свободными от нуклеосом могут быть не только участки связывания транскрипционных факторов и других регуляторных белков. Некоторые последовательности ДНК не способны наматываться на нуклеосомные глобулы. Это последовательности, обладающие пониженной гибкостью, и последовательности, склонные с созданию неканонических структур, например, шпилек .
Из рисунка [ прояснить ] , представляющего скриншот UCSC, видна колокализация сайта ДНКазной гиперчувствительности ( англ. DNaseI Hypersensitivity Clusters ) с промоторами двух генов. Области открытого хроматина окружены , по 27-му остатку лизина (H3K27Ac), что является меткой активных регуляторных областей хроматина, таких как промоторы и энхансеры. Кроме того, в районе сайта ДНКазной гиперчувствительности находится сайт связывания многих транскрипционных факторов, среди которых можно обнаружить консервативный фактор инициации транскрипции (является основной частью ). Также можно заметить частое связывание в этом районе РНК-полимеразы II , осуществляющей транскрипцию белок-кодирующих генов у человека . Для данного сайта ДНКазной гиперчувствительности характерна повышенная консервативность среди млекопитающих ( англ. Mammal Cons ), что означает сохранение этой последовательности в ходе эволюции , и, как следствие, её функциональное значение .
Образование областей, свободных от нуклеосом, происходит под действием специальных факторов, осуществляющих сборку, разборку и перемещение нуклеосом. Процесс изменения положения нуклеосом называется ремоделированием хроматина . В нём участвуют комплексы ремоделирования хроматина — консервативные белковые комплексы, работающие с затратой энергии АТФ . Ремоделирование хроматина осуществляется после внесения определенных эпигенетических меток — модификации гистонов или метилирования ДНК . Если метки соответствуют активному хроматину (например, ацетилированый 9-й лизин гистона H3, ди- и триметилированный 4-й лизин гистона H3 и многие другие), то образуются участки открытого хроматина. Часто профиль модификаций гистонов имеет определенное распределение вокруг сайта гиперчувствительности к ДНКазе I .
Высокоэффективные методы позволяют сравнивать распределение областей открытого хроматина в различных тканях или культурах клеток из одного организма. Подобное сравнение выявляет существенное различие в распределении таких участков в геноме . Это говорит о различной активности таких участков в разных тканях. Так промотор и энхансер гена могут находиться в области открытого хроматина в одной ткани и быть закрыты нуклеосомами в другой. Это говорит о различной экспрессии генов в разных тканях и наиболее характерно для тканеспецифичных ( англ. tissue-specific ) генов. Наоборот, гены, находящиеся в области открытого хроматина во всех тканях и клеточных линиях, обычно, относятся к генам домашнего хозяйства ( англ. housekeeping genes ). Также может происходить изменение профиля ДНКазной чувствительности в процессе развития и дифференцировки клеток. Для выявления активности тканеспецифичных генов используют определение генной онтологии ( англ. Gene Ontology (GO) ) после проведения DNase-seq .