Interested Article - Глюкозинолаты
- 2020-10-05
- 2
Глюкозинолаты — это органические соединения, встречающиеся в овощах с резким и терпким вкусом, таких как горчица , капуста и хрен . Им придают остроту горчичные масла, которые образуются из глюкозинолатов при пережевывании, нарезании или любом другом повреждении целостности съедобного растения. Эти натуральные химические соединения помогают растениям защищаться от вредителей и болезней и придают характерную терпкость вкусу всех крестоцветных овощей . Между видами варьируются по химической структуре и по содержанию .
Глюкозинаты могут быть разделены на 3 класса: алифатические глюкозинолаты, индольные глюкозинолаты и ароматические глюкозинолаты .
Химия
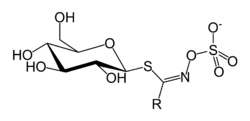
Глюкозинолаты представляют собой природный класс органических соединений, которые содержат серу и азот и являются производными глюкозы и аминокислоты. Они являются водорастворимыми анионами и относятся к глюкозидам. Каждый глюкозинолат содержит центральный атом углерода, который связан с атомом серы тиоглюкозной группы и через атом азота с сульфатной группой (образуя сульфатированный альдоксим). Кроме того, центральный углерод связан с боковой группой; разные глюкозинолаты имеют разные боковые группы, и именно вариации в боковой группе ответственны за изменение биологической активности этих растительных соединений. Суть химии глюкозинолатов заключается в их способности превращаться в изотиоцианат («горчичное масло») при гидролизе тиоглюкозидной связи ферментом мирозиназой .
Биохимия
Природное разнообразие из нескольких аминокислот
Известно, что около 132 различных глюкозинолатов встречаются в растениях в природе. Они синтезируются из определённых аминокислот: так называемых алифатических глюкозинолатов, полученных в основном из метионина, но также аланина, лейцина, изолейцина или валина. (Большинство глюкозинолатов на самом деле получают из гомологов этих аминокислот с удлиненной цепью, например, глюкорафанин получают из дигомометионина, цепь которого удлинена в два раза). Ароматические глюкозинолаты включают индольные глюкозинолаты, такие как глюкобрассицин, полученный из триптофана, и другие изфенилаланин, его гомолог с удлиненной цепью гомофенилаланин и синальбин, полученные из тирозина .
Ферментативная активация
Растения содержат фермент мирозиназу, который в присутствии воды отщепляет глюкозную группу от глюкозинолата . Оставшаяся молекула затем быстро превращается в изотиоцианат, нитрил или тиоцианат; это активные вещества, которые служат защитой для растения. Глюкозинолаты также называют гликозидами горчичного масла. Стандартным продуктом реакции является изотиоцианат (горчичное масло); два других продукта в основном образуются в присутствии специализированных растительных белков, которые изменяют результат реакции .
В химической реакции, проиллюстрированной выше, красные изогнутые стрелки в левой части рисунка упрощены по сравнению с реальностью, поскольку роль фермента мирозиназы не показана. Однако показанный механизм в основном соответствует реакции, катализируемой ферментом.
Напротив, реакция, проиллюстрированная красными изогнутыми стрелками в правой части рисунка, изображающая перегруппировку атомов, приводящую к образованию изотиоцианата, как ожидается, будет неферментативной. Этот тип перегруппировки можно назвать перегруппировкой Лоссена или перегруппировкой, подобной Лоссену, поскольку это название впервые было использовано для аналогичной реакции, приводящей к органическому изоцианату (R-N = C = O).
Чтобы предотвратить повреждение самого растения, мирозиназа и глюкозинолаты хранятся в отдельных ячейках клетки или в разных клетках ткани и собираются вместе только или главным образом в условиях физического повреждения (см. Мирозиназа ).
Растения с глюкозинолатами
Глюкозинолаты образуются как вторичные метаболиты практически во всех растениях порядка Капустоцветные . К порядку Капустоцветные относится, например, экономически важное семейство Капустные, а также Каперсовые и Кариковые . Растения рода Дрипетес и Путранджива , которые не относятся к порядку Капустоцветные, это единственные представители других видов, содержащие глюкозинолаты. Глюкозинолаты встречаются в различных съедобных растениях, например в капусте (белокочанная, пекинская, брокколи), брюссельской капусте, водяном крессе, хрене, каперсах и редисе, отличительный вкус которым придают продукты деструкции этих соединений. Кроме того, глюкозинолаты содержатся в семенах этих растений.
Биологическое воздействие
Люди и животные
Токсичность
Использование глюкозинолат-содержащих культур в качестве основного источника пищи для животных может иметь негативные последствия, если концентрация глюкозинолатов превышает допустимую для данного животного. Было доказано, что высокие дозы некоторых глюкозинолатов оказывают токсическое действие (в основном в качестве зобных и антитиреоидных агентов) как на людей [ нет в источнике ] , так и на животных . Содержание же глюкозинатов в продуктах животного происхождения намного ниже, чем в овощах, поэтому у людей такие продукты не должны вызывать каких-либо негативных эффектов для здоровья . Однако уровень толерантности к глюкозинолатам варьируется даже в пределах одного и того же рода (например, у каирской иглистой мыши (Acomys cahirinus) и золотистой иглистой мыши (Acomys russatus) .
Вкус и пищевое поведение
Наряду с другими глюкозинолатами синигрин сообщает горьковатый привкус приготовленной цветной и брюссельской капусте . Глюкозинолаты могут изменять пищевое поведение животных .
Исследования
Образующиеся из глюкозинолатов изотиоцианаты изучают в лабораторных условиях для оценки экспрессии и активации ферментов, которые подвергают химическим изменениям ксенобиотики , например канцерогены . Были проведены обзорные исследования с целью определить, влияет ли потребление крестоцветных овощей на риск развития рака у людей. Согласно анализу 2017 года, нет достаточных клинических доказательств того, что потребление изотиоцианатов, содержащихся в крестоцветных овощах, полезно для здоровья .
Насекомые
Глюкозинолаты и их производные обладают одновременно отпугивающим и токсичным действием на различных насекомых. В попытке применить этот принцип в полеводческом контексте были разработаны продукты на основе глюкозинолатов, которые можно использовать в качестве , то есть натуральных пестицидов .
В отличие от них такой вредитель крестоцветных, как капустная моль, может распознавать наличие глюкозинолатов и по ним отыскивать нужное для себя растение . Существуют определённые виды насекомых, которые специализируются только на глюкозинолат-содержащих растениях, к ним относятся бабочки-белянки капустница, репница и зорька, некоторые виды тли , мотыльки южная совка, настоящие пилильщики и земляные блошки . Например, бабочка капустница откладывает яйца на растениях, содержащих глюкозинолаты, и личинки способны выживать даже в условиях высокой концентрации этих соединений, питаясь растительной массой. Белянки и зорьки обладают так называемым нитрильным спецификатором, который сводит гидролиз глюкозинолатов к нитрилу, а не реакционноспособным изотиоцианатам . При этом у капустной моли в арсенале совершенно другой белок — глюкозинолат сульфатаза, который десульфатирует глюкозинолаты и не дает им распадаться до токсичных продуктов под действием мирозиназы .
Другие виды насекомых (специализированные пилильщики и тля) изолируют глюкозинолаты . У специализированных тлей, но не у пилильщиков, в мышечной ткани обнаружен особый животный фермент мирозиназа , приводящий к деградации изолированных глюкозинолатов при разрушении тканей тлей . Этот разнообразный ассортимент биохимических решений для одного и того же растительного соединения играет ключевую роль в эволюции отношений между растениями и насекомыми .
См. также
Примечания
- ↑ Masahiko Ishida, Masakazu Hara, Nobuko Fukino, Tomohiro Kakizaki, Yasujiro Morimitsu. // Breeding Science. — 2014-05. — Т. 64 , вып. 1 . — С. 48–59 . — ISSN . — doi : . 25 августа 2022 года.
- Spyridon A. Petropoulos, Isabel C. F. R. Ferreira, Lilian Barros. . — Bentham Science Publishers, 2018. — С. 265. — 492 с. — ISBN 978-1-68108-739-9 . 26 августа 2022 года.
- Masahiko Ishida, Masakazu Hara, Nobuko Fukino, Tomohiro Kakizaki, Yasujiro Morimitsu. (англ.) // Breeding Science. — 2014. — May ( vol. 64 , iss. 1 ). — P. 48–59 . — ISSN . — doi : . — . 25 августа 2022 года.
- ↑ Agerbirk N, Olsen CE (May 2012). "Glucosinolate structures in evolution". Phytochemistry . 77 : 16—45. doi : . PMID .
- Bongoni R, Verkerk R, Steenbekkers B, Dekker M, Stieger M (September 2014). "Evaluation of different cooking conditions on broccoli (Brassica oleracea var. italica) to improve the nutritional value and consumer acceptance". Plant Foods for Human Nutrition . 69 (3): 228—234. doi : . PMID . S2CID .
- Burow M, Bergner A, Gershenzon J, Wittstock U (January 2007). . Plant Molecular Biology . 63 (1): 49—61. doi : . PMID . S2CID .
- James E. Rodman, Kenneth G. Karol, Robert A. Price, Kenneth J. Sytsma. // Systematic Botany. — 1996. — Т. 21 , вып. 3 . — С. 289–307 . — ISSN . — doi : . 25 августа 2022 года.
- . poisonousplants.ansci.cornell.edu . Дата обращения: 25 августа 2022. 12 июня 2022 года.
- Auðunsson, Guðjón Atli et al. (англ.) // EFSA Journal. — 2008. — 15 January ( no. EFSA-Q-2003-061 ). — P. 1—76 . — ISSN . — doi : .
- Michal Samuni-Blank, Zeev Arad, M. Denise Dearing, Yoram Gerchman, William H. Karasov. (англ.) // Evolutionary Ecology. — 2013-11-01. — Vol. 27 , iss. 6 . — P. 1069–1080 . — ISSN . — doi : .
- . Дата обращения: 25 августа 2022. 25 августа 2022 года.
- Michal Samuni-Blank, Ido Izhaki, M. Denise Dearing, Yoram Gerchman, Beny Trabelcy. (англ.) // Current Biology. — 2012-07-10. — Т. 22 , вып. 13 . — С. 1218–1220 . — ISSN . — doi : . 8 мая 2013 года.
- ↑ (англ.) . Linus Pauling Institute (29 апреля 2014). Дата обращения: 25 августа 2022. 5 июля 2019 года.
- Lorenzo Furlan, Christian Bonetto, Andrea Finotto, Luca Lazzeri, Lorena Malaguti. (англ.) // Industrial Crops and Products. — 2010-03-01. — Vol. 31 , iss. 2 . — P. 245–254 . — ISSN . — doi : . 11 марта 2017 года.
- Francisco Rubén Badenes-Pérez, Michael Reichelt, Jonathan Gershenzon, David G. Heckel. // The New Phytologist. — 2011-01. — Т. 189 , вып. 2 . — С. 549–556 . — ISSN . — doi : . 25 августа 2022 года.
- Ute Wittstock, Niels Agerbirk, Einar J. Stauber, Carl Erik Olsen, Michael Hippler. // Proceedings of the National Academy of Sciences of the United States of America. — 2004-04-06. — Т. 101 , вып. 14 . — С. 4859–4864 . — ISSN . — doi : . 25 августа 2022 года.
- Andreas Ratzka, Heiko Vogel, Daniel J. Kliebenstein, Thomas Mitchell-Olds, Juergen Kroymann. // Proceedings of the National Academy of Sciences of the United States of America. — 2002-08-20. — Т. 99 , вып. 17 . — С. 11223–11228 . — ISSN . — doi : . 25 августа 2022 года.
- C. Müller, N. Agerbirk, C. E. Olsen, J. L. Boevé, U. Schaffner. // Journal of Chemical Ecology. — 2001-12. — Т. 27 , вып. 12 . — С. 2505–2516 . — ISSN . — doi : . 25 августа 2022 года.
- Matthew Bridges, Alexandra M. E. Jones, Atle M. Bones, Chris Hodgson, Rosemary Cole. // Proceedings. Biological Sciences. — 2002-01-22. — Т. 269 , вып. 1487 . — С. 187–191 . — ISSN . — doi : . 25 августа 2022 года.
- Christopher W. Wheat, Heiko Vogel, Ute Wittstock, Michael F. Braby, Dessie Underwood. // Proceedings of the National Academy of Sciences of the United States of America. — 2007-12-18. — Т. 104 , вып. 51 . — С. 20427–20431 . — ISSN . — doi : . 25 августа 2022 года.
- 2020-10-05
- 2

