Дифференцировка клеток
- 1 year ago
- 0
- 0
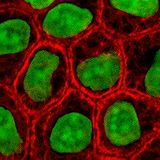
Культивирование клеток представляет собой процесс, посредством которого in vitro отдельные клетки (или единственная клетка) прокариот и эукариот выращиваются в контролируемых условиях. На практике термин « культура клеток » относится в основном к выращиванию клеток, относящихся к одной ткани, полученных от многоклеточных эукариот, чаще всего животных. Историческое развитие технологии и методик выращивания культур клеток неразрывно связаны с выращиванием тканевых культур и целых органов.
В XIX веке английский физиолог С. Рингер разработал солевой раствор , содержащий хлориды натрия, калия, кальция и магния для поддержания биения сердца животных вне организма. В 1885 году Вильгельм Ру установил принцип культивирования тканей, извлек часть костного мозга из куриного эмбриона и держал его в теплом физрастворе в течение нескольких дней . Росс Гранвилл Харрисон , работавший в Медицинской школе Дж. Хопкинса, а затем в Йельском университете , опубликовал результаты своих экспериментов в 1907 −1910 годах, создав методологию культивирования тканей. В 1910 г. Пейтон Раус , работая с культурой клеток саркомы цыплёнка, индуцировал образование опухолей у здоровых животных. Позже это привело к открытию онкогенных вирусов ( Нобелевская премия по физиологии или медицине 1966 г.).
Методы культивирования клеток получили значительное развитие в 1940-х 1950-х годах в связи с исследованиями в области вирусологии. Выращивание вирусов в культурах клеток дало возможность получения чистого вирусного материала для производства вакцин. Вакцина против полиомиелита стала одним из первых препаратов, массово произведённых с использованием технологии культивирования клеток. В 1954 г. Эндерс , Уэллер и Роббинс получили Нобелевскую премию «За открытие способности вируса полиомиелита расти в культурах различных тканей». В 1952 г. была получена широко известная линия раковых клеток человека HeLa .
1885 — Ру (Roux) продемонстрировал возможность поддержания клетками куриного эмбриона жизнеспособности вне тела животного в солевом растворе .
1907 — Гаррисон (Harrison) культивировал спинной мозг амфибий в сгустке плазмы. Он пытался показать, что аксоны образуются в виде выростов отдельных нервных клеток .
1910 — Раус (Raus) с применением фильтрованного экстракта куриной опухоли индуцировал опухоль. Позднее было показано, что в основе такого эффекта лежал РНКовый вирус саркомы Рауса .
1913 — Каррель (Carrel) доказал, что в асептических условиях клетки могут расти в культуре в течение длительного времени, если их обеспечить необходимыми питательными веществами .
1948 — Эрл (Earle) и сотрудники установили, что одиночные клетки линии L в культуре формируют клоны клеток .
1952 — Джей (Gey) и сотрудники получили перевиваемую клеточную линию из карциномы шейки матки; эта клеточная линия широко известна как HeLa .
1954 — Леви-Монтальчини (Levy-Montalchini) и сотрудники показали, что в культуре ткани фактор, стимулирующий рост нервов, вызывает рост аксонов .
1955 — Игл (Eagle) - впервые систематически исследовал пищевые потребности клеток в условиях культуры ткани и обнаружил, что клетки животных способны существовать в определенной смеси низкомолекулярных веществ, дополненной некоторым количеством белков сыворотки .
1956 — Пак (Puck) и сотрудники отобрали мутантные клетки HeLa, потребности которых для роста в культуре существенно отличались от потребностей других клеток .
1958 — Темин и Рубин (Temin, Roubin) количественно описали инфицирование клеток цыпленка в культуре очищенным вирусом саркомы Рауса. В течение следующего десятилетия Стокер, Дульбекко, Грин (Stocker, Dulbecco, Green) и другие вирусологи установили основные характеристики вирусной трансформации различных типов .
1961 — Хайфлик и Мурхед (Hayflick, Moorhend) показали, что в культуре фибробласты человека погибают после определенного числа делений .
1964 — Литлфилд (Littlefield) впервые использовал для выращивания гибридов соматических клеток селективную среду HAT. Это нововведение в сочетании с методом гибридизации клеток позволило приступить к изучению генетики соматических клеток .
1964 — Като и Такеуши (Kato, Takeuchi) получили целое растение моркови из растущей в культуре тканей клетки корня .
1965 — Хэм (Ham) предложил бессывороточную среду определенного химического состава, которая способна поддерживать рост клонов некоторых клеток животных .
1965 — Харрис и Уоткинс (Harris, Watkins) индуцировали вирусом слияние клеток мыши и человека и получили первые гетерокарионы клеток млекопитающих .
1968 — Августи-Точчо и Сато (Augusti-Tocco, Sato) адаптировали к условиям культуры клеток опухолевые клетки мыши (нейробластомы) и выделили клоны, которые реагировали на раздражение электрическим током и разрастались в нервные волокна. Одновременно получено большое количество других дифференцированных клеточных линий, включая линии скелетных мышц и печени .
1975 — Келер и Мильштейн (Kehler, Milstein) получили первые клеточные линии гибридом, секретирующих моноклональные антитела .
1976 — Сато (Sato) и сотрудники опубликовали первую серию статей, в которых было показано, что для роста в бессывороточной среде разным клеточным линиям необходимы различные смеси гормонов и факторов роста .
Для культивирования вне организма живые клетки могут быть получены несколькими способами. Клетки могут быть выделены из крови, но к росту в культуре способны только лейкоциты. Моноядерные клетки могут быть выделены из мягких тканей с помощью таких ферментов , как коллагеназа , трипсин , проназа , разрушающих внеклеточный матрикс . Кроме того, в питательную среду можно поместить кусочки тканей и материалов.
Культуры клеток, взятых непосредственно от объекта ( ex vivo ), называются первичными . Большинство первичных клеток, за исключением опухолевых, имеют ограниченный срок использования. После определённого количества делений такие клетки стареют и прекращают делиться, хотя могут при этом сохранить жизнеспособность.
Существуют , способные размножаться бесконечно. У большинства опухолевых клеток эта способность является результатом случайной мутации , но у некоторых лабораторных клеточных линий она приобретена искусственно, путём активации гена теломеразы .
Клетки выращивают в специальных питательных средах , при постоянной температуре. Для культур растительных клеток используется регулируемое освещение, а для клеток млекопитающих обычно необходима также специальная газовая среда, поддерживаемая в инкубаторе клеточных культур . Как правило, регулируется концентрация в воздухе углекислого газа и паров воды, но иногда также и кислорода. Питательные среды для разных культур клеток различаются по составу, pH , концентрации глюкозы , составу факторов роста и др . Факторы роста , используемые в питательных средах для клеток млекопитающих, чаще всего добавляют вместе с сывороткой крови . Одним из факторов риска при этом является возможность заражения культуры клеток прионами или вирусами. При культивировании одной из важных задач является исключение или сведение к минимуму использование заражённых ингредиентов. Однако на практике это бывает достигнуто не всегда. Наилучшим, но и наиболее дорогостоящим способом является добавление вместо сыворотки очищенных факторов роста .
Клетки можно выращивать в суспензии , либо в адгезивном состоянии. Некоторые клетки (такие, как клетки крови ) в естественных условиях существуют во взвешенном состоянии. Существуют также линии клеток, искусственно изменённых таким образом, чтобы они не могли прикрепляться к поверхности; это сделано для того, чтобы увеличить плотность клеток в культуре. Для выращивания адгезивных клеток требуется поверхность, например, культура ткани, или пластик, покрытый элементами внеклеточного матрикса для улучшения адгезивных свойств, а также для стимулирования роста и дифференцировки. Большинство клеток из мягких и твердых тканей адгезивны. Из адгезивного типа культуры выделяются органотипические культуры клеток, которые представляют собой трёхмерную среду, в отличие от обычной лабораторной посуды. Эта система культивирования физически и биохимически наиболее сходна с живыми тканями, но имеет некоторые технические сложности в обслуживании (например, нуждается в диффузии). С целью обеспечения необходимых физических условий для культивирования адгезивных культур и заселения объёма внеклеточного матрикса тканеинженерных конструкций используются системы динамического культивирования на основе роторных и вихревых биореакторов, биореакторов с непосредственным на скаффолд: компрессионных биореакторов, биореакторов с механическим натяжением и гидростатическим давлением, специальных биореакторов для электростимуляции клеток и тканей, а также комбинированных биореакторов .
При работе с клеточными культурами учёные могут столкнуться с проблемой перекрёстного загрязнения.
При выращивании клеток, из-за постоянного деления может возникнуть их переизбыток в культуре, и, как следствие, возникают следующие проблемы:
Для поддержания нормального функционирования культур клеток а также для предотвращения негативных явлений периодически проводят замену питательной среды, пассирование и трансфекция клеток. Во избежание загрязнения культур бактериями, дрожжами , или другими линиями клеток, все манипуляции обычно проводят с соблюдением правил асептики в стерильном боксе. Для подавления микрофлоры в питательную среду могут быть добавлены антибиотики ( пенициллин , стрептомицин ) и противогрибковые препараты ( амфотерицин B ).
Одним из продуктов метаболизма в клетках являются кислоты, вследствие чего pH среды постепенно снижается. Для контроля кислотности питательных сред, в них добавляют индикаторы pH .
Если культура клеток адгезивная, питательную среду можно полностью заменять.
Пассирование (разделение) клеток — это отбор небольшого количества клеток для выращивания в другом лабораторном сосуде. Если культура быстро растет, это необходимо делать регулярно, поскольку в среде истощаются питательные вещества и накапливаются продукты метаболизма . Суспензивные культуры пассировать проще, так как для этого достаточно всего лишь отобрать необходимое количество клеток, поместить их в другие сосуды, и добавить свежей питательной среды. Адгезивные же клетки перед этим следует отделить от субстрата и разделить их скопления. Чаще всего для этой цели используют смесь трипсина и ЭДТА или другие ферментные смеси, иногда достаточно только ЭДТА в физиологическом растворе (раствор Версена). Если культура растет медленно, её обычно подкармливают без переноса в другой сосуд, периодически (обычно раз в 2-3 дня) отбирая часть использованной среды и добавляя свежую.
В клетки при их выращивании можно внедрять чужеродную ДНК путём трансфекции (невирусный метод). Часто данную технологию применяют для управляемой экспрессии генов . Сравнительно недавно для этих целей была успешно реализована трансфекция иРНК .
ДНК также может быть внедрена в геном клетки с помощью вирусов или бактериофагов . Они, являясь внутриклеточными паразитами, как нельзя лучше подходят для этих целей, так как внедрение генетического материала в клетку-хозяина является обычной частью их жизненного цикла . Этот метод называется трансдукция .
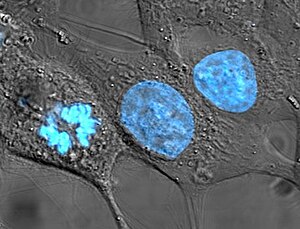
Культивирование человеческих клеток несколько противоречит правилам биоэтики , поскольку изолированно выращиваемые клетки могут пережить родительский организм, а затем использоваться для проведения экспериментов или для разработки новых методов лечения и извлечения из этого прибыли. Первое судебное решение в данной области было вынесено в Верховном суде штата Калифорния по делу «Джон Мур против представителей Калифорнийского университета », согласно которому пациенты не имеют никаких прав собственности на линии клеток, полученных из органов, удалённых с их согласия .
Гибридома — это линия клеток, полученная в результате слияния нормальных лимфоцитов с «бессмертными» раковыми клетками. Используется для получения моноклональных антител . Лейкоциты, выделенные из селезёнки или крови иммунизированных животных, производят антитела с необходимой специфичностью, но как у любой первичной культуры, их способность к пролиферации ограничена пределом Хейфлика . Для иммортализации их искусственно сливают с «бессмертной» линией клеток миеломы , в результате чего происходит рекомбинация признаков. После этого линию клонируют и отбирают клоны, способные одновременно к неограниченной пролиферации и производящие антитела против избранного антигена .
Массовое культивирование клеток является основой для промышленного производства вирусных вакцин и разнообразных продуктов биотехнологии .
Промышленным методом из культур клеток получают такие продукты, как ферменты , синтетические гормоны , моноклональные антитела , интерлейкины , лимфокины , противоопухолевые препараты . Хотя многие простые белки относительно просто могут быть получены с использованием в бактериальных культурах, более сложные белки, такие как гликопротеины, в настоящее время могут быть получены только из животных клеток. Одним из таких важнейших белков является гормон эритропоэтин . Стоимость выращивания культур клеток млекопитающих является довольно высокой, поэтому в настоящее время проводятся исследования по возможности производства сложных белков в культурах клеток насекомых или высших растений .
Культивирование клеток является неотъемлемой частью технологии культивирования тканей и тканевой инженерии, поскольку именно оно определяет основы выращивания клеток и поддержания их в жизнеспособном состоянии ex vivo .
С применением методики культивирования клеток в настоящее время выпускаются вакцины против полиомиелита , кори , эпидемического паротита , краснухи , ветрянки . Вследствие угрозы пандемии гриппа , вызываемого штаммом вируса H5N1 , в настоящий момент правительство Соединённых Штатов финансирует исследования по получению вакцины против птичьего гриппа с использованием клеточных культур.
Культуры клеток растений, как правило, выращиваются либо в виде суспензии в жидкой питательной среде, либо в виде каллусной культуры на твердой питательной основе. Культивирование недифференцированных клеток и каллуса требует соблюдения определённого баланса гормонов роста растений ауксинов и цитокининов .
Для культивирования небольшого количества клеток бактерий и дрожжей клетки высеивают на твердую питательную среду на основе желатина или агар-агара . Для массового производства применяют выращивание в жидких питательных средах (бульонах).
Культуры вирусов выращивают на культурах клеток млекопитающих , растений , грибов или бактерий , в зависимости от природного хозяина конкретного типа вирусов . Но при некоторых условиях могут быть выращены и в клетках другого типа.
В этом случае культура клеток сама служит средой для роста и репликации вируса.
Приведённый здесь список наиболее распространённых клеточных линий не является полным и исчерпывающим.
| Линия клеток | Расшифровка сокращения | Организм | Ткань | Морфология | Примечания и ссылки | |
|---|---|---|---|---|---|---|
| 293-T | человек | почка (эмбриональная) | Производная от HEK-293 | |||
| 3T3 cells | «3-day transfer, inoculum 3 x 105 cells» | мышь | эмбриональные фибробласты | Известна также как NIH 3T3 | ||
| 721 | человек | меланома | ||||
| 9L | крыса | глиобластома | ||||
| A2780 | человек | яичник | рак яичника | |||
| A2780ADR | человек | яичник | производное A2780 с резистентностью к адриамицину | |||
| A2780cis | человек | яичник | производное A2780 с резистентностью к цисплатину | |||
| A172 | человек | глиобластома | злокачественная глиома | |||
| A431 | человек | кожный эпителий | плоскоклеточная карцинома | |||
| A-549 | человек | карцинома лёгких | эпителий | |||
| B35 | крыса | нейробластома | (недоступная ссылка) | |||
| BCP-1 | человек | периферические лейкоциты | HIV+ лимфома | |||
| BEAS-2B | bronchial epithelium + adenovirus 12-SV40 virus hybrid (Ad12SV40) | человек | лёгкие | эпителий | (недоступная ссылка) | |
| bEnd.3 | brain endothelial | мышь | кора головного мозга | эндотелий | ||
| BHK-21 | «Baby Hamster Kidney» | хомяк | почка | фибробласты | от 27 декабря 2009 на Wayback Machine | |
| BR 293 | человек | молочная железа | рак | |||
| BxPC3 | Biopsy xenograph of pancreatic carcinoma line 3 | человек | панкреатическая аденокарцинома | эпителий | (недоступная ссылка) | |
| C3H-10T1/2 | мышь | эмбриональные мезенхимальные клетки | ||||
| C6/36 | Aedes albopictus (комар) | ткани личинки | ||||
| CHO | Chinese hamster ovary | серый хомячок (Cricetulus griseus) | яичник | эпителий | (недоступная ссылка) | |
| COR-L23 | человек | лёгкие | ||||
| COR-L23/CPR | человек | лёгкие | ||||
| COR-L23/5010 | человек | лёгкие | ||||
| COR-L23/R23 | человек | лёгкие | эпителий | |||
| COS-7 | Cercopithecus aethiops, origin-defective SV-40 | обезьяна Cercopithecus aethiops | почка | фибробласты | ||
| CML T1 | Chronic Myelod Leukaemia T-lymphocyte 1 | человек | хроническая миелоидная лейкемия | T-клеточная лейкемия | ||
| CMT | canine mammary tumor | собака | молочная железа | эпителий | ||
| D17 | собака | остеосаркома | ||||
| DH82 | собака | гистиоцитоз | моноциты/макрофаги |
|
||
| DU145 | человек | карцинома | простата | |||
| DuCaP | Dura mater Cancer of the Prostate | человек | метастазирующий рак простаты | эпителий | 11317521 | |
| EL4 | мышь | T-клеточная лейкемия | ||||
| EMT6/AR1 | мышь | молочная железа | эпителий | |||
| EMT6/AR10.0 | мышь | молочная железа | эпителий | |||
| FM3 | человек | метастазы в лимфатический узел | меланома | |||
| H1299 | человек | лёгкие | рак | |||
| H69 | человек | лёгкие | ||||
| HB54 | гибридома | гибридома | секретирует MA2.1 mAb (против HLA-A2 и HLA-B17) | |||
| HB55 | гибридома | гибридома | секретирует L243 mAb (против HLA-DR) | |||
| HCA2 | человек | фибробласты | ||||
| HEK-293 | human embryonic kidney | человек | почка(эмбриональная) | эпителий | ||
| HeLa | Henrietta Lacks | человек | рак шейки матки | эпителий | ||
| Hepa1c1c7 | clone 7 of clone 1 hepatoma line 1 | мышь | гепатома | эпителий |
(недоступная ссылка) |
|
| HL-60 | human leukemia | человек | миелобласты | клетки крови | ||
| HMEC | human mammary epithelial cell | человек | эпителий | |||
| HT-29 | человек | эпителий толстого кишечника | аденокарцинома |
|
||
| Jurkat | человек | T-клеточная лейкемия | белые клетки крови |
|
||
| JY | человек | лимфобласты | В-клетки, иммортализованные EBV | |||
| K562 | человек | лимфобласты | хроническая миелоидная лейкемия | |||
| Ku812 | человек | лимфобласты | эритролейкемия |
|
||
| KCL22 | человек | лимфобласты | хроническая миелоидная лейкемия | |||
| KYO1 | Kyoto 1 | человек | лимфобласты | хроническая миелоидная лейкемия | ||
| LNCap | Lymph node Cancer of the Prostate | человек | аденокарцинома простаты | эпителий | (недоступная ссылка) | |
| Ma-Mel 1, 2, 3….48 | человек | линии клеток меланомы | ||||
| MC-38 | мышь | аденокарцинома | ||||
| MCF-7 | Michigan Cancer Foundation-7 | человек | молочная железа | инвазивная карцинома протоков молочной железы | ER+, PR+ | |
| MCF-10A | Michigan Cancer Foundation | человек | молочная железа | эпителий | ||
| MDA-MB-231 | M.D. Anderson — Metastatic Breast | человек | молочная железа | рак | ||
| MDA-MB-468 | M.D. Anderson — Metastatic Breast | человек | молочная железа | рак | ||
| MDA-MB-435 | M.D. Anderson — Metastatic Breast | человек | молочная железа | меланома или карцинома (единого мнения нет) | ||
| MDCK II | Madin Darby canine kidney | собака | почка | эпителий | ||
| MOR/0.2R | человек | лёгкие | ||||
| NCI-H69/CPR | человек | лёгкие | ||||
| NCI-H69/LX10 | человек | лёгкие | ||||
| NCI-H69/LX20 | человек | лёгкие | ||||
| NCI-H69/LX4 | человек | лёгкие | ||||
| NIH-3T3 | National Institutes of Health, 3-day transfer, inoculum 3 x 10 5 cells | мышь | эмбрион | фибробласты | ||
| NALM-1 | периферическая кровь | хроническая миелоидная лейкемия | ||||
| NW-145 | меланома | от 16 ноября 2011 на Wayback Machine | ||||
| OPCN / OPCT | Onyvax Prostate Cancer…. | человек | линии клеток рака простаты | от 7 июля 2011 на Wayback Machine | ||
| Peer | человек | T-клеточная лейкемия | ||||
| PNT-1A / PNT 2 | линии клеток рака простаты | |||||
| RenCa | Renal Carcinoma | мышь | карцинома почки | |||
| RIN-5F | мышь | поджелудочная железа | ||||
| RMA/RMAS | мышь | T-клеточный рак | ||||
| Saos-2 | человек | остеоксаркома | ||||
| Sf-9 | Spodoptera frugiperda | бабочка Spodoptera frugiperda | яичник | |||
| SkBr3 | человек | карцинома молочной железы | ||||
| T2 | человек | гибридома В-клеток и Т-клеточной лейкемии | ||||
| T-47D | человек | молочная железа | карцинома протоков | |||
| T84 | человек | карцинома толстого кишечника/ метастазы в легкое | эпителий | |||
| THP1 | человек | моноциты | острая миелоидная лейкемия | |||
| U373 | человек | глиобластома-астроцитома | эпителий | |||
| U87 | человек | глиобластома-астроцитома | эпителий | |||
| U937 | человек | лейкемическая моноцитарная лимфома | ||||
| VCaP | Vertebra Prostate Cancer | человек | метастазирующий рак простаты | эпителий | от 19 февраля 2012 на Wayback Machine | |
| Vero | 'Vera Reno' ('почка зелёной') / 'Vero' ('истина') | африканская зелёная мартышка | эпителий почки | |||
| WM39 | человек | кожа | первичная меланома | |||
| WT-49 | человек | лимфобласты | ||||
| X63 | мышь | меланома | ||||
| YAC-1 | мышь | лимфома | ||||
| YAR | человек | B-лимфоциты | трансформированы EBV | от 20 сентября 2008 на Wayback Machine |