Interested Article - Оксимы
- 2021-02-24
- 1
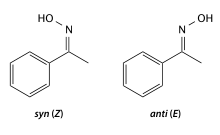
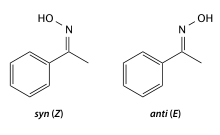
Оксимы (или изонитрозосоединения ) — органические соединения , включающие в себя одну или несколько изонитрозогрупп RR 1 C=N-OH. Обычно рассматриваются как производные альдегидов (R 1 = H) — альдоксимы и кетонов — кетоксимы . Для альдоксимов и оксимов несимметричных кетонов характерна цис - транс -изомерия по связи C=N.
Физические свойства
Оксимы обычно легкоплавкие твердые вещества, в чистом виде — белого цвета. Плохо растворяются в воде, хорошо в органических растворителях. Цис- и транс- изомеры различаются по физическим свойствам (температура плавления, спектры), взаимное превращение стереоизомеров происходит при действии кислот или облучении светом.
В ИК-области в спектрах оксимов наблюдаются слабые полосы валентных колебаний связей O-H при 3650-3500 см −1 и C=N при 1690—1650 см −1 ; валентные колебания N-O обуславливают сильную полосу поглощения при 960—930 см −1 .
Методы синтеза
Синтез с образованием связи C=N
Наиболее распространенным лабораторным методом синтеза оксимов является реакции альдегидов и кетонов с гидроксиламином :
- CH 3 COCH 3 + NH 2 OH CH 3 (C=N-OH)CH 3 + H 2 O
Сходным методом является взаимодействие водного гидроксиламина с алкинами , формально являющимися предшественниками карбонильных соединений :
- R 1 С≡СR 2 + H 2 NOH R 1 СH 2 C(=N-OH)R 2
Другим широко используемым методом является изомеризация нитрозосоединений , содержащих водород в α-положении к нитрозогруппе:
Такая изомеризация проходит in situ при нитрозирования некоторых алканов (например, циклогексана нитрозилхлоридом NOCl) или соединений с активированной метильной либо метиленовой группой:
- PhCOCH 3 + C 5 H 11 ONO [ PhCOCH 2 N=O ] PhCOCH=N-OH
Аналогично проходит нитрозирование некоторых замещенных толуолов: нитротолуолы при взаимодействии с алкилнитритами в присутствии алкоксидов образуют соответствуюцие альдоксимы.
Нитрозирование замещенных нитрометанов также приводит к вводу оксимной группы при атоме углерода с образованием геминальных нитрооксимов - нитроловых кислот :
- RCH 2 NO 2 + HNO 2 RC(NO 2 )=NOH + H 2 O
Окисление или восстановление азота в C-N - соединениях
Оксимы также могут быть синтезированы окислением первичных аминов:
- RR 1 CH-NH 2 + H 2 O 2 RR 1 C=NOH + H 2 O
либо восстановлением нитросоединений :
- RCH 2 NO 2 + [H] RCH=NOH + H 2 O
Введение фрагмента CH=NOH
Специфическим методом синтеза ароматических оксимов является прямое введение альдоксимной группы в ароматическое ядро конденсацией бензола, его алкилпроизводных и фенолов с фульминатом ртути в присутствии хлорида алюминия :
- C 6 H 6 + Hg(ONC) 2 C 6 H 5 CH=NOH
Реакционная способность
Оксимы проявляют амфотерные свойства , являясь как очень слабыми основаниями, так и слабыми кислотами (pK a ~ 11, pK b ~ 12).
Оксимы под действием алкоголятов щелочных металлов депротонируются, образуя соответствующие соли, они также могут образовывать соли с переходными металлами , в последнем случае возможно комплексообразование , особенно в случае бидентантных оксимов. Так, например, диметилглиоксим (реактив Чугаева) образует с двухвалентным никелем прочный нерастворимый комплекс; эта реакция используется для гравиметрического определения никеля.
Реакции по нуклеофильным центрам
Подобно карбонильному углероду альдегидов и кетонов, углерод оксимной группы является электрофильным центром, однако его электрофильность существенно ниже карбонильного углерода из-за меньшей, чем у кислорода, электроотрицательности азота.
Оксимы являются амбидентантными нуклеофилами, способными алкилироваться и по атому кислорода, и по атому азота: так, соли оксимов с щелочными металлами алкилируются алкилгалогенидами с образованием O-алкилоксимов:
- RR 1 C=NOH + C2H5ONa RR 1 C=NONa + C2H5OH
- RR 1 C=NONa + R 2 I RR 1 C=NOR 2 + NaI
Алкилирование может идти и по атому азота, в этом случае образуются нитроны , к образованию нитронов ведет также присоединение к оксимам α,β-ненасыщенных карбонильных соединений :
При взаимодействии с азотистой кислотой кетоксимы образуют N-нитроимины :
- R 2 C=NOH + HNO 2 R 2 C=N-NO 2 + H 2 O
Окисление и восстановление оксимов
Энергичными восстановителями оксимы восстанавливаются до аминов , также возможно восстановление до N-замещенных гидроксиламинов.
Оксимы дегидрируются с образованием иминоксильных радикалов:
- R 2 C=NOH R 2 C=N-O •
Под действием перокситрифторуксусной кислоты, получаемой in situ из трифторуксусного ангидрида и перекиси водорода , оксимы окисляются до нитросоединений ; в случае циклогексаноноксима реакцию проводят в кипящем ацетонитриле в присутствии буфера, при окислении оксимов α-дикетонов в α-нитрокарбонильные соединения в качестве растворителя может быть использован хлороформ или трифторуксусная кислота, необходимости в буфере в этом случае нет, предполагается, что первоначально образуется аци -форма нитросоединения , которая затем таутомеризуется:
- RCOCR=NOH + CF 3 COOOH RCOCR=NO(OH) RCOCHRNO 2
N-бромсукцинимид (NBS) реагирует с оксимами с образованием соответствующего гем -бромнитрозопроизводного:
- R 2 C=NOH + NBS R 2 CBr(NO)
Под действием азотной кислоты кетоксимы дают гем -нитронитрозосоединения ( ):
- R 2 C=NOH + HNO 3 R 2 CNO(NO 2 ) ,
альдоксимы нитруются до изомерных (и, в случае альдоксимов и таутомерных) псевдонитролам нитроловых кислот :
- RCH=NOH + HNO 3 R(CO)C(NO 2 )=NOH + H 2 O
Ароматические альдоксимы хлорируются с образованием гидроксамоилхлоридов (хлорангидридов иминных таутомеров гидроксамовых кислот , которые, в свою очередь, могут быть превращены в :
- Ph-CH=NOH + Cl 2 Ph-CCl=NOH + HCl
- Ph-CCl=NOH + Et 3 N Ph-C≡N + -O -
Под действием кислотных и ацилирующих агентов (PCl 5 , P 2 O 5 , полифосфорные кислоты, хлорангидриды сульфокислот и карбоновых кислот) альдоксимы отщепляют воду с образованием нитрилов :
- RCH=NOH + Ac 2 O RCN + 2 AcOH
Кетоксимы в таких условиях перегруппировываются в амиды .
Перегруппировки оксимов
Кетоксимы под действием кислотных и ацилирующих агентов перегруппировываются в амиды ( Перегруппировка Бекмана ). Перегруппировка стереоспецифична — к азоту мигрирует радикал, находящийся в транс-положении к гидроксилу:
- RR 1 C=NOH RCONHR 1
Перегруппировка Бекмана циклогексаноноксима является промышленным методом синтеза капролактама — мономера капрона (найлона-6):
Перегруппировку Бекмана также претерпевают O-замещённые кетоксимы (сложные эфиры оксимов, перегруппировка Бекмана-Чепмена):
- RR 1 C=NOR 2 RCONR 1 R 2
Перегруппировка Бекмана может проходить и под действием P 2 S 5 , выступающего в роли и катализатора перегруппировки, и тионирующего агента, продуктом реакции в этом случае являются тиоамиды . Так, бензальдоксим в этих условиях образует :
- PhCH=NOH + P 2 S 5 PhCSNH 2 ,
бензофеноноксим перегруппировывается в тиобензанилид :
- (Ph) 2 C=NOH + P 2 S 5 PhCSNHPh
α-Гидроксикетоксимы в условиях перегруппировки Бекмана расщепляются с образованием альдегида и нитрила (расщепление по Бекману или перегруппировка Вернера):
- RCH(OH)CR 1 =NOH RCHO + R 1 CN + H 2 O
O-сульфонаты оксимов алифатических кетонов под действием оснований претерпевают перегруппировку, образуя азирины , гидролизующиеся далее до α-аминокетонов ( перегруппировка Небера ), эта реакция является синтетическим методом α-аминирования кетонов :
Применение
Некоторые оксимы ( аллоксим , диэтиксим , дипироксим , изонитрозин , пралидоксим ) являются реактиваторами холинэстеразы и используются в качестве антидотов при отравлениях фосфорорганическими инсектицидами.
является крупнотоннажным продуктом, используемым в производстве капролактама .
Диметилглиоксим используется в аналитической химии для обнаружения и количественного определения никеля («реактив Чугаева »), никелевый комплекс этого вещества ( ) используется в качестве красного пигмента.
См. также
Примечания
- IUPAC Gold Book: от 21 октября 2012 на Wayback Machine
- . Organic Syntheses . 90 : 87. 2013. doi : . eISSN . ISSN . из оригинала 7 февраля 2021 . Дата обращения: 2 февраля 2021 .
- Nakama, Kimitaka; Sumito Seki, Shuji Kanemasa. (англ.) // : journal. — 2001. — Vol. 42 , no. 38 . — P. 6719—6722 . — ISSN . — doi : .
- Silva, Emerson (2018). . Organic Syntheses . 95 : 192—204. doi : . ISSN . Дата обращения: 23 февраля 2021 .
- (англ.) // : journal. — 1969. — Vol. 49 . — P. 70 . — ISSN . — doi : . 15 марта 2016 года.
- Li, Jiangsheng; Cheng, Chao; Zhang, Xinrui; Li, Zhiwei; Cai, Feifei; Xue, Yuan; Liu, Weidong. (англ.) // Chinese Journal of Chemistry : journal. — 2012. — Vol. 30 , no. 8 . — P. 1687—1689 . — ISSN . — doi : . 27 октября 2016 года.
- Ferguson, Lloyd N. (англ.) // : journal. — 1946. — Vol. 38 , no. 2 . — P. 227—254 . — ISSN . — doi : .
- P. W. Neber, A. v. Friedolsheim: Über eine neue Art der Umlagerung von Oximen. In: 1926, 449. 109—134.
- 2021-02-24
- 1





























