Interested Article - Тозилхлорид
- 2020-08-29
- 2
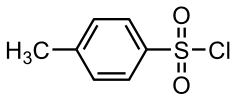
пара -Толуолсульфонилхлорид (тозилхлорид, TsCl) — органическое соединение, хлорангидрид , реагент для образования производных данной сульфокислоты при реакциях с соединениями различных классов .
Очистка
При длительном хранении соединение разлагается водой до пара-толуолсульфокислоты и хлороводорода . Очистить его можно путём растворения в минимальном количестве хлороформа с последующим фильтрованием и разбавлением 5-кратным объёмом легкокипящего петролейного эфира для осаждения примесей. Полученный раствор фильтруют, обесцвечивают активированным углём и упаривают, получая чистый продукт в виде белых кристаллов .
Также тозилхлорид можно очистить перекристаллизацией из петролейного эфира, бензола или смеси толуола с петролейным эфиром. Раствор тозилхлорида в диэтиловом эфире можно промыть 10 %-ным раствором NaOH , высушить и выкристаллизовать вещество при охлаждении на льду .
Использование
Обычным применением тозилхлорида является его реакция со спиртами , приводящая к образованию эфиров пара-толуолсульфокислоты (тозилирование). В качестве основания в этой реакции используют пиридин , а оптимальное соотношение спирта, тозилхлорида и пиридина составляет 1:1,5:2. С хорошим выходом тозилирование можно провести и в гетерофазной системе при участии в качестве .
Реакция тозилирования протекает с участием первичных гидроксильных групп в присутствии вторичных. Также существуют примеры селективного тозилирования аминогрупп в присутствии гидроксильных групп и наоборот. Стереохимия хирального атома углерода при гидроксильной группе в ходе тозилирования не затрагивается .
Иногда тозилхлорид выступает как хлорирующий реагент. В частности его комбинация с 4-диметиламинопиридином превращает аллильные, пропаргильные и гликозидные спирты в соответствующие хлориды, в то время как для вторичных алифатических гидроксильных групп реакция останавливается на стадии тозилатов .
Смешивание карбоновой кислоты с тозилхлоридом в пиридине позволяет эффективно получить симметричный . Если делать это в присутствии спирта, с высоким выходом получается сложный эфир . Особенно этот метод важен для третичных спиртов. Во время данной реакции кислота постоянно превращается в ангидрид в присутствии спирта, что позволяет использовать её в реакции максимально полно .
Безопасность
Тозилхлорид чувствителен к влаге и обладает лакриматорным действием .
Примечания
- 2020-08-29
- 2