К переименованию
- 1 year ago
- 0
- 0

Водяной лёд (от др.-греч. λίθος – камень ) — один из самых распространённых минералов на Земле . В минералогии Группа льда входит в класс Простых и сложных окислов , но выделяется по своим уникальным свойствам .
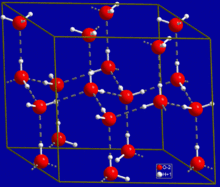
Лед обладает молекулярной кристаллической структурой, в локальном отношении близкой к структуре алмаза (каждая молекула Н 2 О имеет координационное число 4). По общему расположению молекул структура льда аналогична структуре вюртцита , но неупорядочена по атомам водорода.
Обычно кристаллы снега ( Снежинка или иней ) имеют сложную 6-лучевую звёздную фигуру роста различной формы с гексагональной симметрией ( Гексагональная сингония ).
В морозные дни выпадают Ледяные иглы . Широко известны дендриты и узорчатые образования льда. В ледяных пещерах кристаллы льда встречаются в виде правильных шестиугольных пластинок, таблитчатых индивидов и сложных по форме сростков. Известны уникальные по величине и хорошему огранению кристаллы льда (до 40 см в длину и до 15 см в поперечнике), встреченные на северо-востоке Азии в горных выработках в условиях вечной мерзлоты.
По международной классификации :
Статические идеи системы природы К. Линнея отводили малое значение изучению воды в минералогии . Воду рассматривали, как объект исследования географии .
Вода имеет исключительное значение не только в химии , физике (см. лёд ) но и в минералогии . В генезисе многих минералов принимает участие вода. Она часто играет определяющую роль и позволяет объяснить происхождение большинства минералов. Это подтверждает, что природные воды сами принадлежат к числу минералов. [ источник не указан 2148 дней ]
В 1931 году В. И. Вернадский обратил особое внимание на изучение воды как минерала . Он выделил соединения кислорода с водородом в :
Вода как геологическое явление существует на Земле несколько миллиардов лет и имеет более 1000 разновидностей (В. И. Вернадский описал около 540 из них) .

В зависимости от условий (температура, давление, удельный объём) лёд может быть в нескольких модификациях :
Аморфный лёд возникает при конденсации паров воды на поверхности охлаждённой до −160° С, существует при температурах ниже −130° С.
Лёд распространён во вселенной, огромные массы льда находятся на различных планетах.
Водяной лед в межзвёздном пространстве может принимать различные кристаллические и аморфные формы в зависимости от температуры и давления. Кристаллизация первоначально аморфного льда происходит при температурах около 90 К (или −183°С). Это изменение фазы необратимо. Межзвездный лёд, при температурах ниже 90 К, находится в основном в плотной аморфной фазе .