Interested Article - Оксид бора
- 2020-10-15
- 1
Окси́д бо́ра ( сесквиоксид бора , борный ангидрид ) — бинарное неорганическое химическое соединение бора с кислородом , ангидрид борной кислоты , бесцветное, довольно тугоплавкое, стекловидное или кристаллическое вещество, диэлектрик .
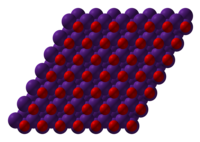
Стеклообразный оксид бора имеет слоистую структуру (расстояние между слоями 0,185 нм), в слоях атомы бора расположены внутри равносторонних треугольников (d В—О=0,145 нм). Эта модификация плавится в интервале температур 325—450 °C и обладает высокой твёрдостью. Она получается при нагревании бора на воздухе 700 °C или обезвоживанием ортоборной кислоты . Кристаллический , который получают осторожным отщеплением воды от метаборной кислоты , существует в двух модификациях — с гексагональной кристаллической решёткой , при 400 °C и 2200 МПа переходящей в моноклинную .
Свойства
- Борный ангидрид гигроскопичен, он бурно растворяется в воде, образуя вначале различные метаборные кислоты общей формулы . Дальнейшее оводнение приводит к образованию ортоборной кислоты .
- Расплавленный хорошо растворяет оксиды многих элементов. С оксидами металлов образует соли бораты .
- является кислотным ангидридом , проявляя также очень слабые признаки амфотерности :
-
С соляной кислотой реагирует при нагревании (
):
- Сам оксид бора не восстанавливается углеродом даже при температуре белого каления, однако разлагается, если одновременно ввести в реакцию вещества, способные заместить кислород (хлор или азот):
- При нагревании оксида бора с элементарным бором выше 1000 о в парах существуют термически устойчивые линейные молекулы O=B—B=O. При быстром охлаждении паров ниже 300 о может быть получен белый твёрдый полимер состава , не имеющий определённой точки плавления и сильно реакционноспособный. Под давлением в 60 тыс. ат. и температуре 1500 о оксид бора взаимодействует с элементарным бором по реакции:
-
- Этот имеет графитоподобную слоистую структуру.
Получение
Образуется при нагревании бора в атмосфере кислорода или на воздухе
А также при обезвоживании борной кислоты :
Применение
- Исходный материал для синтеза других соединений бора , таких как карбид бора .
- Добавка, используемая в стекловолокне (оптических волокнах).
- Используется в производстве боросиликатного стекла.
- Используется в качестве кислотного катализатора в органическом синтезе .
Биологическая роль
Токсикология
Оксид бора B 2 O 3 (сесквиоксид бора; ангидрид борной кислоты) по степени воздействия на организм человека относится к веществам 3-го класса опасности ("умеренно-опасное" химическое вещество ).
Высокотоксичен для насекомых.
Предельно допустимая концентрация оксида бора в воздухе рабочей зоны составляет 5 мг/м 3 .
Реактив пожаро- и взрывобезопасен.
Вдыхание пыли оксида бора, судя по всему, может вызвать раздражение слизистых оболочек.
В больших концентрациях оксид бора может обладать гонадотропным или гепатотоксическим действием .
Примечания
- (англ.) . — The Electrochemical Society, 2000. — P. 496. — ISBN 1-56677-261-3 .
- ↑
- (англ.) : A CRC quick reference handbook — CRC Press , 1993. — ISBN 978-0-8493-4498-5
Литература
- Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия. М.: Химия 1994
- Реми Г. «Курс неорганической химии» М.: Иностранная литература, 1963
- 2020-10-15
- 1