Interested Article - Монохлоруксусная кислота

- 2020-08-16
- 1
Монохлоруксусная кислота CH 2 ClCOOH — уксусная кислота , в которой один атом водорода метильной группы замещён на атом хлора, бесцветные кристаллы.
Физические свойства
t пл 61,2 °C t кип 189,3 °C. Растворима в воде , спирте , ацетоне , эфире .
Применение
Монохлоруксусная кислота — промежуточный продукт в синтезе индиго и многих др. кубовых красителей; её применяют также при получении карбоксиметилцеллюлозы , снотворного средства барбитала , гербицидов (например, солей и эфиров 2,4-дихлорфеноксиуксусной кислоты), витамина B6 .
Иллюстрацией её полезности в органической химии является O -алкилирование салицилового альдегида хлоруксусной кислотой с последующим декарбоксилированием образовавшегося эфира , получая бензофуран .
Большинство реакций используют высокую реакционную способность связи C-Cl. Она прекурсор для гербицида глифосата . Гербицид (2-метил-4-хлорофенокси уксусная кислота) был получен алкилированием хлоруксусной кислотой. Хлоруксусную кислоту переводят в хлорацетилхлорид, прекурсор адреналина .
Замещение хлора серой даёт тиогликолевую кислоту, которая используется как стабилизатор ПВХ и иногда как компонент в косметике. Наибольшее количество хлоруксусной кислоты используется для приготовления загустителя — карбоксиметилцеллюлозы .
Получение
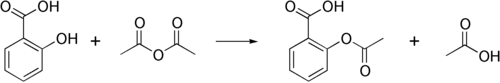
В основном получают монохлоруксусную кислоту хлорированием ледяной уксусной кислоты при катализе уксусным ангидридом:
Другой промышленный метод — гидролиз трихлорэтилена
Гидролиз даёт чистый продукт, тогда как при хлорировании необходимо проводить сложную дистилляцию для отделения моно- би- трихлоруксусных кислот .
Годовое производство хлоруксусной кислоты составляет ориентировочно 420 тыс. тонн.
При взаимодействии хлора с уксусной кислотой в присутствии небольшого количества красного фосфора, образуется смесь моно-, ди- и трихлоруксусной кислот.
Безопасность
Как и другие галогенкислоты и галогеналканы, хлоруксусная кислота — потенциально опасный алкилирующий агент. ЛД50 на крысах 76 мг/кг
Примечания
- (англ.) : A CRC quick reference handbook — CRC Press , 1993. — ISBN 978-0-8493-4498-5
- Burgstahler, A. W.; Worden, L. R. (1966). « от 14 июня 2012 на Wayback Machine .» 46 : 28.
- Günter Koenig, Elmar Lohmar, Norbert Rupprich «Chloroacetic Acids» in Ullmann’s Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi :
Литература
- Химическая энциклопедия / Редкол.: Зефиров Н.С. и др.. — М. : Большая Российская энциклопедия, 1998. — Т. 5 (Три-Ятр). — 783 с. — ISBN 5-85270-310-9 .
- 2020-08-16
- 1