Хлорид рутения(III)
- 1 year ago
- 0
- 0
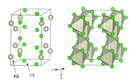
Хлорид родия(III) (трихлорид родия) — неорганическое соединение , соль родия и соляной кислоты с формулой RhCl 3 , один из трёх известных хлоридов родия , соответствующий трёхвалентному металлу. Красно-коричневый порошок, нерастворим в воде. Образует кристаллогидрат состава RhCl 3 •3H 2 O, хорошо растворимый в воде. Применяется для родирования — нанесения родиевых покрытий на металлы и как катализатор в органическом синтезе . Также находит применение в фотографии и производстве фотобумаг.
Имеет вид красных кристаллов с моноклинной сингонией . Не растворяется в воде и кислотах, а также в растворах щелочей. Возгоняется около 800 °С и разлагается при 970 °С .
Образует кристаллогидрат RhCl 3 •nH 2 O, выглядящий как стекловидная масса (по другим данным способен образовывать кристаллы) красного цвета. Соединение является полиядерным и имеет переменный состав, Мейер и Кавчик приписали этому соединению состав тригидрата RhCl 3 •3H 2 O .
Кристаллогидрат хорошо растворим в воде, образуя при этом красно-коричневый раствор. Выпаривание раствора снова даёт стеклообразную массу .
В солянокислых растворах соединение находится в форме иона [RhCl 6 ] 3- , либо замещённых аквакомплексов этого иона .
В составе позитивных фотографических эмульсий сильно снижает светочувствительность и также сильно увеличивает контрастность , даже в крайне незначительных количествах, позволяя получать коэффициент контрастности γ = 5. Для обычных эмульсий, где достаточно γ = 4, использование хлорида родия не требуется .
В связи с тем, что трихлорид родия крайне нестабилен в растворах, вместо него можно применять гексахлорородат(III) аммония (RhCl 6 (NH 4 ) 3 •H 2 O), который используют в количествах порядка 0,4 мг / литр эмульсии. Это двойное соединение малопригодно для бромосеребряных эмульсий, которые уже через три месяца теряют контрастность и из особоконтрастных превращаются просто в контрастные. Однако с хлоридом серебра данный двойной хлорид образует достаточно стабильные комплексы .
Безводное соединение получают действием хлора на нагретый порошкообразный родий. Реакция начинает протекать при температуре 250—300 °C, в промышленном процессе температура удерживается в диапазоне 900—948 °C, выше 948 °C трихлорид начинает переходить в дихлорид :
Помимо этого, трихлорид может быть получен другими способами, все из которых протекают при нагревании в токе хлора: из сульфида родия, хлоропентааминхлорида родия, сплава родия с оловом (при 360—440 °C). Для получения соединения, не содержащего примесей щелочных металлов, используют гексахлорородиат(III) аммония, реакцию также ведут в токе хлора при температуре в 440 °C .
Кристаллогидрат получают, растворяя свежеполученный гидроксид родия(III) в соляной кислоте с последующим выпариванием досуха :
Тригидрат применяют для приготовления электролитов, предназначенных для родирования металлических поверхностей. Также тригидрат используют в органическом синтезе, как катализатор в реакциях изомеризации и полимеризации алкенов .
В фотографии вместе с другими хлоридами металлов платиновой группы может использоваться для тонирования отпечатков, замещая серебро с образованием металлического родия и нерастворимого галогенида серебра в кислой среде :
Используется при производстве фотобумаг с очень высокой степенью контрастности .