Interested Article - Марганцево-цинковый элемент

- 2020-07-20
- 1
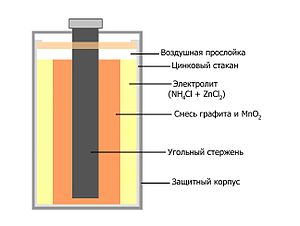
Марганцево-цинковый элемент , солевой элемент питания , также известный как элемент Лекланше — это первичный химический источник тока , в котором катодом является пиролюзит ( диоксид марганца MnO 2 ) в смеси с графитом (около 9,5 %), электролитом — раствор хлорида аммония NH 4 Cl , анодом — металлический цинк Zn .
Марганцево-цинковый элемент является известным первичным элементом питания одноразового использования, и на сегодняшний день широко используется в переносных устройствах. Изначально элементы заполнялись жидким электролитом. В дальнейшем электролит стали загущать с помощью крахмалистых веществ — это позволяло сделать более практичные элементы питания, называемые сухими, в которых возможность вытекания электролита сведена к минимуму. В отличие от щелочного элемента , в котором в качестве электролита используется щелочь KOH , марганцево-цинковый элемент является солевым, так как в нем в качестве электролита используется соль — хлорид аммония .
История изобретения
Первый марганцево-цинковый элемент был собран Жоржем Лекланше в 1865 году . Хотя образец элемента по своим параметрам уступал известным в то время образцам Даниэля Якоби и Бунзена Вильгельма , вскоре элементы Лекланше заняли первое место. Простота и безопасность в изготовлении и эксплуатации, широкий интервал рабочих температур и другие преимущества обеспечили интенсивное развитие производства этих элементов. Уже в 1868 г. их было выпущено более 20 тыс. шт.
Характеристики
|
|
В разделе
не хватает
ссылок на источники
(см.
рекомендации по поиску
).
|
-
Теоретическая
энергоёмкость
:
- Удельная энергоёмкость: 67—99 Вт∙час/кг
- Удельная энергоплотность: 122—263 Вт∙час/дм³.
- ЭДС : 1,51 В.
- Рабочая температура: от −40 до +55 °C.
Принцип действия

При потреблении тока электроны поступают через внешнюю электрическую цепь с цинкового электрода на угольный стержень. Происходят следующие реакции:
Анод: Zn → Zn 2+ + 2e −
На угольном стержне электроны расходуются на восстановление H 3 O + - ионов:
Катод: 2H 3 O + + 2e − → H 2 + 2H 2 O
Ионы H 3 O + образуются в результате частичного протолиза NH 4 + - ионов электролита:
NH 4 + + H 2 O ↔ H 3 O + + NH 3
При восстановлении H 3 O + - ионов образуется водород , который не может удалиться (корпус герметичен) и образует вокруг угольного стержня прослойку газа ( поляризация угольного электрода). Из-за этого ток медленно затухает. Чтобы избежать образования водорода, угольный электрод окружают слоем диоксида марганца (MnO 2 ). В присутствии диоксида марганца H 3 O + -ионы восстанавливаются с образованием воды:
2MnO 2 + 2H 3 O + + 2e − → 2MnO (OH) + 2H 2 O
Таким способом избегают поляризации электрода, а диоксид марганца называют деполяризатором.
Электролит NH 4 Cl диссоциирует и частично протолизируется:
2NH 4 Cl + 2H 2 O ↔ 2NH 3 + 2H 3 O + + 2Cl −
Образующиеся на аноде ионы Zn 2+ поступают в раствор и образуют труднорастворимую соль :
В общем:
Общая реакция: Zn + 2MnO 2 + 2NH 4 Cl → 2MnO (OH) + [Zn (NH 3 ) 2 ]Cl 2 Во время разрядки цинковый стакан растворяется. Во избежание вытекания электролита или продуктов реакции стаканчик имеет запас по толщине или окружён железной защитной оболочкой.
Устройство
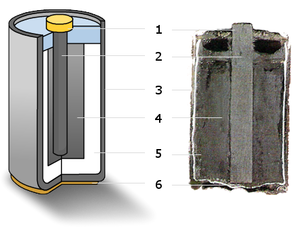
(1) — металлический колпачок,
(2) — графитовый электрод («+»),
(3) — цинковый стакан («—»),
(4) — оксид марганца,
(5) — электролит,
(6) — металлический контакт.
В качестве электродов в «сухом элементе» выступают цинковый стакан и угольный стержень. Поэтому сухой элемент называют ещё угольно-цинковым. Положительным электродом «+» является угольный стержень, отрицательным — цинковый стакан. Угольный стержень окружен смесью диоксида марганца MnO 2 и угля (сажи). В качестве электролита выступает раствор хлорида аммония NH 4 Cl с небольшой добавкой хлорида цинка ZnCl 2 , загущённый крахмалом и мукой — это необходимо для того, чтобы электролит не мог вытечь или высохнуть при хранении и эксплуатации элемента. Тем не менее при неправильной эксплуатации или слишком длительном хранении электролит всё же может потечь или высохнуть.
Производство
|
|
Этот раздел
не завершён
.
|
Хранение и эксплуатация
|
|
Этот раздел
не завершён
.
|

Восстановление работоспособности
По мере разрядки цинковый стакан покрывается слоем цинкдиамминхлорида, за счёт чего увеличивается внутреннее сопротивление элемента. Частично восстановить ёмкость элемента можно, если удалить слой цинкдиамминхлорида с поверхности цинкового стакана. Сделать это удаётся несколькими способами:
- путём деформации цинкового стакана
- подачей на выводы батареи переменного тока особой формы.
Второй способ нередко ошибочно называют перезарядкой. Оба способа сопряжены с риском повреждения цинкового стакана и подтекания электролита. Более того этот способ может также привести к взрыву элемента.
Другой распространённой причиной потери ёмкости является высыхание электролита. Это обычно происходит в тех случаях, когда элемент используется в течение длительного времени в устройствах, потребляющих небольшой ток (например, электронных часах), либо после длительного хранения. В этом случае восстановление работоспособности возможно после шприцевания батарейки водой, однако после этого необходимо плотно закрыть отверстие, иначе электролит может в скором времени снова высохнуть, либо начать подтекать.
Ещё одной известной неисправностью является коррозия (окисление) цинкового стакана. В результате окисления происходит истончение стакана, а также (при окислении контактных площадок) — увеличение сопротивления элемента. Коррозия в дальнейшем может также перекинуться на другие металлические детали, расположенные близко к батарее. Окислившийся элемент восстановлению не подлежит.
-
 Цинковый стаканчик («-» электрод) частично вскрыт, под ней бумажный стаканчик, пропитанный электролитом и залитый битумной мастикой
Цинковый стаканчик («-» электрод) частично вскрыт, под ней бумажный стаканчик, пропитанный электролитом и залитый битумной мастикой -
 Цинковый стаканчик удалён, угольный стержень («+» электрод), впрессованный в «+» контакт-крышку, демонтирован
Цинковый стаканчик удалён, угольный стержень («+» электрод), впрессованный в «+» контакт-крышку, демонтирован -
 Внутри бумажного стаканчика прессованный марганцево-графитный порошок с каналом для «+» электрода
Внутри бумажного стаканчика прессованный марганцево-графитный порошок с каналом для «+» электрода
Области применения
Все первичные источники тока, за исключением серебряно-цинкового, обладают большим внутренним сопротивлением — десятки Ом, не допускающим разряда их токами большой силы из-за чрезмерного падения напряжения на внутреннем сопротивлении. Это надо учитывать при использовании их в качестве силовых источников тока.
Наиболее эффективной областью применения солевых батареек являются приборы со средним и низким энергопотреблением, например, в ДУ пультах и часах, по причине более медленного саморазряда [ источник не указан 1057 дней ] солевой батарейки (в сравнении с щелочными элементами питания).
Примечания
- Лекланше элемент — статья из Большой советской энциклопедии .
- . zinref.ru . Дата обращения: 16 октября 2022. 16 октября 2022 года.
Литература
- Кромптон, Т. Первичные источники тока = Small Batteries. Volume 2. Primary Cells. T. R. Crompton. The Macmillan Press Ltd., London, Basingstocke. 1982 : [пер. с англ. ] / Под ред. канд. хим. наук Ю. А. Мазитова. — М. : Мир, 1986. — 328 с. : ил. — ББК 31.251 . — УДК .
- : Источники тока химические. Термины и определения : (С изменением № 1.) Дата введения 1982-07-01.
- : Батареи первичные. Часть 1. Общие требования : Дата введения 2011-07-01.
Ссылки
- . PowerInfo.ru .
- . Энциклопедия Кругосвет .
|
|
В статье есть список
источников
, но
не хватает
сносок
.
|
- 2020-07-20
- 1



