Эмбриогенез животных
- 1 year ago
- 0
- 0
Плодовая мушка Drosophila melanogaster была введена в качестве модельного организма в генетические эксперименты Томасом Морганом в 1909 году и до настоящего времени является одним из самых любимых модельных организмов среди исследователей, изучающих эмбриональное развитие животных. Малый размер, быстрая смена поколений, высокая плодовитость , прозрачность эмбрионов — делают дрозофилу идеальным объектом для генетических исследований.
Дрозофила имеет голометаболический жизненный цикл — три отдельных стадии постэмбрионального развития, отличающиеся строением тела: личинка , куколка и имаго . В ходе эмбриогенеза образуются структуры, необходимые для функционирования организма в течение этих фаз и перехода между ними. В результате эмбриогенеза формируется личинка мухи. Личинка содержит имагинальные диски — группы клеток, из которых затем образуются структуры имаго. На стадии куколки ткани личинки разрушаются, и из имагинальных дисков образуются ткани взрослого организма. Такое развитие называется .
Эмбриогенез дрозофилы уникален среди других модельных организмов тем, что дробление у неё . В результате дробления образуется синцитий . Около 5000 ядер накапливаются в неразделенной цитоплазме и далее мигрируют к поверхности ооцита. Происходит целлюляризация — образование индивидуальных плазматических мембран, при этом обособляются клетки, окружающие желточный мешок . Первыми на заднем конце эмбриона отделяются полярные клетки ( ).
Как и у других трехслойных многоклеточных , гаструляция приводит к образованию трех зародышевых листков — энтодермы , мезодермы и эктодермы .
Мезодерма инвагинирует по вентральной бороздке. Средняя кишка образована эктодермой. Полярные клетки интернализуются другим образом. удлиняется, задняя часть, включая заднюю кишку, растягивается и расширяется к переднему концу по спинной стороне зародыша. На ранних этапах сегментации образуются межсегментные бороздки. В момент формирования трахей появляются первые признаки дыхательной активности. Втягивание зародышевой полоски возвращает заднюю кишку к спинной стороне заднего конца зародыша. Оставшиеся стадии включают в себя интернализацию нервной системы (эктодермального происхождения) и образование внутренних органов.
Одним из наиболее изученных примеров формирования паттернов развития вдоль передне-задней оси является формирование передне-задней оси тела, зависящее от градиентов морфогенов , у плодовой мушки Drosophila melanogaster . Некоторые другие многоклеточные организмы используют сходные механизмы формирования осей тела, хотя относительное значение передачи сигнала между первичными клетками многих развивающихся организмов выше, чем в описанном случае.
Основа для формирования передне-задней оси закладывается во время формирования яйца ( оогенеза ), задолго до момента оплодотворения и откладки яиц.
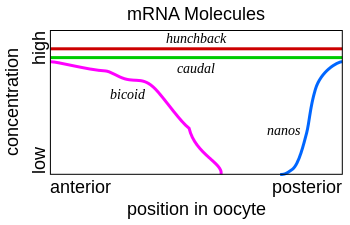
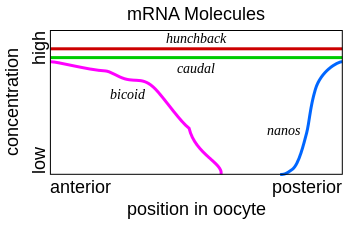
Во время созревания ооцита (nursing cells) синтезируют большое количество РНК и белков, которые переносятся в созревающий ооцит по цитоплазматическим мостикам. Большинство этих молекул бывают необходимы в первые два часа эмбрионального развития дрозофилы, до начала транскрипции в зиготе . Развивающийся ооцит имеет градиенты концентраций мРНК . Гены, которые кодируют такие мРНК, называют генами материнского эффекта . Bicoid и hunchback — это гены материнского эффекта, которые имеют особое значение в формировании передних частей зародыша дрозофилы (головы и груди). Nanos и Caudal — это гены материнского эффекта, которые определяют формирование задних брюшных сегментов зародыша дрозофилы.
В яйце микротрубочки реорганизуются в ходе оогенеза . Сначала центр организации микротрубочек находится у заднего полюса ооцита, и микротрубочки направлены своими ±концами к переднему полюсу ооцита. Однако перед формированием градиентов мРНК генов bicoid и nanos локализация центра организации и положение микротрубочек меняется на противоположное: в этот период они направлены своими ±концами к заднему полюсу яйца . мРНК гена bicoid связывается с микротрубочками и накапливается на переднем конце формирующихся яиц дрозофилы. В неоплодотворенных яйцах транскрипты находятся на самом кончике передней части яйца. Последние данные указывают на то, что сразу после оплодотворения образуется градиент мРНК в результате направленной диффузии мРНК в яйце, видимо, по периферической сети микротрубочек при участии белкового продукта гена Staufen.
мРНК Nanos связана с цитоскелетом яйца, но располагается на заднем конце яйца. мРНК генов Hunchback и caudal теряют системы контроля положения и распределяются практически равномерно в объеме яйца.
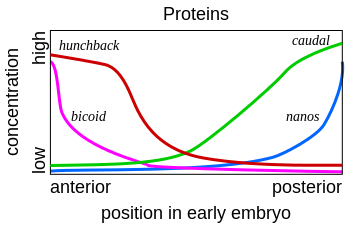
Когда мРНК генов материнского эффекта транслируется в белки, образуются градиенты белка Bicoid на переднем полюсе яйца и белка Nanos—на заднем полюсе. Белок Bicoid блокирует трансляцию мРНК белка caudal , и поэтому белковый продукт этого гена образуется только на заднем конце яйца. Белок Nanos связывает мРНК hunchback и блокирует её трансляцию на заднем конце эмбриона дрозофилы.
Белки Bicoid , Hunchback , и Caudal являются факторами транскрипции . Bicoid имеет ДНК-связывающий гомеодомен , который связывает ДНК и мРНК nanos . Bicoid связывается со специфической последовательностью на 3' нетранслируемом участке мРНК caudal и блокирует трансляцию.
Уровень белка Hunchback в раннем эмбрионе значительно увеличивается за счет трансляции мРНК, которая образована уже зиготой. В течение раннего эмбриогенеза дрозофилы происходит деление ядра без деления цитоплазмы. Множество образующихся ядер расходятся к периферии цитоплазмы. Экспрессия генов в этих ядрах регулируется белками Bicoid, Hunchback, и Caudal. Например, Bicoid является транскрипционным активатором гена hunchback .
Использование направленного мутагенеза позволяет изменять функции генов и следить за изменениями в эмбриогенезе . Существуют способы маркировки белков дрозофилы флюоресцентными белками, например, ( GFP ). Таким образом можно следить за динамикой распределения белкового продукта в клетке. Геном дрозофилы полностью секвенирован . Исследователи могут найти ортологи интересующих генов в геноме дрозофилы и изучить их вклад в эмбриогенез.