Interested Article - Сульфат хрома(II)

- 2021-07-06
- 1
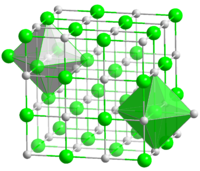
Сульфат хрома(II) — неорганическое соединение, соль металла хрома и серной кислоты с формулой CrSO 4 , бесцветные кристаллы, растворимые в воде, образует кристаллогидраты .
Получение
- Действие на металлический хром разбавленной серной кислоты:
- Действие на разбавленной серной кислоты:
- Восстановление подкисленных растворов сульфата хрома(III) цинком :
Физические свойства
Сульфат хрома(II) образует бесцветные кристаллы, растворимые в воде, водные растворы устойчивы в отсутствие кислорода .
Образует кристаллогидраты состава CrSO 4 • n H 2 O, где n = 1, 2, 4, 5 и 7.
При нормальных условиях образуется кристаллогидрат CrSO 4 •5H 2 O — синие кристаллы триклинной сингонии , параметры ячейки a = 0,724 нм, b = 1,094 нм, c = 0,601 нм, α = 125,32°, β = 97,63°, γ = 94,32°.
Химические свойства
- Водные растворы поглощают кислород :
- В отсутствие окислителя медленно восстанавливает воду , в которой растворён, проявляя свои сильные восстановительные свойства:
- В инертной атмосфере реагирует с растворами щелочей и аммиака с выпадением коричневого осадка гидроксида хрома(II) :
- Реагирует с раствором сульфида натрия с выпадением чёрного осадка сульфида хрома(II) :
- Реагирует с раствором карбоната натрия в инертной атмосфере с выпадением серовато-белого осадка карбоната хрома(II):
Применение
- В аналитической химии, как поглотитель кислорода.
- Катализатор и восстановитель в органической химии.
Литература
- Химическая энциклопедия / Редкол.: Зефиров Н.С. и др.. — М. : Большая Российская энциклопедия, 1998. — Т. 5. — 783 с. — ISBN 5-85270-310-9 .
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л. : Химия, 1971. — Т. 2. — 1168 с.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М. : Мир, 1972. — Т. 2. — 871 с.
- Неорганическая химия / под ред. Ю.Д. Третьякова. — М. : Академия, 2007. — Т. 3. — 352 с.
- 2021-07-06
- 1