Interested Article - Гидроксид марганца(II)

- 2020-07-29
- 1
Гидроксид марганца(II) — неорганическое соединение, гидроксид металла марганца с формулой Mn(OH) 2 , телесные кристаллы, не растворимые в воде.
Описание
Гидроксид марганца(II) — студнеобразный светло-розовый осадок. Нерастворим в воде. Проявляет средне основные свойства. Окисляется на воздухе.
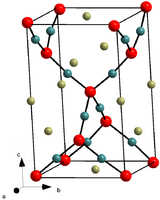
Гидроксид марганца(II) образует белые кристаллы триклинной сингонии , пространственная группа P 3 m1 , параметры ячейки a = 0,334 нм, c = 0,468 нм, Z = 1.
Химические свойства
- Гидроксид марганца (II) легко окисляется на воздухе до бурого оксогидроксида марганца , который далее окисляется до оксида марганца (IV) :
- Гидроксид марганца (II) обладает основными свойствами. Он реагирует с кислотами и кислотными оксидами :
- Гидроксид марганца (II) обладает восстановительными свойствами. В присутствии сильных окислителей он может окисляться до перманганата :
Получение
- Образуется гидроксид марганца (II) при взаимодействии его солей со щелочами:
См. также
- 2020-07-29
- 1