Interested Article - Карбид хрома(II)

- 2020-12-01
- 1
Карбид хрома(II) — химическое соединение металла хрома и углерода с формулой Cr 3 C 2 . Представляет собой упорядоченную фазу с очень узкой областью гомогенности. Содержание углерода в карбиде хрома составляет 13,34% по массе.
Получение
Карбид хрома можно получить одним из следующих способов .
- Непосредственным насыщением хрома углеродом:
-
-
Порошкообразный углерод может быть заменен на углеродосодержащие газы (например
метан
), в этом случае реакция имеет следующий вид:
- где символом (СН) обозначены продукты разложения углеводородов
- Восстановлением оксида хрома углеродом с последующим образованием карбида:
-
В основе процесса лежит реакция:
- Образование карбида Cr 3 C 2 начинается при температуре 1150–1200 °C через образование низших карбидов хрома (Cr 23 C 6 , Cr 7 C 3 ). Повышение температуры до 1500–1600 °C приводит к образованию однофазного карбида Cr 3 C 2 с незначительным содержанием свободного углерода. Обычно процесс получения карбида ведут в среде водорода .
Физические свойства
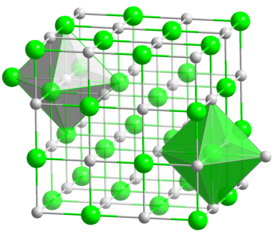
Карбид хрома представляет собой порошок серого цвета. Имеет ромбическую решетку , в которой каждый из 8 атомов углерода расположен в центре трёхгранной призмы, в углах которой находятся атомы хрома. Пространственная группа Pnma , периоды решетки а = 0,5532 нм, b = 0,2829 нм, c = 1,1471 нм. Плавление карбида хрома происходит инконгруэнтно по перитектической реакции .
- Удельное электрическое сопротивление 75 мкОм∙см
- Коэффициент линейного теплового расширения 11,7∙10 -6 1/K (20–1100 °C)
- Микротвёрдость карбида хрома равна 10,4–20,2 ГПа, что связано с анизотропией кристаллической решетки
- Модуль упругости 372 ГПа
Химические свойства
Карбид хрома является стойким соединением по отношению к действию всех минеральных кислот . При действии расплавленной селитры и перекиси натрия окисляется. Кипящая концентрированная хлорная кислота разлагает карбид хрома с выделением ацетилена .
Среди карбидов переходных металлов IV, V, VI групп, карбид хрома является самым стойким при высокотемпературном окислении. Так, окисление карбида хрома в виде порошка начинается при температуре около 700 °C, а в виде компактных образцов окисляется при температуре выше 1000–1100 °C .
Применение
Карбид хрома может входить в состав различных керметов и покрытий, работающих в условиях износа, повышенных температур и в агрессивных средах . Является основным компонентом безвольфрамовых твёрдых сплавов марки КХН (карбид хрома – никель). Близость коэффициента термического расширения Cr 3 C 2 к КТР стали позволяет наносить карбидохромовые покрытия, в которых отсутствуют значительные остаточные напряжения .
Примечания
- ↑ Косолапова Т. Я. . — Металлургия, 1968. — С. .
- Самсонов Г. В. Физическое материаловедение карбидов. — Наукова думка, 1974. — С. 454.
- Самсонов Г. В., Виницкий И. М. Тугоплавкие соединения (справочник). — Металлургия, 1976. — С. 560.
- V. Singh, R. Diaz, K. Balani, A. Agarwal, S. Seal. (недоступная ссылка) // Acta Materialia, 2009. Vol.57. Р.335-344.
- 2020-12-01
- 1