Interested Article - Соли аммония

- 2021-02-01
- 1

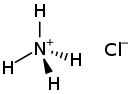
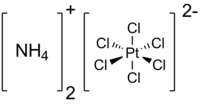
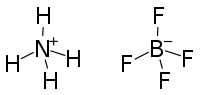
Соли аммония — соли , содержащие аммоний , NH 4 + ; по строению, цвету и другим свойствам похожи на соответствующие соли натрия . Все соли аммония хорошо растворимы в воде, кроме метаванадата аммония NH 4 VO 3 и триметаванадата аммония (NH 4 ) 3 V 3 O 9 и полностью диссоциируют в водном растворе. Соли аммония проявляют общие свойства солей. При действии на них щёлочи выделяется газообразный аммиак . Все соли аммония при нагревании разлагаются.
Применение
- Нитрат аммония (аммиачная селитра) NH 4 NO 3 применяют как азотные удобрения и для изготовления взрывчатых веществ — аммонитов ;
- Сульфат аммония (NH 4 ) 2 SO 4 — как дешёвое азотное удобрение;
- Гидрокарбонат аммония NH 4 HCO 3 и карбонат аммония (NH 4 ) 2 CO 3 — в пищевой промышленности при производстве мучных кондитерских изделий в качестве химического разрыхлителя , при крашении тканей , в производстве витаминов , в медицине;
- Хлорид аммония ( нашатырь ) NH 4 Cl — в гальванических элементах (сухих батареях), при пайке и лужении , в текстильной промышленности, как удобрение , в ветеринарии , в медицине .
Химические свойства солей аммония
- Сильные электролиты, диссоциируют в водных растворах:
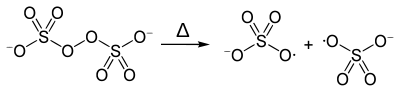
При нагревании разлагаются:
- если кислота летучая
- если анион проявляет окислительные свойства
Вступают в реакции обмена:
- с кислотами :
- c солями :
Соли аммония подвергаются гидролизу (как соль слабого основания и сильной кислоты ):
При нагревании со щелочами выделяют аммиак (качественная реакция на ион аммония):
Получение
Получают соли аммония при взаимодействии аммиака или гидроксида аммония с кислотами:
Реакция аммиака с хлором — качественная реакция на хлор:
Литература
- Глинка Н. Л. Общая химия : [учеб. пособие для вузов] 30-е изд. М.: Интеграл-Пресс, 2003, 727 с.: ил. ISBN 5-89602-017-1
- 2021-02-01
- 1