Interested Article - Реакция Виттига

- 2021-11-07
- 1
Реакция Виттига — химическая реакция альдегидов или кетонов с илидами фосфора (которые иногда называют «реагентами Виттига»), которая приводит к образованию алкенов или алленов и оксида трифенилфосфина .

Реакция была открыта в 1954 году Георгом Виттигом . За открытие этой реакции он был награждён Нобелевской премией в области химии в 1979 году.
Реакции Виттига широко используется в органическом синтезе для получения алкенов .
Реакцию Виттига не следует путать с .
Механизм реакции
Классический механизм
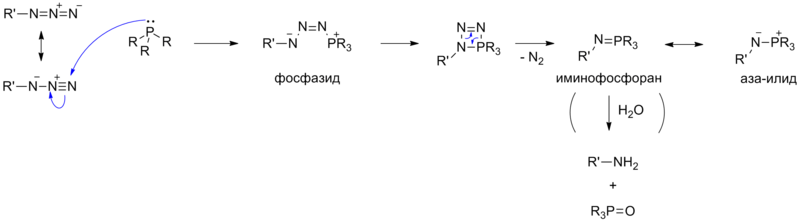
При нуклеофильном присоединении илида 1 к карбонильному соединению образуется бетаин 3 , который вследствие свободного вращения вокруг связи С-С может переходить в конформер 4 . Последний способен быстро и обратимо изомеризоваться, образуя четырехчленный оксафосфетановый цикл (соединение 5) . Элиминирование 6 приводит к образованию Z-изомера целевого алкена 7 .

Изомеризация бетаина 4 в оксафосфетан 5 является лимитирующей стадией реакции. Скорость реакции нуклеофильного присоединения илида к карбонильному соединению сильно зависит от природы илида. В случае незамещенного илида (R 1 = H) присоединение проходит относительно быстро с подавляющим большинством альдегидов и кетонов . Однако в случае «стабилизированных реагентов Виттига» (R 1 = электроноакцепторная группа) скорость нуклеофильного присоединения значительно снижается, что приводит к уменьшению скорости реакции в целом. Также возрастает количество побочного продукта в виде E-изомера алкена. Кроме этого, «стабилизированные реагенты Виттига» практически не взаимодействуют со альдегидами и кетонами.
Стадия элиминирования с образованием продукта протекает из интермедиата, а не устойчивого выделяемого соединения. Этот интермедиат образуется в реакции in situ и самопроизвольно разлагается. Следовательно, реакция Виттига является еще одной реакцией олефинирования, но, в отличие от или , протекает в одну стадию, и поэтому намного более распространена.
Реагенты Виттига
Получение илидов фосфора
Реагенты Виттига обычно получают из соответствующих солей фосфония , которые в свою очередь образуются в результате реакции трифенилфосфина с алкилгалогенидами . Триалкилфосфониевая соль депротонируется сильными основаниями, такими как н-бутиллитий :
[Ph 3 P + CH 2 R]X − + C 4 H 9 Li → Ph 3 P=CHR + LiX + C 4 H 10
См.также
Примечания
- Georg Wittig, Ulrich Schöllkopf. Über Triphenyl-phosphin-methylene als olefinbildende Reagenzien I (нем.) // : magazin. — 1954. — Bd. 87 . — S. 1318 . — doi : .
- Georg Wittig, Werner Haag. Über Triphenyl-phosphin-methylene als olefinbildende Reagenzien II (нем.) // : magazin. — 1955. — Bd. 88 . — S. 1654—1666 . — doi : .
- Maercker, A. Org. React. 1965 , 14 , 270—490. (Review)
- W. Carruthers, Some Modern Methods of Organic Synthesis , Cambridge University Press, Cambridge, UK, 1971, pp81-90. ( ISBN 0-521-31117-9 )
- R. W. Hoffmann. Wittig and His Accomplishments: Still Relevant Beyond His 100th Birthday (англ.) // Angewandte Chemie : journal. — 2001. — Vol. 40 , no. 8 . — P. 1411—1416 . — doi : .
Литература
- Обзорные статьи
- Maryanoff B. E., Reitz A. B. The Wittig olefination reaction and modifications involving phosphoryl-stabilized carbanions. Stereochemistry, mechanism, and selected synthetic aspects (англ.) // Chem. Rev. — 1989. — Vol. 89 , no. 4 . — P. 863—927 . — doi : .
- Byrne P. A., Gilheany D. G. The modern interpretation of the Wittig reaction mechanism (англ.) // Chem. Soc. Rev. — 2013. — Vol. 42 . — P. 6670—6696 . — doi : .
- 2021-11-07
- 1