Interested Article - Оксид хрома(VI)

- 2021-02-01
- 1


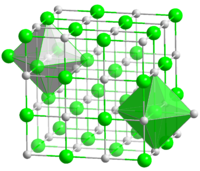
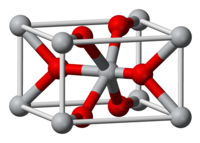
Окси́д хро́ма(VI) (триоксид хрома, трёх окись хрома , хромовый ангидрид ), CrO 3 — соединение хрома с кислородом , тёмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот.
Свойства
Физические свойства
Чёрно- красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен , расплывается на воздухе.
t пл =196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO 3 — кислотный оксид . При его растворении в воде образуется хромовая кислота (при недостатке CrO 3 ):
или дихромовая кислота (при избытке CrO 3 ):
При взаимодействии CrO 3 со щелочами образуются хроматы :
При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода :
Как и все соединения Cr(VI), CrO 3 является сильным окислителем (восстанавливается до Cr 2 O 3 ). Например этанол , ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с предварительно измельченным до состояния порошка оксидом хрома VI (хотя некоторые справочники указывают «растворим в спирте и эфире »). Без тщательного измельчения кристаллов хромового ангидрида добиться воспламенения спиртов и кетонов при контакте с ним невозможно. Окисляет иод , серу , фосфор , уголь , например:
Комплекс триоксида хрома с пиридином используется для окисления спиртов в соответствующие карбонильные соединения ( реакция Саретта ).
Получение
Получают действием H 2 SO 4 на хромат натрия Na 2 CrO4 (реже дихромат калия K 2 Cr 2 O 7 ).
Окислением диоксида хрома или оксида хрома (III) или хрома кислородом в присутствии ультрафиолета :
Применение
Используется для получения хрома электролизом , электролитического хромирования ; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах .
Применяют также, как окислитель в органической химии (в производстве изатина , индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, ди хромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений ( хромовая смесь ).
Токсичность
Оксид хрома(VI) очень ядовит и канцерогенен , как и многие другие соединения шестивалентного хрома . Летальная доза для человека при попадании внутрь 0,08 г/кг.
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. Сам негорюч, но воспламеняет бензин при комнатной температуре и используется в качестве воспламенителя топлива в ракетной технике. При попадании на кожу вызывает сильные раздражения, экземы и дерматиты , а также может спровоцировать развитие рака кожи . Даже при своевременном удалении с кожных покровов оставляет пятна коричневого цвета. Весьма опасно вдыхание паров хромового ангидрида, хотя он и малолетуч.
Для хранения его применяется стеклянная или фарфоровая герметичная посуда, необходимо исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
- 2021-02-01
- 1