Interested Article - Эпихлоргидрин

- 2021-04-23
- 1
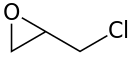
Эпихлоргидрин (хлорметилоксиран) — органическое вещество , хлорпроизводное окиси пропилена, с формулой СH 2 (O)CH-CH 2 Cl. Широко применяется в органическом синтезе, используется в производстве эпоксидных смол и глицерина . Высокотоксичен, ирритант .
Синтез
Эпихлоргидрин получают из пропилена , который хлорируют при температуре 500 °С и давлении 18 атмосфер до аллилхлорида:
Затем аллилхлорид подвергается действию хлорноватистой кислоты и получают изомерные дихлоргидрины глицерина:
Далее на дихлоргидрины глицерина действуют щёлочью ( NaOH ), в результате чего образуется эпихлоргидрин:
Образовавшийся эпихлоргидрин отделяют перегонкой с паром и дистилляцией . Также его можно получить восстановлением хлорированного акролеина .
Физические свойства
Представляет собой бесцветную подвижную прозрачную жидкость с раздражающим запахом хлороформа , плохо растворимую в воде , хорошо в большинстве органических растворителях. С водой образует азеотропную смесь с температурой кипения +88 °С и содержит 75 % эпихлоргидрина. Образует азеотропные смеси с большим числом органических жидкостей. Вследствие наличия асимметричного атома углерода эпихлоргидрин .
Химические свойства
Эпихлоргидрин химически высокореакционное соединение, имеющее активную эпоксидную группу и подвижный атом хлора .
Реакция галогенирования
При взаимодействии хлора с эпихлоргидрином при обычных условиях образуется окись 3,3-дихлорпропилена (3,3-дихлорэпоксипропилен) :
Реакция гидрохлорирования
Легко присоединяет хлороводород при обычной температуре как в растворе, так и в безводной среде, с образованием 1,3-дихлоргидрина :
Реакция дегидрохлорирования
В присутствии небольших количеств щёлочи эпихлоргидрин легко присоединяет соединения содержащие один или несколько подвижных атомов водорода, с образованием хлоргидринов :
При увеличении концентрации щёлочи реакция идет с отщеплением хлористого водорода и с восстановлением эпоксидной группы, но уже в другом положении :
Реакция гидролиза
При избытке щёлочи (чаще всего применяют карбонат натрия ) и при температуре 100 °С эпихлоргидрин медленно превращается в глицерин :
Реакция гидратации
в присутствии разбавленных неорганических кислот ( серной или ортофосфорной ) эпихлоргидрин образует α-монохлоргидрин глицерина :
С повышением температуры повышается гидратация эпихлоргидрина.
Реакция этерификации
При взаимодействии эпихлоргидрина со спиртами происходит раскрытие эпоксидного кольца с образованием гидроксильной группы в положении 2 и с образованием простого эфира :
С карбоновыми кислотами эпихлоргидрин образует сложные эфиры хлоригидрина, например с ледяной уксусной кислотой при нагревании до 180 °С образуется преимущественно 1-хлор-2-гидрокси-3-пропилацетат :
Реакция аминирования
Эпихлоргидрин уже при обычной температуре присоединяет аммиак или амины с раскрытием цикла :
Реакция конденсации
Эпихлоргидрин реагирует с дифенилолпропаном с образованием полимерного диглицидного эфира :
Данная реакция является примером получения эпоксидных смол , получивших за последнее время в силу своих исключительных свойств очень широкое распространение .
Реакция полимеризации
Эпихлоргидрин способен полимеризоваться. В зависимости от применяемого катализатора получаются подвижные жидкости, высоковязкие масла или смолоподобные продукты .
Применение
Применяется как полупродукт для синтеза производных глицерина , красителей и поверхностно-активных веществ ; для получения синтетических материалов (главным образом, эпоксидных смол ).
Токсикология и безопасность
Общий характер действия
Обладает раздражающим и аллергическим действием. В опытах на животных избирательно поражает почки. Проникает через кожу .
Эпихлоргидрин является высокотоксичным и огнеопасным соединением . Пары эпихлоргидрина при вдыхании даже небольших концентраций вызывают тошноту , головокружение и слезотечение , а при длительном воздействии приводят к более тяжёлым последствиям (нередко возникают сильнейшие отёки лёгких ) . Эпихлоргидрин при попадании на кожу и длительном контакте вызывает дерматиты, вплоть до поверхностных некрозов. Все работы с эпихлоргидрином необходимо проводить в резиновых перчатках, резиновом фартуке, а при сильной загазованности его парами — в противогазе марки А .
Безопасность
Эпихлоргидрин — легковоспламеняющееся вещество. При возгорании тушить диоксидом углерода, пеной или водой, равномерно распределяя её по поверхности.
ПДК в воздухе рабочей зоны производственных помещений не должен превышать 1 мг/м³, ПДК в атмосферном воздухе населённых мест 0,2 мг/м³ (рекомендуемая)
.
Примечания
- ↑
- (англ.) : A CRC quick reference handbook — CRC Press , 1993. — ISBN 978-0-8493-4498-5
- ↑ Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей. Изд. 7-е, пер. и доп. В трёх томах. Том I. Органические вещества. Под ред. засл. деят. науки проф. Н. В. Лазарева и докт. мед. наук Э. Н. Левиной. Л., «Химия», 1976. 592 стр., 27 табл., библиография — 1850 названий.
- Григорьев А. П., Федотова О. Я. Лабораторный практикум по технологии пластических масс. В двух частях. Часть 2. Поликонденсационные и химически модифицированные пластические массы. — Учеб. пособие для химико-технол. вузов. - 2-е изд., перераб. и доп.. — М. : Высшая школа, 1977. — Т. 2. — 264 с.
- ↑ Гольдберг М. М., Ермолаева Т. А., Лившиц М. Л., Лубман А. М., Рассудова Н. С., Сергеева 3. И., Фартунин В. И. Сырьё и полупродукты для лакокрасочных материалов / Под ред. М. М. Гольдберга.. — М. : Химия, 1978. — 512 с.
- ↑ Ошин Л.А. Промышленные хлорорганические продукты. — М. : Химия, 1978. — 656 с.
- Брацыхин Е. А., Шульгина Э. С. Технология пластических масс. — Учебное пособие для техникумов. – 3-е изд., перераб. и доп.. — Л. : Химия, 1982. — 328 с.
См. также
- 2021-04-23
- 1





![{\displaystyle {\mathsf {RH+CH_{2}CH{-}O{-}CH_{2}Cl{\xrightarrow[{}]{[NaOH]}}RCH_{2}{-}CHOH{-}CH_{2}Cl}}}](/images/008/286/8286537/13.jpg?rand=146422)
![{\displaystyle {\mathsf {RCH_{2}{-}CHOH{-}CH_{2}Cl{\xrightarrow[{}]{[NaOH]}}RCH_{2}{-}CH{-}O{-}CH_{2}}}}](/images/008/286/8286537/14.jpg?rand=969086)

![{\displaystyle {\mathsf {CH_{2}CH{-}O{-}CH_{2}Cl+H_{2}O{\xrightarrow[{}]{[H_{2}SO_{4}]}}CH_{2}OH{-}CHOH{-}CH_{2}Cl}}}](/images/008/286/8286537/16.jpg?rand=918498)