Interested Article - Бензилхлорид

- 2021-02-01
- 1
Бензилхлорид (хлористый бензил) — бесцветная жидкость с резким запахом, нерастворимая в воде , смешивается с этанолом , хлороформом и другими органическими растворителями. Лакриматор , огнеопасен.
Получение
В промышленности бензилхлорид получают жидкофазным радикальным хлорированием толуола :
Таким способом получают около 100,000 тонн бензилхлорида в год . Побочными продуктами являются и бензотрихлорид ( и ).
Существует несколько вариантов процесса: хлорирование толуола в присутствии 1 % PCI 3 при 90—100 °C, хлорирование при УФ-облучении или в присутствии 2,2'-азо-бис-изобутиронитрила.
Бензилхлорид также может быть получен хлорированием толуола
сульфурилхлоридом
SO
2
Cl
2
,
бензола:
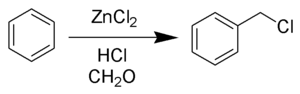
В лаборатории получают реакцией бензилового спирта с концентрированной соляной кислотой , или прямым хлорированием сухого толуола в газовой фазе сухим хлором при облучении, в качестве облучения удобнее всего использовать энергосберегающее диодное ультрафиолетовое освещение, даже не яркий источник ультрафиолетового света приводит к разрыву связи молекулы Cl2, или потребуется мощная лампа накаливания ~500Вт.
Применение и реакции
- Бензилхлорид применяют для получения бензилового спирта и особенно бензилцеллюлозы (см. Целлюлоза ), широко используемой в производстве пластмасс , плёнок, электроизоляционных покрытий и лаков.
- В промышленности бензилхлорид играет роль прекурсора к бензиловым эфирам, которые используются как пластификаторы , ароматизаторы и парфюмерия .
- Фенилуксусную кислоту , прекурсор к фармацевтическим препаратам , получают через бензилцианид , который образуется при обработке бензилхлорида цианидом натрия .
- Четвертичные аммониевые соли, используемые в качестве поверхностно-активных веществ , легко образуются алкилированием третичного амина бензилхлоридом:
- В органическом синтезе, бензилхлорид используется для введения бензильной защитной группы , получая соответствующий бензиловый эфир. Снимается данная группа гидрированием на палладии .
- С карбоновыми кислотами, даёт соответствующие бензильные сложные эфиры .
- Бензойная кислота (C 6 H 5 COOH) может быть получена окислением бензилхлорида щелочным раствором перманганата калия (KMnO 4 ).
- Он может быть использован в синтезе наркотиков класса амфетаминов, и по этим причинам продажи бензилхлорида находятся под мониторингом в США
- Бензилхлорид также легко реагирует с металлическим магнием давая реактив Гриньяра . Он предпочтительнее чем бензил бромид для получения реагента Гриньяра, так как бромид даёт в качестве продукта также продукт сочетания по Вюрцу — 1,2-дифенилэтан.
Бензилирование гетероатомных функциональных групп
Бензилхлорид — удобный бензилирующий агент для гетероатомных функциональных групп и наиболее часто используется для введения этой защитной группы . Бензилирование спиртов этим реагентом достигается в условиях катализа сильным основанием таким как KOH , и в спиртовых растворителях и в условиях фазового переноса с n-Bu 4 NHSO 4 Оксид серебра в ДМФА также эффективен Фенолы могут также быть бензилированы в условиях основного катализа .
Амино группы легко бензилируются при обработке бензилхлоридом в присутствии карбоната или гидроксида при этом дибензилирование является конкурентной реакцией . Тиолы бензилируются в присутствии гидроксида натрия или цезия карбоната и полярных растворителях, таких как этанол или ДМФА .
Амиды могут быть N-бензилированы бензилхлоридом при действии сильных оснований таких как метал гидриды 11
Бензилирование метиленактивных соединений
Анионы и дианионы β-кетоэфиров, , замещённые малоновые эфиры , β-кетоальдегиды, β-дикетоны, β-кетоамиды, и β-кетонитрилы все эффективно реагируют давая С-бензилированные продукты. Когда генерируется дианион из β-кетоамида, β-кетоэфир или β-дикетоне бензилируется менее кислотное положение. Нитрил стабилизированные карбанионы легко бензилируются в эфирных растворителях, аммиаке или ДМСО Бензилхлорид также реагирует с карбанионами генерированными из кетонов, эфиров , иминов (металлоенаминов) и гидразонов , оксимов .
Безопасность
Бензилхлорид является алкилирующим агентом. Он реагирует с водой, гидролизуясь до бензилового спирта и хлороводорода . Так как бензилхлорид достаточно летуч при комнатной температуре и раздражает слизистые оболочки глаз и кожу, является лакриматором .
Работу с ним ведут в вытяжном шкафу и с соответствующей защитой кожи. Бензилхлорид является мутагеном и, возможно, канцерогеном .
Ссылки
- ↑
- Furniss, B. S.; Hannaford, A. J.; Smith, P. W. G.; Tatchell, A. R. (1989), Vogel’s Textbook of Practical Organic Chemistry (5th ed.), Harlow: Longman, p. 864, ISBN 0-582-46236-3
- Shaw, J. E.; Kunerth, D. C.; Sherry, J. J. Tetrahedron Lett. 1973, 689.
- (a) Greene, T. W.; Wuts, P. G. M., Protective Groups in Organic Synthesis, 2nd ed.; Wiley: New York, 1991. (b) Protective Groups in Organic Chemistry, McOmie, J. F. W., Ed.; Plenum: New York, 1973.
- Fletcher, H. G., Methods Carbohydr. Chem. 1963, 166.
- Freedman, H. H.; Dubois, R. A. Tetrahedron Lett. 1975, 3251.
- Kuhn, R.; Löw, I.; Trischmann, H. Chem. Ber. 1957, 90, 203.
- Heer, J.; Billeter, J. R.; Miescher, K. Helv. Chim. Acta 1945, 28, 991
- Yamashita, M.; Takegami, Y. Synthesis 1977, 803.
- Velluz, L.; Amiard, G.; Heymès, R. Bull. Soc. Chim. Fr., Part 2 1954, 1012.
- (a) Frankel, M.; Gertner, D.; Jacobson, H.; Zilkha, A. J. Chem. Soc. 1960, 1390. (b) Vogtle, F.; Klieser, B. S 1982, 294.
- (a) Xia, Y.; Kozikowski, A. P. J. Am. Chem. Soc. 1989, 111, 4116. (b) Bryant, D. R.; Work, S. D.; Hauser, C. R. J. Org. Chem. 1964, 29, 235.
- (a) Elsinger, F. OS 1973, 5, 76. (b) Stork, G.; McElvain, S. M. J. Am. Chem. Soc. 1946, 68, 1053
- Cope, A. C.; Holmes, H. L.; House, H. O. Org. React. 1957, 9, 107.
- Ravikumar, V. T.; Sathyamoorthi, G.; Thangaraj, K.; Rajagopalan, K. Indian J. Chem., Sect. B 1985, 24, 959
- Hauser, C. R.; Harris, T. M. J. Am. Chem. Soc. 1958, 80, 6360.
- Hubbard, J. S.; Harris, T. M. Tetrahedron Lett. 1978, 4601.
- Baraldi, P. G.; Pollini, G. P.; Zanirato, V. Synthesis 1985, 969.
- Arseniyadis, S.; Kyler, K. S.; Watt, D. S. Org. React. 1984, 31, 1.
- Bates, G. S.; Ramaswamy, S. Can. J. Chem. 1980, 58, 716.
- Muller-Uri, C.; Singer, E. A.; Fleischacker, W. J. Med. Chem. 1986, 29, 125
- (a) Stork, G.; Dowd, S. R. J. Am. Chem. Soc. 1963, 85, 2178. (b) Hosomi, A.; Araki, Y.; Sakurai, H. J. Am. Chem. Soc. 1982, 104, 2081
- Henoch, F. E.; Hampton, K. G.; Hauser, C. R. J. Am. Chem. Soc. 1969, 91, 676.
- 2021-02-01
- 1




![{\displaystyle {\ce {C6H5CH2Cl ->[NaCN] C6H5CH2CN ->[H2O] C6H5CH2COOH}}}](/images/008/286/8286545/9.jpg?rand=776731)
![{\displaystyle {\ce {R3N + C6H5CH2Cl -> [R3N(C6H5CH2)]^+Cl^-}}}](/images/008/286/8286545/10.jpg?rand=56550)
![{\displaystyle {\ce {C6H5CH2Cl ->[ROH] C6H5CH2OR ->[Pd][H2] ROH + C6H5CH3}}}](/images/008/286/8286545/11.jpg?rand=668465)
![{\displaystyle {\ce {C6H5CH2Cl ->[KMnO4][OH^-] C6H5COOH}}}](/images/008/286/8286545/12.jpg?rand=382143)