Interested Article - Трифторуксусная кислота

- 2021-11-09
- 1
Трифтору́ксусная кислота́ (трифторэтановая кислота, ТФУК) — фторорганическая карбоновая кислота , органическое вещество. По внешнему виду представляет собой бесцветную дымящую жидкость с резким специфическим запахом (отдалённо напоминающим запах уксусной кислоты ).
Смешивается во всех отношениях с водой , этанолом , ацетоном , диэтиловым эфиром . С водой образует азеотроп (20,6 масс. % воды, 79,4 масс. % кислоты) (т. кип. 105,46 °C). В жидком виде и в парах вызывает сильные ожоги кожных покровов и слизистых оболочек. ПДК в воздухе рабочей зоны 2 мг/м 3 .
Получение
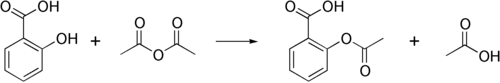
В промышленности трифторуксусную кислоту получают электрохимическим фторированием уксусного ангидрида или фторангидрида в безводном HF . В лаборатории чаще используют кислотный гидролиз 1,1,1-трифтор-2,2,2-трихлорэтана или окисление 2,2,2-трифторэтанола.
Химические свойства
Типичная сильная карбоновая одноосновная кислота. Разрушает металлы, пробку, резину, бакелит , полиэтилен . Не действует на фторопласт и сухое стекло. Термически стабильна, не разлагается при нагревании до 400 °С.
С диалкиловыми эфирами , кетонами , карбоновыми кислотами и другими электронодонорными соединениями даёт прочные комплексы.
Легко присоединяется по кратным связям алкенов , циклоалкенов , ацетиленов с образованием трифторацетатов. С галогенами даёт малоустойчивые гипогалогениты, которые селективно галогенируют различные соединения. Реакция с многоатомными спиртами (например, с триолами) приводит к полициклическим ортоэфирам .

При действии оксида фосфора(V) на трифторуксусную кислоту образуется ангидрид трифторуксусной кислоты ((CF 3 CO) 2 O) — сильный ацилирующий агент. Реакция трифторуксусной кислоты со спиртами даёт эфиры , с аминами — амиды , с карбоновыми кислотами - смешанные ангидриды. Последние, а также (CF 3 CO) 2 O в присутствии минеральных кислот или сульфокислот используют в качестве промоторов при ацилировании спиртов, фенолов, тиолов
Трифторуксусная кислота легко присоединяется по кратным связям алкенов, циклоалкенов, ацетиленов с образованием трифторацетатов; с галогенами даёт малоустойчивые гипогалогениты CF 3 COOHal, которые селективно галогенируют различные. соединения.
При нагревании серебряной соли трифторуксусной кислоты с избытком I 2 образуется трифторметилиодид;
При восстановлении трифторуксусной кислоты и её эфиров LiAlH 4 при О °C - трифторацетальдегид CF 3 CHO, а при избытке восстановителя при 30 °C - 2,2,2-трифторэтанол.

Трифторуксусная кислота - сырьё в органическом синтезе, катализатор в реакциях этерификации и полимеризации, растворитель для ряда термостойких полимеров. Трифторацетангидрид применяют в производстве ацетатного шёлка (США, Великобритания), фармацевтических препаратов, пестицидов, в качестве реагента для защиты функциональных групп в синтезе пептидов.
Физико-химические свойства
ТФУК смешивается с водой в любых соотношениях. Регенерировать "сухую" ТФУК можно ректификацией с осушителем (Серная кислота, Ангидридом или оксидом фосфора) или вымораживанием.

Примечания
- ↑ (англ.) / — 95 — Boca Raton: CRC Press , 2014. — P. 6—182. — ISBN 978-1-4822-0868-9
- ↑ (англ.) / — 95 — Boca Raton: CRC Press , 2014. — P. 6—231. — ISBN 978-1-4822-0868-9
- ↑ (англ.) / — 95 — Boca Raton: CRC Press , 2014. — P. 6—95. — ISBN 978-1-4822-0868-9
- (англ.) / — 95 — Boca Raton: CRC Press , 2014. — P. 15—21. — ISBN 978-1-4822-0868-9
- (англ.) / — 95 — Boca Raton: CRC Press , 2014. — P. 9—59. — ISBN 978-1-4822-0868-9
- Dietrich Mootz, Dagmar Boenigk. . Kristallstrukturen von Säurehydraten und Oxoniumsalzen, XXII [2]. Hydratbildung der Trifluoressigsäure sowie Strukturen eines Monohydrats und eines Tetrahydrats [3]. / Fluorides and Fluoro Acids, VII [1] Crystal Structures of Acid Hydrates and Oxonium Salts, XXII [2]. Hydrate Formation of Trifluoroacetic Acid and Structures of a Monohydrate and a Tetrahydrate [3]] (англ.) // Zeitschrift für Naturforschung B. — 1984-03-01. — Vol. 39 , iss. 3 . — P. 298–304 . — ISSN . — doi : . 4 января 2023 года.
- Howard H. Cady, George H. Cady. (англ.) // Journal of the American Chemical Society. — 1954-02. — Vol. 76 , iss. 3 . — P. 915–916 . — ISSN . — doi : . 4 января 2023 года.
- Zhixian Huang, Ling Li, Miaomiao Zhou, Haiming Jiang, Ting Qiu. (англ.) // Fluid Phase Equilibria. — 2016-01-25. — Vol. 408 . — P. 88–93 . — ISSN . — doi : .
Литература
- «Химическая энциклопедия». — Т.5. — М.: Советская энциклопедия, 1999. — С. 9
- Альберт А., Сержент Е. «Константы ионизации кислот и оснований». — М.-Л.: Химия, 1964. — С. 118
- Гудлицкий М. «Химия органических соединений фтора». — М.: ГНТИХЛ, 1961. — С. 270
- Некрасов Б. В. «Основы общей химии». — Т.1. — М.: Химия, 1973. — С. 563—564
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник». — Л.: Химия, 1977. — С. 184
- Промышленные фторорганические продукты. Справочник, Л., 1990, с. 367-71. И. И. Крылов.
- Физер Л., Физер M., Реагенты для органического синтеза, пер. с англ., т. 3, M., 1970;
- Исикаве H., Кобаяси Ё., Фтор. Химия и применение, пер. с япон., M., 1982;
- 2021-11-09
- 1