Interested Article - Селенистая кислота

- 2021-04-04
- 1
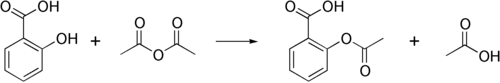
Селе́нистая кислота́ — неорганическое химическое соединение селена , кислота . Химическая формула H 2 SeO 3 .
Является аналогом сернистой и теллуристой кислот.
Селенистая кислота — одна из двух основных оксикислот селена (вторая из них — селеновая кислота H 2 SeO 4 )
Токсична.
Физические свойства
Белые ромбические кристаллы. Очень гигроскопична . Хорошо растворима в воде и этаноле . При растворении происходит сильное поглощение тепла [ источник не указан 2150 дней ] . Неустойчивая кислота, при нагревании выше 70 °C распадается на воду и диоксид селена SeO 2 .
Химические свойства
- Слабая кислота. Образует два ряда солей — кислые и средние соли — и селениты в результате реакций нейтрализации щелочей (и кислые, и средние), или сплавления с оксидами металлов (средние).
-
Является окислителем средней силы, проявляет окислительно-восстановительную двойственность:
- реагирует с концентрированным растворами галогеноводородных кислот (кроме фтороводородной), окисляя их до галогенов. В результате этой реакции элементарный селен выпадает в осадок;
- может быть окислена сильными окислителями ( хлор и бром в щелочной среде, озон в сильнокислой среде, пероксид водорода ) до селеновой кислоты.
- В результате электролиза водного раствора на катоде выделяется водород, а на аноде — селеновая кислота.
Получение
Селенистую кислоту получают из оксида селена(IV) SeO 2 , растворяемого в воде, либо окислением селена разбавленной азотной кислотой .
Применение
Селенистую кислоту обычно применяют для травления металлов, например меди или магния , для оксидирования стали в процессе холодного воронения стали , в основном деталей огнестрельного оружия .
Применяется для получения глиоксаля окислением ацетальдегида .
Основной компонент в реактиве на некоторые наркотические вещества .
Также из селенистой кислоты окислением либо электролизом получают селеновую кислоту H 2 SeO 4 .
Токсичность
Селенистая кислота, как и другие соединения селена H 2 SeO 3 , в больших дозах токсична для человека. При попадании на кожу вызывает раздражение и химические ожоги .
См. также
Примечания
- . National Institute of Justice (1 июля 2000). Дата обращения: 26 января 2012. 1 апреля 2010 года.
Ссылки
|
|
Это
заготовка статьи
о
неорганическом веществе
. Помогите Википедии, дополнив её.
|
- 2021-04-04
- 1