Алканы
- 1 year ago
- 0
- 0


|

|
|
Химическая структура
(вверху)
и 3D-модель
(внизу)
метана
— простейшего алкана
|
Алка́ны ( парафи́ны , также насы́щенные или преде́льные углеводоро́ды ) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые (одинарные) связи и образующие гомологический ряд с общей формулой C n H 2n+2 .
Все алканы и алкены относятся к классу алифатических углеводородов. Алканы являются насыщенными углеводородами, то есть содержат максимально возможное число атомов водорода для заданного числа атомов углерода. Каждый атом углерода в молекулах алканов находится в состоянии sp 3 -гибридизации — все 4 гибридные орбитали атома С идентичны по форме и энергии, 4 связи направлены в вершины тетраэдра под углами 109°28'. Связи C—C представляют собой σ-связи , отличающиеся низкой полярностью и поляризуемостью . Длина связи C—C составляет 0,154 нм , длина связи C—H — 0,1087 нм .
Простейшим представителем класса является метан (CH 4 ). Углеводород с самой длинной цепью — нонаконтатриктан C 390 H 782 синтезировали в 1985 году английские химики И. Бидд и М. К. Уайтинг .
Выбирается один из атомов углеродной цепи, он считается замещённым метаном, и относительно него строится название «алкил1алкил2алкил3алкил4метан», например:
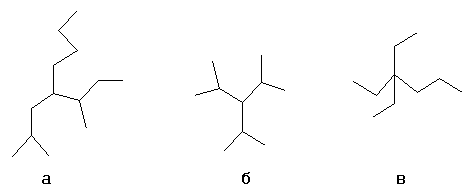
По номенклатуре ИЮПАК названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. Выбирается наиболее длинная неразветвлённая углеводородная цепь, при этом нумерация этой цепи начинается со стороны ближайшего к концу цепи заместителя. В названии соединения цифрой указывают номер углеродного атома, при котором находится замещающая группа или гетероатом , затем название группы или гетероатома и название главной цепи. Если группы повторяются, то перечисляют цифры, указывающие их положение, а число одинаковых групп указывают приставками ди-, три-, тетра-. Если группы неодинаковые, то их названия перечисляются в алфавитном порядке.
Например:
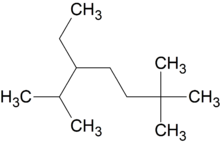
При сравнении положений заместителей в обеих комбинациях, предпочтение отдается той, в которой первая отличающаяся цифра является наименьшей. Таким образом, правильное название — 2, 2 ,6-триметил-5-этилгептан .
Алканы образуют гомологический ряд .
| Гомологический ряд алканов (первые 10 членов) | ||
|---|---|---|
| Метан | CH 4 | CH 4 |
| Этан | CH 3 —CH 3 | C 2 H 6 |
| Пропан | CH 3 —CH 2 —CH 3 | C 3 H 8 |
| Бутан | CH 3 —CH 2 —CH 2 —CH 3 | C 4 H 10 |
| Пентан | CH 3 —CH 2 —CH 2 —CH 2 —CH 3 | C 5 H 12 |
| Гексан | CH 3 —CH 2 —CH 2 —CH 2 —CH 2 —CH 3 | C 6 H 14 |
| Гептан | CH 3 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 3 | C 7 H 16 |
| Октан | CH 3 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 3 | C 8 H 18 |
| Нонан | CH 3 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 3 | C 9 H 20 |
| Декан | CH 3 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 2 —CH 3 | C 10 H 22 |
Алканы, число атомов углерода в которых больше трёх, имеют изомеры. Изомерия предельных углеводородов обусловлена простейшим видом структурной изомерии — изомерией углеродного скелета, а начиная с C 7 H 16 — также оптической изомерией . Число структурных изомеров алканов C n H 2n+2 в зависимости от числа атомов углерода n без учёта стереоизомерии и с учётом стереоизомерии :
| n | Число изомеров | С учётом стереоизомерии |
|---|---|---|
| 4 | 2 | 2 |
| 5 | 3 | 3 |
| 6 | 5 | 5 |
| 7 | 9 | 11 |
| 8 | 18 | 24 |
| 9 | 35 | 55 |
| 10 | 136 | |
| 11 | 159 | 345 |
| 12 | 355 | 900 |
| 13 | 802 | 2412 |
| 14 | 1858 | 6563 |
| 15 | 4347 | 18 127 |
| 20 | 366 319 | 3 396 844 |
| 25 | 36 797 588 | 749 329 719 |
| 30 | 4 111 846 763 | 182 896 187 256 |
Число структурных изомеров низших углеводородов до C 14 H 30 было установлено прямым подсчётом; в 1931 году был разработан рекурсивный метод подсчёта числа изомеров . Какой-либо простой связи между числом атомов углерода n и числом изомеров обнаружено не было . При число различных структурных изомеров алканов можно оценить посредством теоремы Редфилда — Пойи .
[ источник не указан 1184 дня ]
| n | Название | Т пл , °C | Т кип , °C | Плотность , г/см 3 | Показатель преломления |
|---|---|---|---|---|---|
| 1 | Метан | −182,48 | −161,5 | 0,416 при T кип | |
| 2 | Этан | −183,3 | −88,63 | 0,546 при T кип | |
| 3 | Пропан | −187,7 | −42,1 | 0,585 при T кип | |
| 4 | Бутан | −138,35 | −0,5 | 0,6 при T кип | 1,3326 |
| Изобутан | −159,60 | −11,73 | 0,5510 при T кип | ||
| 5 | Пентан | −129,7 | 36,07 | 0,6262 | 1,3575 |
| 6 | Гексан | −95,3 | 68,7 | 0,6594 | 1,3749 |
| 7 | Гептан | −90,6 | 98,4 | 0,6795 | 1,3876 |
| 8 | Октан | −55,8 | 125,7 | 0,7025 | 1,3974 |
| 9 | Нонан | −54 | 150,8 | 0,718 | 1,4054 |
| 10 | Декан | −29,7 | 174,1 | 0,730 | 1,4119 |
| 11 | Ундекан | −25,6 | 195,9 | 0,7402 | 1,4151 |
| 12 | Додекан | −9,6 | 216,3 | 0,7487 | 1.4216 |
| 13 | Тридекан | −5,4 | 235,5 | 0,7564 | 1,4256 |
| 14 | Тетрадекан | 5,9 | 253,6 | 0,7628 | 1,4289 |
| 15 | Пентадекан | 9,9 | 270,6 | 0,7685 | 1,4310 |
| 16 | Гексадекан | 18,2 | 286,8 | 0,7734 | 1,4345 |
| 17 | Гептадекан | 22,0 | 301,9 | 0,778* | 1,4369* |
| 18 | Октадекан | 28,2 | 316,1 | 0,7819* | 1,4390* |
| 19 | Нонадекан | 32,1 | 329,76 | 0,7855* | 1,4409* |
| 20 | Эйкозан | 36,8 | 342,7 | 0,7887* | 1,4426* |
| 21 | Генэйкозан | 40,5 | 355,1 | 0,7917* | 1,4441* |
| 22 | Докозан | 44,4 | 367,0 | 0,7944* | 1,4455* |
| 23 | Трикозан | 47,6 | 380,2 | 0,7969* | 1,4468* |
| 24 | Тетракозан | 50,9 | 389,2 | 0,7991* | 1,4480* |
| 25 | Пентакозан | 53,7 | 401,0 | 0,8012* | 1,4491* |
| 26 | 57 | 262 (15 мм рт. ст.) | 0,778 | ||
| 27 | 60 | 270 (15 мм рт. ст.) | 0,780 | ||
| 28 | 61,1 | 280 (15 мм рт. ст.) | 0,807 | ||
| 29 | 64 | 286 (15 мм рт. ст.) | 0,808 | ||
| 30 | 65,8 | 446,4 | 0,897* | 1,4536* | |
| 31 | Гентриаконтан | 67,9 | 455 | 0,8111* | 1,4543* |
| 32 | 69,7 | 463 | 0,8124* | 1,4550* | |
| 33 | 71 | 474 | 0,811 | ||
| 34 | 73,1 | 478 | 0,8148* | 1,4563* | |
| 35 | 74,7 | 486 | 0,8159* | 1,4568* | |
| 36 | 75 | 265 при 130 Па | 0,814 | ||
| 37 | 77,4 | 504,14 | 0,815 | ||
| 38 | 79 | 510,93 | 0,816 | ||
| 39 | 78 | 517,51 | 0,817 | ||
| 40 | 81,4 | 523,88 | 0,817 | ||
| 41 | 80,7 | 530,75 | 0,818 | ||
| 42 | 82,9 | 536,07 | 0,819 | ||
| 43 | 85,3 | 541,91 | 0,820 | ||
| 44 | 86,4 | 547,57 | 0,820 | ||
| 45 | 553,1 | 0,821 | |||
| 46 | 558,42 | 0,822 | |||
| 47 | 563,6 | 0,822 | |||
| 48 | 568,68 | 0,823 | |||
| 49 | 573,6 | 0,823 | |||
| 50 | 93 | 421 | 0,824 | ||
| 51 | 583 | 0,824 | |||
| 52 | 94 | 587,6 | 0,825 | ||
| 53 | 592 | 0,825 | |||
| 54 | 95 | 596,38 | 0,826 | ||
| … | … | … | … | … | … |
| 60 | 98,9 | ||||
| … | … | … | … | … | … |
| 70 | 105,3 | ||||
| … | … | … | … | … | … |
| 100 | Гектан | 115,2 | |||
| … | … | … | … | … | … |
| 150 | 123 | ||||
| … | … | … | … | … | … |
| 390 | Нонаконтатриктан | 132 |
Примечание к таблице: * отмечены значения, полученные для переохлаждённой жидкости.
В ИК-спектрах алканов четко проявляются частоты валентных колебаний связи С—Н в области 2850—3000 см −1 . Частоты валентных колебаний связи С—С переменны и часто малоинтенсивны. Характеристические деформационные колебания в связи С—Н в метильной и метиленовой группах обычно лежат в интервале 1400—1470 см −1 , однако метильная группа даёт в спектрах слабую полосу при 1380 см −1 .
Чистые алканы не поглощают излучение в ультрафиолетовой области выше 2000 Å и по этой причине часто оказываются отличными растворителями для измерения УФ-спектров других соединений.
Алканы имеют низкую химическую активность. Это объясняется тем, что одинарные связи C—H и C—C относительно прочны, и их сложно разрушить. Поскольку связи С—C неполярны, а связи С—Н малополярны, оба вида связей малополяризуемы и относятся к σ-виду, их разрыв наиболее вероятен по гомолитическому механизму, то есть с образованием радикалов.
Галогенирование алканов протекает по радикальному механизму. Для инициирования реакции необходимо смесь алкана и галогена облучить УФ-излучением или нагреть.
Хлорирование метана не останавливается на стадии получения метилхлорида (если взяты эквимолярные количества хлора и метана), а приводит к образованию всех возможных продуктов замещения, от хлорметана до тетрахлорметана . Хлорирование других алканов приводит к смеси продуктов замещения водорода у разных атомов углерода. Соотношение продуктов хлорирования зависит от температуры. Скорость хлорирования первичных, вторичных и третичных атомов зависит от температуры, при низкой температуре скорость убывает в ряду: третичный, вторичный, первичный. При повышении температуры разница между скоростями уменьшается до тех пор, пока не становится одинаковой. Кроме кинетического фактора на распределение продуктов хлорирования оказывает влияние статистический фактор: вероятность атаки хлором третичного атома углерода в 3 раза меньше, чем первичного, и в 2 раза меньше, чем вторичного. Таким образом, хлорирование алканов является нестереоселективной реакцией, исключая случаи, когда возможен только один продукт монохлорирования.
Галогенирование происходит тем легче, чем длиннее углеродная цепь н -алкана. В этом же направлении уменьшается энергия ионизации молекулы вещества, то есть, алкан легче становится донором электрона .
Галогенирование — это одна из реакций замещения . В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атомы галогенируются в последнюю очередь). Галогенирование алканов проходит поэтапно с последовательным образованием хлорметана , дихлорметана , хлороформа и тетрахлорметана : за один этап замещается не более одного атома водорода:
Под действием света молекула хлора распадается на радикалы, затем они атакуют молекулы алкана, отрывая у них атом водорода, в результате этого образуются метильные радикалы ·СН 3 , которые сталкиваются с молекулами хлора, разрушая их и образуя новые радикалы.
Цепной механизм галогенирования:
1) Инициирование
2) Рост цепи
3) Обрыв цепи
Бромирование алканов отличается от хлорирования более высокой стереоселективностью из-за большей разницы в скоростях бромирования третичных, вторичных и первичных атомов углерода при низких температурах.
Иодирование алканов иодом не происходит, получение иодидов прямым иодированием осуществить нельзя.
С фтором и хлором реакция может протекать со взрывом, в таких случаях галоген разбавляют азотом или подходящим растворителем.
При одновременном действии на алканы оксидом серы (IV) и кислородом, при ультрафиолетовом облучении или при участии веществ, являющихся донорами свободных радикалов (диазометан, органические перекиси), протекает реакция сульфирования с образованием алкилсульфокислот :
 При облучении ультрафиолетовым излучением алканы реагируют со смесью
SO 2
и Cl
2
, После того, как с уходом хлороводорода образуется алкильный радикал, присоединяется диоксид серы. Образовавшийся сложный радикал стабилизируется захватом атома хлора с разрушением очередной молекулы последнего.
При облучении ультрафиолетовым излучением алканы реагируют со смесью
SO 2
и Cl
2
, После того, как с уходом хлороводорода образуется алкильный радикал, присоединяется диоксид серы. Образовавшийся сложный радикал стабилизируется захватом атома хлора с разрушением очередной молекулы последнего.
Развитие цепного процесса:
Легче всего сульфохлорируются углеводороды линейного строения, в отличие от реакций хлорирования и нитрования.
Образовавшиеся сульфонилхлориды широко применяются в производстве ПАВ .
Алканы реагируют с 10 % раствором азотной кислоты или оксидом азота NO 2 в газовой фазе при температуре 140 °C и небольшом давлении с образованием нитропроизводных:
Имеющиеся данные указывают на свободнорадикальный механизм. В результате реакции образуются смеси продуктов.
Окисление алканов в жидкой фазе протекает по свободно-радикальному механизму и приводит к образованию гидропероксидов , продуктов их разложения и взаимодействия с исходным алканом. Схема основной реакции автоокисления:
Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения . Пример:
Значение Q достигает 46 000 — 50 000 кДж/кг .
В случае нехватки кислорода вместо углекислого газа получается оксид углерода(II) или уголь (в зависимости от концентрации кислорода).
В реакциях каталитического окисления алканов могут образовываться спирты , альдегиды , карбоновые кислоты .
При мягком окислении СН 4 в присутствии катализатора кислородом при 200 °C могут образоваться:
Окисление также может осуществляться воздухом. Процесс проводится в жидкой или газообразной фазе. В промышленности так получают высшие жирные спирты и соответствующие кислоты .
Реакция окисления алканов :
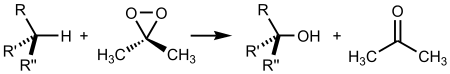
Механизм реакций получения кислот путём каталитического окисления и расщепления алканов показан ниже на примере получения из бутана уксусной кислоты :

Реакции разложения происходят лишь под влиянием больших температур. Повышение температуры приводит к разрыву углеродной связи и образованию свободных радикалов .
Примеры:
При нагревании выше 500 °C алканы подвергаются пиролитическому разложению с образованием сложной смеси продуктов, состав и соотношение которых зависят от температуры и времени реакции. При пиролизе происходит расщепление углерод-углеродных связей с образованием алкильных радикалов.
В 1930—1950 гг. пиролиз высших алканов использовался в промышленности для получения сложной смеси алканов и алкенов, содержащих от пяти до десяти атомов углерода. Он получил название «термический крекинг». С помощью термического крекинга удавалось увеличить количество бензиновой фракции за счёт расщепления алканов, содержащихся в керосиновой фракции (10—15 атомов углерода в углеродном скелете) и фракции солярового масла (12—20 атомов углерода). Однако октановое число бензина, полученного при термическом крекинге, не превышает 65, что не удовлетворяет требованиям условий эксплуатации современных двигателей внутреннего сгорания.
В настоящее время термический крекинг полностью вытеснен в промышленности каталитическим крекингом, который проводят в газовой фазе при более низких температурах — 400—450 °C и низком давлении — 10—15 атм на алюмосиликатном катализаторе, который непрерывно регенерируется сжиганием образующегося на нём кокса в токе воздуха. При каталитическом крекинге в полученном бензине резко возрастает содержание алканов с разветвлённой структурой.
Для метана:
Во время крекинга одна из связей (С-С) разрывается, образуя два радикала. Далее одновременно происходят три процесса, вследствие которых реакция дает множество различных продуктов:
1) Рекомбинация:
2) Диспропорционирование:
3) β-распад (разрыв связи (C-H)):
1) В углеродном скелете 2 (этан) или 3 (пропан) атома углерода — получение (терминальных) алкенов, так как других в данном случае не может получиться; выделение водорода:
Условия протекания: 400—600 °C, катализаторы — Pt, Ni, Al 2 O 3 , Cr 2 O 3 , например, образование этилена из этана:
2) В углеродном скелете 4 (бутан, изобутан) или 5 (пентан, 2-метилбутан, неопентан ) атомов углерода — получение алкадиенов, например, бутадиена-1,3 и бутадиена-1,2 из бутана:
3) В углеродном скелете 6 (гексан) и более атомов углерода — получение бензола и его производных:
В присутствии никелевого катализатора протекает реакция:
Продукт этой реакции (смесь CO и H 2 ) называется « синтез-газом ».
Изомеризация:
Под действием катализатора (например, AlCl
3
) происходит изомеризация алкана: например, бутан (C
4
H
10
), взаимодействуя с хлоридом алюминия (AlCl
3
), превращается из
н
-бутана в 2-метилпропан.
С марганцевокислым калием (KMnO 4 ) и бромной водой (раствор Br 2 в воде) алканы не взаимодействуют.
В небольших количествах алканы содержатся в атмосфере внешних газовых планет Солнечной системы: на Юпитере — 0,1 % метана , 0,0002 % этана , на Сатурне метана 0,2 %, а этана — 0,0005 %, метана и этана на Уране — соответственно 1,99 % и 0,00025 %, на Нептуне же — 1,5 % и 1,5⋅10 −10 , соответственно . На спутнике Сатурна Титане метан (1,6 %) содержится в жидком виде, причём, подобно воде, находящейся на Земле в круговороте , на Титане существуют (полярные) озёра метана (в смеси с этаном) и метановые дожди. К тому же, как предполагается, метан поступает в атмосферу Титана в результате деятельности вулкана . Кроме того, метан найден в хвосте кометы Хиякутаке и в метеоритах ( углистых хондритах ). Предполагается также, что метановые и этановые кометные льды образовались в межзвёздном пространстве .

В земной атмосфере метан присутствует в очень небольших количествах (около 0,0001 %), он производится некоторыми археями (архебактериями) , в частности, находящимися в кишечном тракте крупного рогатого скота . Промышленное значение имеют месторождения низших алканов в форме природного газа , нефти и, вероятно, в будущем — газовых гидратов (найдены в областях вечной мерзлоты и под океанами). Также метан содержится в биогазе .
Высшие алканы содержатся в кутикуле растений , предохраняя их от высыхания, паразитных грибков и мелких растительноядных организмов. Это обыкновенно цепи с нечётным числом атомов углерода , образующиеся при декарбоксилировании жирных кислот с чётным количеством углеродных атомов. У животных алканы встречаются в качестве феромонов у насекомых , в частности у мухи цеце (2-метилгептадекан C 18 H 38 , 17,21-диметилгептатриаконтан C 39 H 80 , 15,19-диметилгептатриаконтан C 39 H 80 и 15,19,23-триметилгептатриаконтан C 40 H 82 ). Некоторые орхидеи при помощи алканов-феромонов привлекают опылителей.
Главным источником алканов (а также других углеводородов) являются нефть и природный газ , которые обычно встречаются совместно.
Восстановление галогенпроизводных алканов:
При каталитическом гидрировании в присутствии палладия галогеналканы превращаются в алканы :
Восстановление иодалканов происходит при нагревании последних с иодоводородной кислотой:
Для восстановления галогеналканов пригодны также амальгама натрия, гидриды металлов, натрий в спирте, цинк в соляной кислоте или цинк в спирте
Восстановление спиртов :
Восстановление спиртов приводит к образованию углеводородов, содержащих то же количество атомов С. Так, например, проходит реакция восстановления бутанола (C 4 H 9 OH), проходящую в присутствии LiAlH 4 . При этом выделяется вода .
Восстановление карбонильных соединений

Реакцию проводят в избытке гидразина в высококипящем растворителе в присутствии KOH .
Реакция Клемменсена :

Гидрирование непредельных углеводородов
Катализатором реакции являются соединения никеля , платины или палладия .
При электролизе солей карбоновых кислот, анион кислоты — RCOO − перемещается к аноду, и там, отдавая электрон превращается в неустойчивый радикал RCOO•, который сразу декарбоксилируется. Радикал R• стабилизируется путём сдваивания с подобным радикалом, и образуется R—R . Например:
Газификация твёрдого топлива (Процессы Бертло, Шрёдера, Бергиуса )
Проходит при повышенной температуре и давлении. Катализатор — Ni (для Бертло), Mo (для Шрёдера) или без катализатора (для Бергиуса):
Реакция идёт в ТГФ при температуре −80 °C . При взаимодействии R и R` возможно образование смеси продуктов (R—R, R`—R`, R—R`)
Получением алканов с помощью декарбоксилирования солей карбоновых кислот, при сплавлении со щелочью (обычно NaOH или KOH):
Низшие алканы обладают наркотическим действием , вызывают асфиксию, раздражают органы дыхания. При хроническом действии алканы нарушают работу нервной системы, что проявляется в виде бессонницы, брадикардии , повышенной утомляемости и функциональных неврозов. Вследствие раздражающего действия газов при подострых, острых и хронических отравлениях развивается пневмония и отёк лёгких.