Реакция Гриньяра
- 1 year ago
- 0
- 0

Реакция Гриньяра — металлорганическая химическая реакция , в которой арил- или алкилмагнийгалогениды (также называемые реактивами Гриньяра) действуют как нуклеофилы , атакуя электрофильный атом углерода с образованием углерод — углеродной связи. Реакция Гриньяра — важный метод как создания углерод -углеродных связей, так и связей углерод-гетероатом ( P , Sn , B , Si и др.)
Реактивы Гриньяра обычно синтезируют в абсолютном простом эфире ( диэтиловом , или тетрагидрофуране ) реакцией металлического магния с арил- или алкилгалогенидом , и другими галоген-содержащими соединениями (обычно применяют иодиды или бромиды ; хлориды применяют редко, а фториды к реакции с магнием не способны). Сама реакция протекает через образование четырёх или шестичленного интермедиата радикалов, галогенид ионов и катионов магния, после перераспределения зарядов устанавливается равновесие Шленка :
Для смещения реакции влево применяются координирующиеся на магний растворители (с жестким гетероатомом, например, простые эфиры — диэтиловый эфир, тетрагидрофуран). Поскольку в них кислород является жестким донором с высоким сродством к жесткому катиону магния, при координировании молекул растворителя из частицы : · вытесняется « мягкий » анион галогена и присоединяется органический радикал, являющийся слабым донором. Кроме того, диоксан образует нерастворимые комплексы с галогенидами магния, а из бензола они выпадают самопроизвольно.
Похожие свойства проявляет цинк , являющийся более мягким аналогом реактивов Гриньяра (в реакциях с галогенидами карбонилов металлов магниевые реагенты атакуют CO даже при сильном охлаждении реакционной смеси, тогда как цинковый реагенты обменивают радикал на атом галогена)
Некоторые реактивы Гриньяра (например) являются коммерчески доступными в виде растворов в диэтиловом эфире или тетрагидрофуране.
1) Взаимодействие металлического магния с органическими галогенидами .
2) Трансметаллирование других металлорганических соединений (например литийорганических).
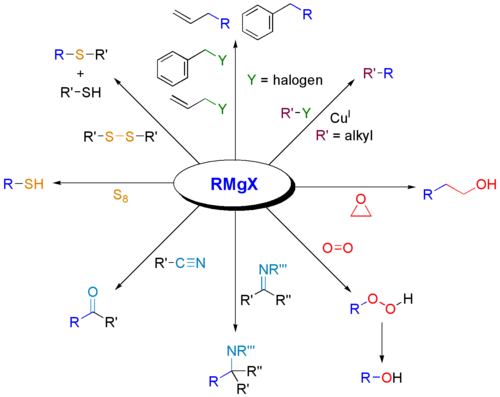
Реактивы Гриньяра широко применяются для синтезов разных классов органических соединений . Некоторые примеры представлены ниже.
Реакции с карбонильными соединениями:

Реакции с другими электрофилами: