Ио (спутник)
- 1 year ago
- 0
- 0


«Спу́тник V» ([спу́тник ви]; «V» от англ. victory — «победа» [ источник не указан 218 дней ] ), регистрационное наименование « Гам-КОВИД-Вак » ( лат. Gam-COVID-Vac ) — комбинированная векторная вакцина для профилактики коронавирусной инфекции COVID-19 , разработанная Национальным исследовательским центром эпидемиологии и микробиологии имени Н. Ф. Гамалеи .
В основе вакцины использован аденовирусный вектор со встроенным в него фрагментом генетического материала SARS-CoV-2 , имеющим в себе информацию о структуре S-белка шипа вируса. Сам фрагмент генетического материала безопасен для человека, но при этом способен обеспечить формирование устойчивого антительного и клеточного иммунного ответа к вирусу. Ввиду применяемой технологии «гетерологический прайм-буст» ( heterologous prime-boost ) препарат состоит из двух компонентов, в состав которых входят рекомбинантные аденовирусные векторы на основе двух различающихся сборок аденовируса человека .
Вакцина была зарегистрирована 11 августа 2020 года Министерством здравоохранения Российской Федерации (регистрационное удостоверение номер ЛП-006395 ), на основании результатов клинических исследований фазы I/II. Данные результаты исследований были опубликованы позже, 4 сентября 2020 года в журнале « The Lancet » . Безопасность вакцины также была показана промежуточными результатами III фазы испытаний , а затем — результатами мониторинга здоровья провакцинированного населения в России и в других странах (от нескольких тысяч до нескольких миллионов человек в каждой), в том числе для лиц старше 60 лет . В июле 2021 года начато также исследование безопасности вакцины для подростков .
2 февраля 2021 года в журнале «The Lancet» были опубликованы промежуточные результаты исследования фазы III, согласно которым эффективность вакцины «Спутник V» составила 91,6 %, а эффективность вакцины против средней или тяжёлой степени COVID-19 — 100 % . После этого вакцина получила разрешение на ввод в гражданский оборот сроком на 5 лет . По предварительным результатам испытаний эффективности вакцины для пожилых было установлено, что она обеспечивает одинаковую защиту для лиц старше 60 лет и даже старше 80 лет . В апреле 2021 года разбработчики вакцины заявили, что по результатам анализа данных 3,8 млн россиян, провакцинированных обоими компонентами «Спутника V», эффективность этой вакцины составила 97,6 % . Данные об эффективности вакцины, в том числе и для лиц старше 60 лет, подтверждаются результатами вакцинации в других странах . Кроме того, по данным разработчиков и независимых исследований , «Спутник V» эффективен против различных штаммов коронавируса.
Помимо «Спутника V», в оборот выпущена однокомпонентная вакцина «Спутник Лайт», которая представляет собой первый компонент «Спутника V». По данным исследований, эффективность «Спутника Лайт» составляет 79,4 % .
Для предоставления населению точной и актуальной информации о вакцине был создан официальный сайт вакцины с информацией на девяти языках. Стратегическим инвестором в разработке и производстве вакцины выступил Российский фонд прямых инвестиций (РФПИ) . По состоянию на июнь 2021 года вакцина «Спутник V» была зарегистрирована в 67 странах .
В России, для жителей застрахованных в системе ОМС , вакцинация «Спутником V» бесплатная, как и любая другая включённая в Национальный календарь профилактических прививок. Массовая вакцинация препаратом стартовала в России в декабре 2020 года .
Вакцина Гам-КОВИД-Вак представляет собой вирусную векторную вакцину на основе ДНК- аденовируса человека, который содержит в своём геноме вставку, кодирующую фрагмент S-белка SARS-CoV-2 и вызывающего иммунный ответ . При создании вакцины использовалась клеточная линия HEK 293 , полученная из абортированного человеческого эмбриона. По утверждению разработчиков вакцины, в самой вакцине этой линии нет, так как с помощью очистки вирусная частица избавлялась от следов человеческой клетки .
Вакцина разработана коллективом лаборатории клеточной микробиологии отдела медицинской микробиологии Национального Центра микробиологии и эпидемиологии им. Н. Ф. Гамалеи Минздрава РФ (руководитель лаборатории — доктор биологических наук, член-корреспондент РАН Д. Ю. Логунов ) и вирусологического центра 48-го Центрального научно-исследовательского института Минобороны РФ , которые разрабатывали также вакцины против Эболы и БВРС .
Вакцина получена биотехнологическим путём, при котором не используется патогенный для человека коронавирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент Ⅰ и компонент Ⅱ. В состав компонента Ⅰ входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа (rAd26), несущий ген S-белка вируса SARS-CoV-2; в состав компонента Ⅱ входит вектор на основе аденовируса человека 5 серотипа (rAd5), также несущий ген S-белка вируса SARS-CoV-2. Компоненты вакцины вводятся внутримышечно , в два этапа с интервалом в 3 недели . Использование двух разных серотипов аденовируса предназначено для обхода любого возможного ранее приобретённого аденовирусного иммунитета в популяции . К тому же если бы использовался один и тот же серотип, то после первой дозы к нему выработался бы иммунитет и вектор был бы уничтожен при получении второй дозы, два разных серотипа уменьшают шансы на такой сценарий .
В основе препарата «Спутник V» находятся две цепи ДНК-вируса, что отличает её от вакцин Pfizer и Moderna, которые используют более хрупкую цепь РНК. Прочная белковая оболочка обеспечивает лучшую сохранность генетического материала, что позволяет перевозить и хранить вакцину без использования критически низких температур .

После введения вакцины ген-вектор попадает в соматические [ какие? ] клетки, в результате чего происходит продуцирование ими S-белка SARS-CoV-2, в ответ на что в организме хозяина (привитого) вырабатываются антитела к этому белку . По данным директора НКО «Коллективный иммунитет», биолога Антонины Обласовой, этот процесс происходит в клетках в месте введения вакцины, а не по всему организму . Введение второго компонента вакцины способствует формированию более полноценного иммунитета против инфекции и большего количества B-клеток памяти . Два разных серотипа аденовируса использованы во избежание возникновения выраженного иммунного ответа к нему и уничтожения вектора до его внедрения в клетку и начала продукции клеткой S-белка . Двухвекторный вариант вызывает более сильный иммунный ответ по сравнению с одновекторным; кроме того, аденовирус 26 серотипа стимулирует также клеточный иммунитет (формирование специализированных лимфоцитов , развивающихся в вилочковой железе ) . В некоторых случаях при тестировании после вакцинации методом ИФА на антитела, они могут показать отрицательные результаты, так как ряд тестов рассчитан на выявление (к N-белкам вируса), а не (в данном случае к S-белкам вируса) .

Полноценный иммунный ответ вырабатывается через 3 недели после V2 (введения второго компонента вакцины), таким образом, на 42-й день от момента начала курса вакцинации при соблюдении его сроков (3 недели между V1 и V2) .
Изначально было установлено, что для сохранности свойств вакцины «Спутник V» во всей цепочке холодовой цепи транспортировки и хранения требуется температура не выше минус 18 °С , что привело к дозакупке соответствующего холодильного ( морозильного ) оборудования . Впоследствии министр здравоохранения России М. Мурашко, заявил, что Минздрав одобрил изменения в регистрационное удостоверение условий хранения и перевозки «Спутник V», разрешив температуру от +2 до +8 градусов, при этом такая вакцина будет выпускаться отдельно .
Создание сухой лиофилизированной формы является длительным и довольно сложным процессом (поэтому себестоимость выше), но она более удобна для хранения и транспортировки, и предназначается для использования в труднодоступных регионах России . По оценкам главы Центра им. Гамалеи Александра Гинцбурга, на вакцинацию бо́льшей части населения России, исходя из доступных мощностей, потребуется 9—12 месяцев .
23 октября 2020 года министр здравоохранения России Михаил Мурашко заявил, что вакцинация против коронавирусной инфекции после запуска больших объёмов производства Гам-КОВИД-Вак будет бесплатной для всех граждан России . Минздрав России зарегистрировал предельную отпускную цену производителя на вакцину от коронавируса «Спутник V» на уровне 1942 рубля за два компонента . 25 февраля 2021 года было объявлено о снижении отпускной цены за 2 компонента в 2 раза до 866 рублей 81 копейки, что объясняется отработкой и оптимизацией технологии промышленного производства препарата, а также ростом объёмов производства .
С 3 декабря 2020 года вакцины против COVID-19 включены в России в перечень жизненно необходимых и важнейших лекарственных препаратов . Вакцинация против COVID-19 в России также внесена в национальный календарь профилактических прививок для вакцинации по эпидемическим показаниям .
В мае 2020 года Национальный центр эпидемиологических и микробиологических исследований объявил о разработке вакцины, не имеющей серьёзных побочных эффектов . К августу 2020 года были закончены два клинических испытания первой и второй фазы с участием по 38 испытуемых в каждом . По данным, предоставленным главой Центра Гамалеи, разработка вакцины «Спутник V» стоила 1,5 млрд рублей .
Разработка вакцины, а также доклинические и I / II этапы клинических испытаний велись совместно «НИЦЭМ им. Н. Ф. Гамалеи» Минздрава России и «48 ЦНИИ» Минобороны России , имевших до этого опыт разработки подобных вакцин ( ГамЭвак и ). В числе 18 разработчиков вакцины также значатся и руководители этих научных учреждений: А. Л. Гинцбург и С. В. Борисевич .
11 августа 2020 года о регистрации в России первой вакцины от коронавируса на совещании с президентом В. В. Путиным доложил министр здравоохранения М. А. Мурашко . Вакцина зарегистрирована условно, в соответствии с принятым Правительством Российской Федерации порядком доступа на рынок препаратов, предназначенных для профилактики COVID-19 . Соответствующее регистрационное удостоверение под номером ЛП-006395 было выдано 11 августа Минздравом России . 25 августа было выдано удостоверение ЛП-006423 для лиофилизата «Гам-КОВИД-Вак-Лио» .
Начало промышленного выпуска вакцины Гам-КОВИД-Вак было запланировано на сентябрь 2020 года . К концу 2020 года собственное производство Гамалеи, согласно интервью латвийскому интернет-изданию Meduza , планировалось вывести к рубежу 2020—2021 года на производственную мощность 3—5 млн доз в месяц . По данным телеканала Вести.ру , к 15 августа произошёл запуск производства; три предприятия могли выпускать порядка миллиона доз в месяц на каждом с потенциальным удвоением мощностей к зиме .
В начале сентября 2020 года создатели вакцины опубликовали в журнале The Lancet статью с описанием вакцины и результатами её клинических испытаний I и II фазы на людях . 2 февраля 2021 года в журнале были опубликованы промежуточные результаты III фазы клинических испытаний вакцины .
21 декабря 2020 года Российский фонд прямых инвестиций (РФПИ), Центр им. Гамалеи, российская фармкомпания « Р-Фарм » с одной стороны и англо-шведская фармацевтическая компания AstraZeneca с другой подписали соглашение о разработке и реализации программы клинических исследований комбинации вакцин от коронавируса. Стороны договорились развивать научные и деловые взаимоотношения, в рамках которых будут изучены возможности совместного использования российской вакцины «Спутник V» и препарата AZD1222 , разработанного AstraZeneca и Оксфордским университетом , ради более стойкой и длительной защиты человека от коронавируса .
В январе 2021 года начаты испытания вакцины «Спутник Лайт», представляющей собой по существу первый компонент вакцины «Гам-КОВИД-Вак» и предназначенной для ускорения массовой вакцинации путём однократного введения препарата. Длительность защитного эффекта при этом предполагается ниже, чем от полной вакцинации «Спутник V» (со слов А. Гинцбурга, в пределах 4—5 месяцев ), при этом при необходимости возможно довакцинирование вторым её компонентом .
4 марта 2021 года Европейское агентство лекарственных средств (EMA) начало проверку вакцины «Спутник V» на соответствие стандартам ЕС по эффективности, безопасности и качеству .
Доклинические испытания рекомбинантной вакцины на токсичность, безопасность, иммуногенность и защитную эффективность на крупных и мелких животных были проведены на базе 48 ЦНИИ МО РФ . Испытания проводились на двух видах чувствительных млекопитающих: на золотистых сирийских хомячках и двух видах приматов . Достижения сотрудников военного НИИ помогли сократить сроки доклинической оценки безопасности и эффективности вакцины. В частности, использовалась разработанная в НИИ методология количественной оценки возбудителя и лабораторная модель воспроизводства тяжёлого острого респираторного заболевания .
Результаты 1 и 2 фазы испытаний были опубликованы 4 сентября 2020 года в журнале « The Lancet » . В них приняло участие в общей сложности 76 человек (2 группы по 38 человек ), большинство побочных эффектов было умеренным, серьёзных побочных эффектов не было, смертей не было. Испытания 3 фазы были проведены с 7 сентября по 24 ноября 2020 года уже после регистрации вакцины Министерством здравоохранения РФ , и также опубликованы в журнале « The Lancet » . В них получили вакцину 16 427 человек, и 5 435 были в группе плацебо. Эффективность вакцины составила 91—95 %. У получивших вакцину большинство нежелательных явлений было 1-й степени (7 485 явлений). 45 человек из вакцинной группы и 23 из плацебо-группы имели серьёзные побочные явления, но ни одно из них не было признано связанным с вакцинацией. Было зарегистрировано четыре случая смерти (три из вакцинной группы и один из группы плацебо), однако они не были связаны с вакциной .
Данная фаза клинических испытаний представляет собой открытое исследование безопасности, переносимости и иммуногенности препарата «Гам-КОВИД-Вак» ( англ. Gam-COVID-Vac ). 16 июня 2020 года Минздрав РФ выдал разрешение № 241 на проведение данного клинического исследования (КИ) .
Испытания жидкой вакцины проводились в Главном военном клиническом госпитале (ГВКГ) имени Н. Н. Бурденко (в филиале № 7 в г. Сергиев Посад-6) . В испытании приняли участие 38 добровольцев. На первом этапе испытания (фаза I) была протестирована безопасность, переносимость и иммуногенность каждого компонента вакцины в отдельности: первой группе из 9 человек был инъецирован компонент I, второй группе из 9 человек был инъецирован компонент II. На втором этапе (фаза II) испытание проводилось по бустерной схеме: 20 человек получили инъекции компонента I, и через 21 день — компонента II. У всех добровольцев выработались высокие титры антител COVID‑19. При этом ни у кого из них не было отмечено серьёзных осложнений иммунизации .
Данная фаза клинических испытаний представляет собой открытое исследование безопасности, переносимости и иммуногенности препарата «Гам-КОВИД-Вак Лио» ( англ. Gam-COVID-Vac Lyo ). 16 июня 2020 года Минздрав РФ выдал разрешение № 242 на проведение КИ .
Испытания лиофильно высушенной вакцины проводились в Сеченовском университете . В испытании приняли участие 38 добровольцев. На первом этапе (фаза I) была протестирована безопасность, переносимость и иммуногенность каждого компонента вакцины в отдельности: первой группе из 9 человек был введён компонент I, второй группе из 9 человек был введён компонент II. На втором этапе (фаза II) испытание проводилось по бустерной схеме: 20 человек получили инъекции компонента I, а через 21 день — компонента II. У всех добровольцев были определены высокие титры антител к COVID‑19, ни у кого из них не было отмечено серьёзных осложнений после иммунизации .
Данная фаза представляет собой рандомизированное двойное слепое плацебо-контролируемое многоцентровое клиническое исследование при параллельном определении эффективности, безопасности и иммуногенности комбинированной векторной вакцины «Гам-КОВИД-Вак» в профилактическом лечении инфекции SARS-CoV-2. Разрешение на проведение данного КИ под номером № 450 было выдано Минздравом РФ 25 августа 2020 года, уже после регистрации вакцины . В данном КИ предполагалось принять 40 000 добровольцев в возрасте от 18 лет, разделённых на две группы (3:1) — исследовательская группа из 30 000 добровольцев, получающих комбинированную векторную вакцину Гам-КОВИД-Вак против вируса SARS-CoV-2, и контрольная группа из 10 000 добровольцев, получающих плацебо . В итоге, согласно промежуточным результатам, которые были опубликованы в журнале «The Lancet» , непосредственно вакцину получили от 14 964 до 16 427 человек, в группу плацебо вошли от 4902 до 5435 . Прививка первой дозой выполнена с 7 сентября по 24 ноября 2020 года . Вакцинация участников третьей фазы испытаний закончилась в декабре 2020 года, а наблюдение за ними должно было длиться 180 дней .
Исследование началось 26 августа 2020 на территории Москвы, были задействованы 25 медицинских организаций города . Мониторинг здоровья участников должен был длиться как минимум 6 месяцев, для этого было создано специальное мобильное приложение с дневником самонаблюдения, а некоторые участники получили электронные браслеты для измерения артериального давления и температуры тела .
Согласно реестру испытаний, завершение III—IV фаз на основной выборке из 40 000 участников запланировано на 31 декабря 2022 .
В феврале 2022 года стало известно, что вакцина получила постоянную регистрацию в России .
5 июля 2021 года в Москве на базе двух больниц начались первая и вторая фаза испытаний вакцины на подростках в возрасте от 12 до 17 лет. Исследование ведётся на 100 добровольцах, ранее не болевших COVID-19 и продлится один год, при этом для подростков предполагается использовать меньшую дозировку препарата. Начало третьей фазы этих испытаний запланирована на конец лета 2021 года .
Проводится исследование безопасности, переносимости и иммуногенности вакцины «Гам-КОВИД-Вак» против COVID-19 с участием добровольцев в возрастной группе старше 60 лет. Разрешение на проведение было выдано Минздравом РФ 13 октября 2020 года (№ 566); завершение испытаний запланировано на 31 декабря 2021 года . В исследовании принимают участие 110 человек (по данным реестра может принять до 150 человек).
В марте 2021 года глава центра Гамалеи сообщил, что, несмотря на предварительные опасения, вакцина показала одинаковую эффективность для пациентов старше 60 и даже старше 80 лет .
Клинические исследования II / III фазы проводились в Беларуси , Индии , Венесуэле , ОАЭ .
Наблюдательные клинические исследования проводятся в Сан-Марино , Сербии , Бразилии , Аргентине и других странах.
11 ноября 2020 года НИЦЭМ им. Н. Ф. Гамалеи совместно с Российским фондом прямых инвестиций опубликовали первый промежуточный анализ данных фазы III клинических исследований вакцины в России. Согласно публикации, эффективность применения вакцины «Спутник V» составила 92 %, расчёт проводился на основе распределения 20 подтверждённых случаев, выявленных в группе плацебо и в группе, получавшей вакцину .
2 февраля 2021 года в журнале «The Lancet» были опубликованы более полные промежуточные результаты исследования
фазы III
. В анализ первичных результатов были включены
19 866 человек
, получивших вакцину или плацебо. После 21-го дня исследования у 16 из
14 964 участников
в группе вакцинированных (0,1 %) и 62 из
4 902 участников
в группе плацебо (1,3 %) подтвердился COVID-19. Эпидемиологическая эффективность
вакцины составила 91,6 %
+3,6%
−5,7%
(погрешность указывает
95%-й
доверительный интервал
, обусловленный вероятностным статистическим разбросом). 97 случаев COVID-19 (63 в группе вакцинированных и 34 в группе плацебо) отмечены ранее, чем через 21 день после введения первой дозы, то есть до начала действия иммунитета, вызванного вакциной, и в анализ не включены. Эпидемиологическая эффективность для участников старше 60 лет равна 91,8 % (в 95%-м доверительном интервале от 67,1 % до 98,3 %) и статистически не отличается от эффективности для всей группы. Случаев умеренного или тяжёлого течения COVID-19 в группе вакцинированных не отмечено, в группе плацебо таких было 20; это означает эффективность против таких форм болезни в 95%-м доверительном интервале от 94,4 % до 100 %. Расхождение между вероятностями заболевания в группах вакцинированных и плацебо на временно́м графике начинается примерно на 18-й день после получения первой дозы
.
| Возраст, лет |
Случаев
COVID-19 |
Группа вакцины
(случаев / из / %) |
Группа плацебо
(случаев / из / %) |
Эффективность
(в доверит. интервале 95 %) |
|---|---|---|---|---|
| 18—30 | 5 | 1 / 1596 (0,1 %) | 4 / 521 (0,8 %) | 91,9 % (51,2—99,3) |
| 31—40 | 17 | 4 / 3848 (0,1 %) | 13 / 1259 (1,0 %) | 90,0 % (71,1—96,5) |
| 41—50 | 19 | 4 / 4399 (0,1 %) | 15 / 1443 (1,0 %) | 91,3 % (73,7—96,9) |
| 51—60 | 27 | 5 / 3510 (0,1 %) | 22 / 1146 (1,9 %) | 92,7 % (81,1—97,0) |
| > 60 | 10 | 2 / 1611 (0,1 %) | 8 / 533 (1,5 %) | 91,8 % (67,1—98,3) |
| Всего | 78 | 16 / 14964 (0,1 %) | 62 / 4902 (1,3 %) | 91,6 % (85,6—95,2) |
| Эффективность вакцины «Спутник V» в зависимости от времени | ||||
| Начиная со дня 1-й дозы | 175 | 79 / 16427 (0,5 %) | 96 / 5435 (1,8 %) | 73,1 % (63,7—80,1) |
| Начиная с 14 дня после 1-й дозы | 109 | 30 / 14999 (0,2 %) | 79 / 4950 (1,6 %) | 87,6 % (81,1—91,8) |
19 апреля 2021 представители Российского фонда прямых инвестиций в своём пресс-релизе заявили, что эффективность вакцины «Спутник V» по результатам анализа данных 3,8 млн вакцинированных россиян составила 97,6 % . Согласно данным о вакцинации россиян, полностью привитых обоими компонентами в период с 5 декабря 2020 года по 31 марта 2021 года в рамках программы массовой гражданской вакцинации, заболеваемость начиная с 35-го дня с даты первого укола составила всего 0,027 %. При этом заболеваемость среди невакцинированного взрослого населения за сопоставимый период с 35-го дня после запуска массовой гражданской вакцинации составила 1,1 % .
16 февраля 2021 года специалисты научного центра вирусологии и биотехнологии «Вектор» заявили о подтверждении эффективности «Спутника V» в отношении британского штамма COVID-19 («Альфа») , а 16 июня 2021 года А. Л. Гинцбург сообщил, что лабораторные исследования показали высокую эффективность вакцины против «индийского» штамма коронавируса («Дельта») .
12 июля 2021 года в ведущем международном журнале «Vaccines» опубликовали данные о том, что «Спутник V» эффективен против новых штаммов коронавируса . Согласно данным статьи, снижение уровня вируснейтрализующей активности к ряду штаммов у «Спутника V» значительно меньше по сравнению другими вакцинами.
В сентябре 2021 года аргентинские учёные заявили, что вакцинация двумя компонентами «Спутник V» эффективнее против дельта-штамма, чем после препаратов компаний AstraZeneca и Sinopharm .
Россия. НИИ гриппа им. А. А. Смородинцева в сотрудничестве с Институтом междисциплинарных медицинских исследований при Европейском университете в Санкт-Петербурге с 19 февраля 2021 года проводят исследование жителей Санкт-Петербурга , привитых «Спутником V» и давших согласие на измерение уровня антител в крови. Выраженный иммунный ответ уже после первой дозы вакцины отмечался у 83 % участников; на 70-й день (уже после введения второй дозы) антитела IgG не были обнаружены у единственного участника из нескольких сотен. Также у большинства привитых нарастали титры нейтрализующих антител (нейтрализующие антитела на протяжении 70 дней не определялись только у 3 из 57 исследованных) . Методика исследований и предварительные данные были опубликованы в американском журнале « » , а текущие результаты — в журнале « », издаваемым британской Nature Publishing Group . Один из авторов исследования, эпидемиолог Антон Барчук считает, что исследование подтверждает данные по эффективности, полученные создателями «Спутника V» .
В препринте исследования, проведённого этой группой учёных, был сделан вывод о 81 % эффективности вакцины в предотвращении госпитализации и 76 % эффективности в защите от тяжёлых повреждений лёгких . Хотя достоверно неизвестно, какой вакциной прививались испытуемые и каким штаммом заражались, подавляющее большинство россиян привито вакциной «Спутник V» и заражено штаммом Дельта.
В публикации научной статьи в журнале Vaccines, авторами которой являются Ольга Матвеева и Александр Ершов описан анализ выборки заболевших москвичей. Выборка была создана летом 2021 года из тех, кто обратился за медицинской помощью в июне и июле 2021 года. В это время в Москве доминировал Дельта вариант коронавируса. В анализе был выявлен тренд на повышение эффективности вакцины «Спутник V» по мере увеличения тяжести заболевания. Эффективность вакцины была выше в отношении смерти или тяжелой формы COVID-19. Кроме того, защитный эффект вакцины был сильнее выражен в более молодых возрастных группах. Для наиболее молодой группы (18—50 лет) эффективность вакцины по предотвращению смерти составляла 95 %, а для старшего поколения (50+) эффективность вакцины была уже ниже и составила 74 %. Защита от тяжелой формы заболевания в группе 18-50 лет в июне-июле была оценена как 81 %, а в группе старше 50 лет — 68 % .
Венгрия. В апреле 2021 года власти Венгрии опубликовали результаты исследований эффективности пяти вакцин (используемых в стране «Спутника V», «Moderna», «Pfizer», «Sinopharm» и «AstraZeneca»), проводившихся период с декабря 2020 года по 20 апреля 2021 года и оценивающих процент заболевших и умерших среди вакцинированных двумя компонентами. Согласно их данным, «Спутник V» показал наименьший процент по обоим показателям: на 100 000 населения, привитого этой вакциной, заболело 95 человек (менее 0,1 %), а средняя смертность составила 1 человек (0,001 %) . Ряд исследователей обратили внимание, что «Спутник V» начал использоваться в стране позже других вакцин (с 11 февраля), в связи с чем вероятность заболеть после прививки им была меньше, а также что не были опубликованы возрастные группы вакцинированных и методика подсчёта, в связи с чем цифры могут быть неточны. В то же время, сама эффективность «Спутника V» под сомнение ими не ставилась .
В ноябре 2021 опубликовано исследование, оценивающее эффективность тех же пяти вакцин на 3,74 млн жителей Венгрии, привитых обеими дозами, в том числе на 0,82 млн, привитых «Спутником V». Согласно опубликованным результатам, относящимся к периоду с 22 января по 10 июля 2021, усреднённая по возрастным когортам эффективность «Спутника V» против заражения составила 85,7 % («Pfizer» — 83,3 %, «Moderna» — 88,7 %, «AstraZeneca» — 71,5 %, «Sinopharm» — 68,7 %). Эффективность вакцин против смерти от COVID-19 составила от 87,8 % («Sinopharm») до 97,5 % («Спутник V»). Частота заражений среди людей, привитых «Спутником V», составила 1,73 случая на 100 000 человеко-дней (среди невакцинированных — 59,03 случая, отношение рисков — 34,1); частота смертей — 0,04 случая на 100 000 человеко-дней (среди невакцинированных — 1,88 случая, отношение рисков — 47) .
Аргентина. Министерство здравоохранения провинции Буэнос-Айрес ( Аргентина ) заявило в начале июня 2021, что согласно проведённому в регионе исследованию среди населения в возрасте 60—79 лет , эффективность первой дозы «Спутника V» составляет 78,9 % против заражения COVID-19, 84,7 % против смерти от коронавирусной болезни и 87,6 % против госпитализации. Группы включали 40 387 однократно вакцинированных с 29 декабря 2020 по 21 марта 2021 и 146 194 невакцинированных; включены только лица, ранее не болевшие COVID-19; учитывались лишь случаи болезни с 21 дня после вакцинации. Этот результат согласуется с опубликованной разработчиками эффективностью от заражения, равной 79,4 % для первой дозы.
Чуть позже, 1 июля 2021 года, министерство здравоохранения Аргентины сообщило, что по предварительным результатам на выборке из 471 682 аргентинцев возрастом старше 60 лет в феврале-июне 2021, эффективность против смерти от COVID-19 составляет 74,9 % для первой дозы «Спутника V» и 93,3 % для полного двухдозового курса вакцинации (для сравнения, в тех же условиях вакцина AstraZeneca показала эффективность 79,5 % и 88,8 %, вакцина Sinopharm — 61,6 % и 84,0 %) .
15 июля власти Аргентины опубликовали результаты нового исследования , проведённого Национальным научно-техническим исследовательским советом. Согласно данным исследования, более 90 % привитых «Спутником V», помимо выработки антител, получают и долгосрочный клеточный иммунитет .
Ещё одно исследование, проведённое под руководством американских учёных и опубликованное 26 июля в журнале « Nature Communications » , показало эффективность «Спутника V» против различных штаммов коронавируса. Учёные установили, что вакцина хорошо справляется с исходной версией вируса и штаммом « Альфа »; со штаммом « Бета » и вирусами с мутацией E484K — хуже, но при этом всё равно защищает от тяжёлых форм заболевания. Действие против штамма « Дельта » в данной работе не оценивалось .
В проведённом сотрудниками НИИ Гамалеи исследовании нейтрализующих антител против штамма Омикрон и против штамма B.1.1.1. после вакцинации «Спутник V» был сделан вывод, что уровень нейтрализующих антител против Омикрона в 11,76 раз ниже у вакцинированных и в 7,13 раз ниже у вакцинированных и ревакцинированных, чем уровень нейтрализующих антител против штамма B.1.1.1., причём нейтрализующие антитела к Омикрону были обнаружены у всех ревакцинированных .
В журнале EClinicalMedicine от Lancet было опубликовано исследование эффективности однокомпонентной вакцины «Спутник Light» для пожилых людей . Она была проверена в реальных условиях в ходе ретроспективного когортного исследования. Приняли участие около 80000 человек в возрасте от 60 до 79 лет, наблюдение длилось до 82 дней, в среднем 44 дня.
Вакцина оказалась на 78,6 % процента эффективна против инфекции, на 87,6 % против госпитализации и на 84,8 % против смерти. Такая эффективность сопоставима с эффективностью одной дозы других вакцин от COVID-19. Люди, принявшие участие в исследовании, могли не отражать всю популяцию, бессимптомные инфекции и эффективность вакцинации против новых штаммов вируса не были тщательно изучены.
В ещё одном исследовании из Аргентины были изучены антитела после «Спутника V» у 118 медицинских работников младше 65 лет . В течение 6 месяцев изучалось их количество и эффективность против различных штаммов вируса. Титры антител за это время сократились в 3-4 раза. Но нейтрализующая способность этих антител против всех штаммов коронавируса при этом росла. Явление увеличения эффективности антител при снижении их концентрации уже наблюдалось у переболевших людей. Нейтрализующая активность антител была снижена в 2,9, 9,7, 4,2 и 3,4 раза для Альфа, Бета, Гамма и Дельта штаммов по сравнению с оригинальным штаммом через 120 дней после прививки.
В сентябре 2021 года специалисты Института вирусологии факультета медицинских наук Национального университета Кордовы обнародовали результаты исследования ведущих мировых вакцин на способность защищать людей от штамма «Дельта». Самой эффективной в этом вопросе была названа российская «Спутник V», следовали за ней в рейтинге AstraZeneca и Sinopharm. При этом лучше, по версии аргентинских учёных, «Спутник V» от «Дельта»-штамма защищает тех, кто привился его обоими компонентами, но до этого никогда не болел COVID-19 .
Белоруссия. В ноябре 2021 опубликован препринт специалистов из Белоруссии, где выполнена оценка эффективности «Спутника V». На 1 сентября 2021 (7—8 месяцев с начала вакцинации) среди 1,216 млн полностью вакцинированных «Спутником V» доля заболевших ковидом составляет 0,19 %, тогда как среди непривитого населения — 5,08 % (отношение рисков — 26,7) .
Другие страны. 6 июля 2021 года в журнале « Nature » была опубликована статья, обобщающая имеющиеся данные о безопасности и эффективности вакцины . Автор статьи сделал вывод, что несмотря на преждевременную регистрацию вакцины в России и критику первых исследований, данные указывают на то, что вакцина безопасна и эффективна и может в скором времени получить одобрение ВОЗ и EMA . По данным статьи, исследования «Спутника V» в ОАЭ , проведённые на 81 тыс. человек с введением обеих доз вакцины, показало эффективность 97,8 % в предотвращении симптоматического COVID-19 и 100 % — от предотвращения тяжёлого течения болезни. Изложены также вышеприведённые оценки эффективности, полученные в Аргентине, и резюмированы исследования безопасности в Аргентине и Сан-Марино (см. ).
Высокая эффективность российского «Спутника V» доказана и эпидемиологами Сан-Марино и римского Национального института инфекционных заболеваний имени Л. Спалланцани . Их совместное исследование показало, что антитела вырабатываются у 99 % привитых российской вакциной против коронавируса — в большом количестве и высокого качества. Исследование было не только лабораторным, но и жизненным: подавляющее большинство граждан Сан-Марино привиты «Спутником V» — заболеваемость в государстве нулевая, как официально не раз заявляли власти .
Технологической платформой, на которой создана вакцина «Спутник V», является вирусный вектор — инструмент, используемый для доставки генетического материала в клетки. Впервые такая технология была использована в 1970-х годах . В «Спутнике V» используется нереплицируемый вирусный вектор — то есть вирус, лишённый механизма размножения , поэтому он не представляет опасности заражения для организма. Вектор используется для транспортировки в клетку вакцинируемого организма генетического материала из другого вируса, против которого делается вакцина.
Конкретно в качестве вектора в вакцине «Спутник V» используется аденовирусный вектор. Аденовирусы , извлекаемые из аденоидов человека и в обычном состоянии вызывающие ОРВИ ( аденовирусную инфекцию ), уже в 1990-х годах стали использовать для создания векторов . Технология использования аденовирусных векторов в качестве векторных вакцин является безопасной и эффективной, что подтверждается в многочисленных исследованиях .
На этой технологической платформе создано 3 вакцины против лихорадки Эбола , с помощью которых вакцинировано более 60 000 человек в Африке, Китае и России ; одобрено 2 препарата против рака, использованные для терапии более 30 000 человек в Китае ; проведено более 250 клинических исследований , проведены или ведутся исследования по долгосрочной безопасности, в том числе отсутствие риска канцерогенности и снижения фертильности препарата .
По предварительным данным фазы III клинических исследований вакцины «Спутник V», опубликованных её разработчиками в феврале 2021 года в медицинском журнале The Lancet , вакцина является безопасной в применении. Статью разработчиков в журнале прокомментировал профессор Ян Джонсон ( Великобритания ), признавший эффективность и безопасность этой вакцины .
45 участников (0,3 %) из 16 427 в группе вакцинирования и 23 (0,4 %) из 5435 в группе плацебо сообщили о серьёзных побочных эффектах, однако независимый комитет по мониторингу данных подтвердил, что они не связаны с вакцинированием. В ходе исследования умерло четыре испытуемых: 3 из 16 427 вакцинированных и 1 из 5435 в группе плацебо. В группе вакцинированных одна смерть была связана с переломом грудного отдела позвоночника, две — с COVID-19. У умерших от COVID-19 симптомы развились на 4-й и на 5-й день после первой дозы вакцины (таким образом, оба участника были инфицированы до включения в исследование, несмотря на отрицательный результат ПЦР), оба имели сопутствующие заболевания (сердечно-сосудистые и эндокринологические, соответственно). В группе плацебо участник умер от геморрагического инсульта .
Государственный конгресс Сан-Марино объявил о первых результатах двух начатых исследований вакцины Sputnik V, широко используемой в этой маленькой стране, совместно с Болонским университетом и Римским Национальным институтом инфекционных заболеваний Lazzaro Spallanzani («Спалланцани») в Риме. Первое исследование, проведённое в сотрудничестве с Болонским университетом, было посвящено выявлению побочных реакций на введение препарата, которые на данный момент «можно сказать практически нулевые».
Второе исследование, даже более важное, касается количественной и качественной оценки антител, разработанных российской вакциной: «Исследование все ещё продолжается, но собранные на данный момент данные показывают, что эффективность вакцины выше, чем указано в исследованиях, опубликованных в специализированных журналах, таких как Lancet. Эффективность близка к 100 %». Члены Государственного Конгресса оценили сотрудничество с Российским фондом РФПИ как «отличное» и выбор использования Sputnik V «выигрышным» .
Аргентина. Министерство здравоохранения провинции Буэнос-Айрес ( Аргентина ) опубликовало 24 июня 2021 года результаты мониторинга безопасности вакцин на материале 2,8 млн доз вакцины «Спутник V», использованных в этом регионе с 29 декабря 2020 по 3 июня 2021 (в сравнении с 1,3 млн доз и 0,9 млн доз вакцин «Sinopharm» и «Covishield/AstraZeneca», соответственно). Частота тяжёлых «реакций, предположительно обусловленных иммунизацией» (РПОИ), составляет 0,7; 0,8 и 3,2 случая на миллион доз для перечисленных трёх вакцин, соответственно. Среди лёгких РПОИ, связанных с вакцинацией «Спутником V», отмечаются лихорадка (47 %), головная боль (45 %), боль в мышцах или суставах (39,5 %), а также реакции в месте инъекции: боль (46,5 %) и зуд (7,4 %). Смертей, связанных с иммунизацией, не зафиксировано .
Опубликован также более полный отчёт Минздрава Аргентины о безопасности вакцин по результатам применения 6 964 344 доз «Спутника V» (в основном первой инъекции) с 29 декабря 2020 по 2 июня 2021 года включительно. В отчёте утверждается, что количество наблюдавшихся побочных эффектов составляет 40 445 (соответствует частоте 0,58 %), серьёзных (то есть потребовавших госпитализации) побочных эффектов — 194 случая, или 0,00278 % (что чуть меньше, чем у «AstraZeneca», и больше, чем у «Sinopharm») . Авторы отчёта предостерегают от прямого сравнения безопасности вакцин по этим данным, поскольку распределение вакцин по половозрастным когортам и по датам вакцинирования различается. Смертей, связанных с вакцинацией «Спутником V», не зарегистрировано. 38 098 случаев побочных эффектов, считающихся связанными с иммунизацией «Спутником V», классифицированы следующим образом:
Кроме того, для 316 случаев госпитализации (0,0045 %) продолжается анализ их возможной связи с вакцинацией. Для 5 случаев госпитализации после прививки связь с вакцинацией не установлена: 2 случая синдрома Гийена — Барре (острый полирадикулоневрит), 2 случая иммунной тромбоцитопении и 1 случай перикардита .
Белоруссия. В ноябре 2021 опубликован препринт специалистов из Белоруссии , где выполнена оценка безопасности «Спутника V» по результатам его применения в этой стране. На 1 сентября 2021 (7-8 месяцев с начала вакцинации) среди 1,487 млн вакцинированных «Спутником V» (в том числе 1,216 млн полностью вакцинированных, то есть в сумме 2,703 млн доз) наблюдалось 80 832 случая побочных реакций (2,99 %), большинство из которых оценены как слабые и умеренные (головная боль, гипертермия, астения). Обнаружены две серьёзные побочные реакции, обе после первой дозы: аллергическая крапивница и анафилактоидная реакция; оба пациента полностью восстановились без каких-либо последствий. За рассматриваемый период среди вакцинированного населения зарегистрирована 281 смерть (независимо от причины), все случаи не связаны с вакцинацией.
Сан-Марино. Исследователи из Италии, Великобритании и Сан-Марино выполнили обследование лиц, вакцинированных «Спутником V» в Сан-Марино, которые опрашивались через 7 дней после прививки (2558 человек после введения первой дозы, 1288 человек — после второй дозы). Медианный возраст участников 68 лет, 56 % — женщины. После первой дозы 16,4 % участников сообщили и о местных, и о системных побочных эффектах, 25,8 % — только о системных, 10,2 % — только о местных симптомах. После второй дозы проявления побочных эффектов составляли, соответственно, 31,9 %, 18,5 % и 16,1 %. Главные побочные эффекты вакцинирования: боль в месте укола (24,8 % после первой дозы и 43,8 % после второй), астения (23,8 % и 31,9 %), головная боль (18,5 % и 21,0 %), боль в суставах (16,5 % и 21,9 %). Степень проявления побочных симптомов (оценивалась по 4-балльной системе) после первой дозы 20 участников оценили как значительную (степень 3) и 8 как сильную (степень 4). После второй дозы 3-ю степень указали 17 участников и 4-ю степень — 4 участника. В абсолютном большинстве случаев все проявления побочных эффектов укладывались в двое суток после прививки. Тяжёлых реакций на иммунизацию не выявлено. Исследования продолжены до 3-месячного срока после прививки.
12 июля 2021 года были опубликованы результаты наблюдательного исследования 4 фазы «ROCCA», проведённого на 2558 пациентах старшего возраста (66±14 лет). Исследование продемонстрировало высокий профиль безопасности вакцины для людей старше 60 лет при массовой вакцинации населения. В сравнении с другими вакцинами против COVID-19 «Спутник V» имеет более высокий или равный профиль переносимости. Побочные эффекты у «Спутник V» не превышают таковых у других вакцин, пациенты с хроническими заболеваниями, согласно результатам исследования, переносят «Спутник V» лучше, чем альтернативы .
Сербия. 12 июля 2021 года заместитель министра здравоохранения Сербии Мирсад Джерлек заявил, что вакцина «Спутник V» вызвала наименьшее число побочных эффектов по сравнению с другими вакцинами. В Сербии двумя компонентами вакцин привито более 3 млн человек (почти половина населения), из них до 25 % — «Спутником V» .
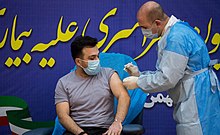
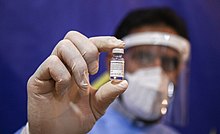
Иран. От 13435 вакцинированных в Иране медицинских работников авторы исследования получили 3236 отчётов о побочных эффектах. Наиболее распространёнными побочными эффектами были боль в месте инъекции (56,9 %), усталость (50,9 %), боль в теле (43,9 %), головная боль (35,7 %), лихорадка (32,9 %), боль в суставах (30,3 %), озноб (29,8 %) и сонливость (20,3 %). Анафилактический шок наблюдался у 0,1 % вакцинированных, о смертельных исходах не сообщалось. Побочные эффекты чаще возникали у молодых людей, чем у старых, чаще у женщин, чем у мужчин, чаще после первой инъекции, чем после второй. Результаты исследования также подтверждают высокую гуморальную иммуногенность против COVID-19 после получения вакцины Спутник V .
Статья в журнале «Nature». Данные различных испытаний «Спутника V» в разных странах были обобщены в журнале « Nature » за 6 июля 2021 года. В нём сообщалось , что упомянутые выше исследования в Аргентине, основанные на применении 2,8 млн доз «Спутника V», показали отсутствие случаев со смертельным исходом и выявили главным образом лёгкие побочные эффекты. О смертельных случаях, по данным статьи, не сообщали также и власти Сан-Марино (данные приведены выше) и Сербии, где вакцина широко применяется. Исследования в других странах, согласно данным статьи, также показали, что вакцина «Спутник V» не приводит к образованию тромбов .
Репродуктивная безопасность. Исследования репродуктивной безопасности «Спутника V» были выполнены в России в Национальном медицинском исследовательском центре акушерства, гинекологии и перинатологии им. В. И. Кулакова группой учёных, независимой от разработчиков вакцины. Исследователи не обнаружили влияния вакцины на репродуктивное здоровье как мужчин , так и женщин .
6 мая 2021 года Министерство здравоохранения Российской Федерации зарегистрировало однокомпонентную вакцину «Спутник Лайт» (регистрационное удостоверение номер ЛП-006993 ). Вакцина «Спутник Лайт» ( англ. Sputnik Light ) — это первый компонент вакцины «Спутник V», он основан на векторе из рекомбинантного аденовируса человека 26-го серотипа (rAd26).
Согласно разработчикам вакцины, эффективность однокомпонентной вакцины «Спутник Лайт» составляет 79,4 % на основании анализа данных с 28 дня после получения иммунизации гражданами РФ в рамках программы массовой вакцинации в период 5 декабря 2020 года — 15 апреля 2021 года , а показатель эффективности на уровне около 80 % превышает показатели эффективности многих вакцин, требующих двукратного введения вакцины на курс вакцинации .
Согласно разработчикам вакцины, фаза I/II исследования безопасности и иммуногенности «Спутник Лайт» продемонстрировала следующие результаты:
25 июня 2021 года первые серии вакцины «Спутник Лайт» вышли из производства в гражданский оборот .
18 ноября 2021 года Минздрав России рекомендовал использовать «Спутник Лайт» для ревакцинации через полгода после первичной в условиях пандемии COVID-19, а также через 6 месяцев после перенесённого заболевания .
По состоянию на начало января 2022 года вакцина «Спутник Лайт» была зарегистрирована более чем в 30 странах мира .
24 ноября 2021 года Министерство здравоохранения Российской Федерации зарегистрировало вакцину от коронавируса «Спутник М» (регистрационное наименование — «Гам-КОВИД-Вак-М» , лат. Gam-COVID-Vac-M ) для подростков в возрасте от 12 до 17 лет . Буква «М» означает «для маленьких» .
Центр имени Гамалеи заявил, что вакцина сформировала клеточный иммунитет у 93,2 % добровольцев .
«Спутник М» представляет собой аналог вакцины «Спутник V», концентрация которой снижена в 5 раз . Прививка проводится двумя компонентами.
Подростков в возрасте до 15 лет прививают с согласия родителей, старше 15 лет при наличии их собственного письменного согласия .
Предполагалось, что в гражданский оборот вакцина «Спутник М» поступит в конце декабря 2021 года . Однако первые поставки вакцины поступили в регионы лишь в середине января 2022 года .
В начале 2021 года стало известно о ведении центром имени Гамалеи работ по созданию назальной формы вакцины Спутник V, которая будет представлять собой второй компонент оригинальной вакцины в виде спрея. По словам главы центра Гамалеи А. Л. Гинцбурга новая форма вакцины позволит сформировать дополнительный иммунитет, благодаря которому вакцинированные не будут распространять инфекцию, хотя и не сможет заменить инъекционную вакцину .
В феврале 2022 года Гинцбург сообщил, что испытания «Спутника V» в виде спрея проходят успешно, при этом срок испытаний могут сократить, чтобы быстрее ввести препарат в гражданский оборот. По мнению разработчиков вакцины, такая форма даёт меньше побочных эффектов .
На начало июля 2021 года выпуск «Спутника V» в России осуществлялся на 9 производственных площадках .
Кроме того, на конец апреля 2021 года РФПИ были заключены соглашения с 20 производителями вакцин в 10 странах мира .
4 июня производство вакцины началось в Сербии, которая стала первой европейской страной, которая начало производство российской вакцины в рамках программы вакцинации населения .
22 июля ряд южнокорейских компаний выступил с заявлением, что они получили все необходимые технические инструкции для производства российской вакцины и для начала её производства необходимо лишь получение разрешения на государственном уровне .
| Страна производства | Дата начала производства | Производитель | Примечания |
|---|---|---|---|
|
|
С 15 августа 2020 года |
«
Медгамал
» (НИЦЭМ им. Н. Ф. Гамалеи), г.
Москва
«Генериум» (АО «Фармстандарт»), п. Вольгинский , Владимирская обл. « Биннофарм » (АФК «Система»), г. Москва, г. Зеленоград « Биокад », Санкт-Петербург « Р-Фарм », г. Москва |
|
|
|
С 21 декабря 2020 года | Карагандинский фармацевтический комплекс (КФК), Караганда | |
|
|
С конца декабря 2020 года | Консорциум из 7 фарм. компаний во главе с «GL Rapha» (Hankook Korus), Чхунчхон | Масштабирование производства с апреля 2021 года |
|
|
С 15 января 2021 года | «Uniao Quimica» (запланировано на июнь 2021) | Серийный выпуск с мая 2021 года. Препарат будет направляться и в другие страны Латинской Америки . |
|
|
С 26 февраля 2021 года | РУП « Белмедпрепараты » | Серийный выпуск с 25 марта 2021 года |
|
|
С 20 апреля 2021 года | «Laboratorios Richmond» SACIF | Серийный выпуск с 4 июня 2021 года |
|
|
С 24 мая 2021 года |
«Hetero Biopharma»
«Virchow Biotech» (запланировано) «Stelis Biopharma» (запланировано) «Panacea Biotec», г. Бадди «Morepen Laboratories» |
Заключено соглашение о производстве более 300 млн доз вакцины в год . |
|
|
С 4 июня 2021 года | Институт вирусологии, вакцин и сывороток «Торлак» ( Белград ) | |
|
|
С 4 июня 2021 года | «Actoverco» | |
|
|
С 16 июня 2021 года | «Adienne Pharma & Biotech» | |
|
|
С 1 июля 2021 года | ||
|
|
С 5 июля 2021 года | «Laboratorios de Biol gicos y Reactivos de Mexico» («BIRMEX») | |
|
|
С 21 июля 2021 года | «Vabiotech» | |
|
|
С 30 июля 2021 года | «Jurabek laboratories», г. Алмалык | Серийный выпуск с 7 октября 2021 года . |
Зарубежные специалисты критиковали разработчиков «Гам-КОВИД-Вак» за отсутствие доказательств её эффективности и научных публикаций о проведённых испытаниях на момент презентации препарата . Соответствующая публикация результатов I и II фазы клинических нерандомизированных исследований вакцины была опубликована в медицинском журнале The Lancet 4 сентября 2020 года, спустя менее месяца после презентации . Согласно рецензии Lancet, главным результатом исследований было доказательство безопасности и иммуногенности вакцины , однако обнадёживающие итоги исследования ещё не говорят о том, что Гам-КОВИД-Вак готова ко всеобщему использованию .
Глава отделения лабораторной медицины Каролинского института Матти Сэльберг отмечает, что малое число участников клинического испытания, в котором были объединены первая и вторая фазы, не позволяет судить об отсутствии побочных эффектов при массовом применении вакцины , однако, сами разработчики вакцины считают её надёжной, поскольку она была разработана на существующей хорошо испытанной платформе . Также существуют опасения, что побочные эффекты от ранее широко не применявшихся живых вакцин на базе генноинженерных вирусов могут оставаться неизученными .
21 декабря 2020 года генеральный директор фармацевтической компании AstraZeneca Паскаль Сорио в ходе видеоконференции по случаю подписания соглашения о сотрудничестве с Центром им. Гамалеи, РФПИ и российской фармкомпанией « Р-Фарм » заявил: «Я хотел бы поздравить российских учёных из института Гамалеи, а также РФПИ с разработкой первой в мире вакцины против COVID-19, которая в последнее время продемонстрировала не только иммунный ответ, но и эффективность, защиту против госпитализации. И [регуляторное] одобрение, безусловно, стало важным этапом для этой вакцины» .
После публикации данных промежуточного этапа III фазы испытаний в журнале «Lancet» в западных СМИ начались публикации положительных отзывов о вакцине «Спутник V». Так, агентство Bloomberg назвало вакцину самым серьёзным научным прорывом России со времён Советского Союза . The Wall Street Journal указывает, что «„Спутник V“ представляет собой значительную победу президента России Владимира Путина в глобальной гонке вакцинаций, даёт вотум уверенности в возможностях российской науки и медицины и помогает отразить некоторую критику, с которой Москва столкнулась за быстрое развитие вакцинации и отсутствие опубликованных данных испытаний» . Радио Канада отмечает, что вакцина Спутник V завоевала доверие, а также стала крупной научной и дипломатической победой России . В медицинском журнале The Lancet появилась новая информация о сомнениях в эффективности препарата из-за недостаточности данных, переданных о третьей фазе клинических испытаний российской вакцины от коронавируса «Спутник V». Группа учёных детально проанализировала сведения о препарате и пришла к выводу, что «ограниченный доступ к данным подрывает доверие к исследованиям». Также, в представленных данных о препарате есть несоответствия, а полный протокол исследования так и не был опубликован и предоставлен институтом Гамалеи международному сообществу . В ответе за авторством разработчиков вакцины, опубликованном в The Lancet 12 мая 2021 года, отмечается, что нет никаких научных оснований сомневаться в эффективности вакцины, полученные данные обработаны и проанализированы в соответствии с протоколом исследований, а полученные в ходе реального применения вакцины в Аргентине данные полностью подтверждают её высокую безопасность и эффективность .
Австралийский учёный, лауреат Нобелевской премии по физиологии и медицине Дохерти, Питер отметил, что «эффективность вакцины „Спутник V“ в более чем 90 % выглядит великолепно, и к тому же Россия имеет долгую историю разработки хороших вакцин» .
Главный иммунолог США Энтони Фаучи заявил: «Если Россия или Китай имеют надёжные вакцины, то они могут обеспечить ими и себя, и некоторые другие страны. Это путь ко всеобщей защите всего человечества» .
Инфекционист медицинского центра при Стэнфордском университете Дин Уинслоу считает, что «Спутник V» сыграет важную роль в борьбе с пандемией в мире. Руководитель отделения инфекционных заболеваний при медицинском факультете Гарвадского университета Дэниел Курицкис заявил: «Из того, что я прочитал о вакцине, я понимаю, что её можно хранить при температуре, которую поддерживает обычный холодильник. Это, разумеется, большое преимущество, поскольку позволяет доставить вакцину в те страны, где гораздо меньше возможностей обеспечить хранение при сверхнизкой температуре. Это означает, что в некоторых странах её значительно проще применять». Инфекционист из Университета штата Джорджия в Огасте Роджер Макартур, говоря о том, что вакцина не требует поддержания сверхнизкой температуры при транспортировке, отметил: «Это, конечно, преимущество, в особенности в том, что касается её доставки в места, где вряд ли есть возможность достичь очень низкой температуры, но, думаю, в вакцине важнее всего эффективность и безопасность» .
7 июля 2021 года вирусолог, начальник лаборатории особо опасных инфекций ФИЦ Фундаментальной трансляционной медицины, профессор Александр Чепурнов сообщил, что считает «Спутник Лайт» наиболее подходящей вакциной для ревакцинации тех, кто ранее переболел коронавирусом .



2 декабря 2020 года состоялась презентация «Спутник V» в виртуальном формате для стран — членов ООН . Согласно данным ТАСС , в мероприятии зарегистрировались представители 55 государств, а также представители руководства ООН, ВОЗ , Красного Креста . При этом чуть ранее, в конце ноября, Российский фонд прямых инвестиций (РФПИ) объявил, что стоимость одной дозы вакцины «Спутник V» для международных рынков составит менее 10 $, что делает её гораздо более доступной в сравнении с мРНК-вакцинами других производителей .
По заявлениям генерального директора РФПИ Кирилла Дмитриева, на первую неделю декабря фонд получил предварительные заявки на покупку 1,2 млрд доз вакцины из более чем 50 стран . Также была подана заявка на одобрение вакцины в 40 странах . 2 февраля The Wall Street Journal отметил, что уже имеется заказов и предварительных договорённостей на 2,4 млрд доз вакцины «Спутник V» .
29 января 2021 года РФПИ подал заявку в Европейское агентство лекарственных средств (EMA) для регистрации российской вакцины в Евросоюзе . 10 февраля EMA сообщило, что они не получали заявку на непрерывный обзор или разрешение на продажу вакцины. Разработчики только выразили заинтересованность в том, чтобы вакцина рассматривалась для непрерывного обзора, но Комитет EMA по лекарственным средствам для человека (CHMP) и Целевая группа по пандемии COVID-19 EMA (COVID-ETF) должны сначала дать своё согласие, прежде чем разработчики смогут представить своё предложение для начала процесса проверки .
Согласно СМИ (французское издание Le Monde , Euronews и другие), применение вакцины «Спутник V» в Европе вызвало дискуссию о «глобальной вакцинной дипломатии» и способствовало расколу между лидерами стран, входящих в Евросоюз . В публикациях говорится, что Европейская комиссия пока не вступила в официальные переговоры с Российским фондом прямых инвестиций о поставках российской вакцины, но часть стран Европы, несмотря на это, намерены заказать её, при этом настаивая на скорейшем одобрении «Спутник V» в Евросоюзе, так как в приоритете должна быть забота о здоровье граждан, а не политика .
Первой страной, одобрившей использование «Спутника V», не дожидаясь решения Еврокомиссии, стала Венгрия . Лидеры Германии и Австрии также настаивали на одобрении вакцины и были готовы приобретать её, не дожидаясь официальных решений Еврокомиссии. Однако против применения российской вакцины выступил, например, французский министр иностранных дел Жан-Ив Ле Дриан . Член Еврокомиссии по вопросам внутреннего рынка, французский бизнесмен Тьерри Бретон выступил с заявлением о том, что закупка «Спутника V» не является нужной Евросоюзу . Франция также заявила, что призывает не признавать российские и китайские вакцины, и осудила Грецию за то что та допускает российских туристов, привитых в том числе «Спутником V» .
30 марта 2021 года стало известно о том, что Австрия приняла решение произвести закупку партии вакцины «Спутник V», несмотря на то, что препарат к тому моменту не успел пройти сертификацию в Европейском агентстве лекарственных средств. О намерении закупить миллион доз российской вакцины заявил австрийский канцлер Себастьян Курц . В ответ на принятое австрийским канцлером решение Еврокомиссия выступила с предупреждением к Австрии о том, что в таком случае вся ответственность за возможные риски ложится на правительство Австрии . Уже 10 апреля австрийский канцлер заявил, что переговоры о закупках «Спутник V» «фактически подошли к концу». «Закупка для нас возможна», — сказал он журналистам на брифинге, его цитирует Kurier. По его словам, речь идёт об 1 млн доз вакцины .
27 мая 2021 года руководство Детского фонда ООН ( ЮНИСЕФ ) и компания Human Vaccine подписали долгосрочное соглашение о поставках российской вакцины «Спутника V» для того, чтобы обеспечить нуждающиеся страны в доступе к вакцине от Covid-19 .
12 июня 2021 года министр иностранных дел Словакии Иван Корчок заявил об отказе республики закупать новые партии российской вакцины против коронавируса «Спутник V» после получения 1 марта первой партии препарата .
21 июля 2021 года Институт общественного здравоохранения Чили одобрил включение российской вакцины «Спутник V» в национальную программу вакцинации. На принятие положительного по интеграции российской вакцины повлияли материалы по вакцинации в Аргентине и Мексике, где «Спутник V» был использован ранее .
Директор службы внешней разведки России Сергей Нарышкин считает, что регистрация «Спутника V» в Европейском Союзе тянется «из-за сигналов, которые поступают из высоких кабинетов ЕС» .
На начало июля 2021 года, несмотря на отсутствие одобрения ВОЗ, «Спутник V» применялся в 69 странах мира
В сентябре 2021 года стало известно, что специалисты финского Национального института здравоохранения и социального развития считают возможным разрешить въезд в Финляндию людям, привитым российской вакциной .
В сентябре 2021 года власти Гонконга признали сертификат о вакцинации «Спутник V» . Теперь россияне смогут лететь в Гонконг напрямую, а не после трёхнедельного пребывания в третьем государстве. Но им предстоит сидеть на карантине 21 день в специализированной гостинице.
Международный союз биатлонистов (IBU) признал вакцину . Полностью вакцинированные освобождаются от любых обязательств по тестированию.
В середине сентября 2021 года ВОЗ приостановила сертификацию российской вакцины от COVID-19 «Спутник V», так как во время инспекции на одной из фабрик, которая составляет часть производства вакцины, было обнаружено, что эта фабрика не соответствует новым правилам наилучшей практики производства .
14 декабря 2021 пресс-секретарь Владимира Путина Дмитрий Песков заявил, что российские власти не предоставили Всемирной организации здравоохранения (ВОЗ) всей информации, необходимой для сертификации вакцины из-за разночтений в стандартах, но работа по прохождению процедуры одобрения ВОЗ продолжается .
Страны, зарегистрировавшие вакцину и начавшие вакцинацию Страны, зарегистрировавшие вакцину Страны Евросоюза, зарегистрировавшие вакцину, не дожидаясь одобрения EMA
|
|

|
|
|

|
В сентябре 2021 года в Эстонии заявили, что россияне будут освобождены от тестирования и изоляции в течение одного года после завершения вакцинации, если они полностью вакцинированы и достигли полной иммунной защиты . Привитым россиянам можно посещать общественные места Эстонии без ограничений.
Спортсмены, привитые российской вакциной, пользуются теми же правами на Олимпиаде в Китае, что и другие. По словам посла России в КНР, фактически получается, что страна признала нашу вакцину .
26 августа 2020 года 48-й Центральный научно-исследовательский институт Министерства обороны РФ , на базе которого проводились доклинические испытания на токсичность, безопасность, иммуногенность и защитную эффективность вакцины «Спутник V», был внесён в список организаций, деятельность которых противоречит интересам национальной безопасности или внешней политики США. Власти США заявили, что у них есть основания считать 48-й ЦНИИ и его филиалы связанными с программой создания биологического оружия .
7 сентября 2020 года профессор биологии американского университета Темпл , Энрико Буччи, на сайте Cattivi Scienziati, специализирующемся на борьбе с псевдонаукой, опубликовал открытое письмо , в котором поставил под сомнение достоверность данных клинических исследований фазы I/II, опубликованных в «The Lancet». Данное письмо было подписано тремя десятками учёных из США, Италии и других стран и было опубликовано во многих ведущих западных СМИ . В тот же день представитель РФПИ от имени Дениса Логунова передал следующее заявление: «НИЦЭМ им. Гамалеи категорически отвергает обвинения в недостоверности статистических данных, опубликованных в журнале The Lancet. Опубликованные данные являются достоверными и точными и прошли экспертизу у пяти рецензентов The Lancet, полноразмерный клинический протокол предоставлялся в редакцию журнала. Мы представили именно те данные, которые получили, а не те, которые должны нравиться итальянским экспертам» .
Позже, 18 сентября, в «The Lancet» был опубликован более подробный ответ разработчиков вакцины на критику. В ответе были даны ответы на вопросы учёных, в том числе было указано, что выявленные совпадения, особенно в близких к исходным и начальным значениям, были связаны с дискретностью данных (получаемые значения были не точными, а в виде диапазонов, что значительно увеличивает вероятность совпадений), а также с малым количеством участников в группах .
22 мая 2021 года профессор Энрико Буччи с коллегами опубликовал в «The Lancet» статью «Расхождения в данных и нестандартная отчётность по промежуточным данным исследования фазы III Спутник V», где раскритиковали авторов III фазы испытаний Спутник V за то, что они не предоставили критикам доступа к полным данным, а также за несоответствия и подозрительные совпадения в данных . Ответ авторов был опубликован в Lancet — они заявили, что ещё 5 ноября 2020 года регулирующим органам и рецензентам Lancet были предоставлены все необходимые данные, и что данных, включённых в статью, достаточно для того, чтобы читатели могли проверить сообщённую эффективность вакцины. Они также заявили, что числовые несоответствия были простыми ошибками или опечатками, которые были легко исправлены . Заслуженный врач РФ, сенатор Владимир Круглый указывал, что попытки дискредитации российской вакцины от коронавируса «Спутник V» — это элемент информационной войны и недобросовестной конкуренции [ значимость факта? ] .
1 марта 2021 года в Словакию была доставлена первая партия вакцины «Спутник V», состоящая из 200 тысяч доз. Всего, согласно договору, было запланировано поставить 2 млн доз . Вакцина была одобрена министром здравоохранения Словакии Мареком Крайчи . Таким образом, Словакия стала второй страной Евросоюза, которая одобрила применение российской вакцины «Спутник V», не дожидаясь решения европейского регулятора EMA.
На следующий день, 2 марта, президент Словакии Зузана Чапутова выразила недовольство решением премьер-министра страны Игора Матовича приобрести для использования в республике российскую вакцину. Она указала, что не будет пропагандировать использование препаратов, не прошедших процесс регистрации в Евросоюзе .
Покупка российской вакцины привела к разногласиям в правительстве. Многие члены правительства осудили премьер-министра, который проигнорировал февральское решение правительства, согласно которому в республике должны использоваться только препараты, зарегистрированные в Евросоюзе .
12 марта министр здравоохранения Словакии Марек Крайчи ради сохранения правительственной коалиции страны подал в отставку . Позже, 15 марта, в связи с правительственным кризисом, подал в отставку министр труда Милан Крайняк . 17 марта о своей отставке объявил министр экономики Рихард Сулик . 24 марта о своей отставке объявили министр иностранных дел Иван Корчок , министр образования Бронислав Грюлинг и министр юстиции Мария Коликова .
30 марта президент Словакии З. Чапутова приняла отставку премьер-министра И. Матовича и поручила сформировать новое правительство .
6 апреля словацкое издание «Dennik» сообщило, что словацкий Государственный институт по контролю лекарств (ŠÚKL), не выдал разрешение на использование вакцины «Спутник V». В сообщении отмечалось, что для одобрения вакцины не хватает дополнительных данных о доклинических и клинических испытаниях. «Значительная часть данных, примерно 80 %, не была предоставлена даже после повторных запросов». Указывалось также, что поставленная в республику вакцина отличается от образцов, результаты испытаний которых были опубликованы в научном журнале «The Lancet» .
7 апреля на официальном аккаунте Спутника в твиттер появилось сообщение, что вышеуказанная публикация является вбросом . Было отмечено, что «в нарушение существующего контракта и в акте саботажа Государственный институт по контролю за лекарствами обеспечил тестирование „Спутник V“ в лаборатории, не входящей в сеть официальных сертифицированных лабораторий ЕС по контролю за лекарствами, хотя такие лаборатории были доступны», а также что «все партии „Спутник V“ одинакового качества и проходят строгий контроль качества в Институте Гамалеи». Указывалось, что против российской вакцины ведётся кампания по дезинформации. РФПИ обратился к правительству Словакии с просьбой отправить вакцину в сертифицированную лабораторию ЕС для тестирования. 6 апреля 2021 года РФПИ потребовал вернуть вакцину из-за многочисленных нарушений контракта, чтобы её можно было использовать в других странах .
В ответ на это 15 апреля президент Словакии Зузана Чапутова потребовала опубликовать договор о покупке республикой российской вакцины «Спутник V» . Российская сторона отметила, что не против публикации договора о поставке «Спутника V» в Словакию, но в таком случае должен быть опубликован и контракт с Pfizer . 29 апреля Словакия опубликовала договор .
7 мая специализированная лаборатория в Венгрии подтвердила надёжность российской вакцины «Спутник V», поступившей в Словакию 1 марта . 7 июня в Словакии началось использование российской вакцины .
В начале 2021 года Министерство здравоохранения и социальных служб США опубликовало отчёт о проделанной работе. Как выяснилось из текста доклада, Министерство здравоохранения США вместе с другими правительственными организациями участвовало в кампании давления на бразильские власти с целью убедить отказаться от закупки вакцины «Спутник V» в России под предлогом, что Россия использует поставки вакцины якобы для «усиления своего влияния в регионе в ущерб безопасности США» .
26 апреля 2021 года Национальное агентство по санитарному надзору Бразилии Anvisa ( порт. Agência Nacional de Vigilância Sanitária ) не разрешила импорт и использование в стране российской вакцины «Спутник V». Согласно заявлению представителей Anvisa, причиной отказа были отсутствие последовательных и надёжных данных, а также наличие в вакцине аденовируса, способного к репликации . Таким образом, 14 штатов Бразилии, ожидавшие разрешения и запланировавшие срочный импорт вакцины для противостояния растущей волне инфекции COVID-19, получили отказ.
28 апреля команда «Спутника V» рассмотрела претензии, заявленные членами правления Anvisa, и продемонстрировала, что эти обвинения не имеют научных оснований и не могут серьёзно рассматриваться в научном сообществе и среди международных регулирующих органов. Представители центра имени Гамалеи заявили, что «ни в одной из производимых серий вакцины „Спутник V“ не было обнаружено воспроизводимых аденовирусов», а существующий контроль гарантирует, что в вакцине нет таких вирусов. В центре отметили, что качество и безопасность вакцины обеспечивается 4-ступенчатой технологией очистки. «В производстве вакцины „Спутник V“ используются только нереплицирующиеся аденовирусные векторы E1 и E3, которые безвредны для человеческого организма», подчеркнули специалисты. Команда Anvisa в Москве имела полный доступ ко всей необходимой документации, а также к исследовательским и производственным площадкам. Также учёные напомнили, что в ходе применения «Спутник V», «в отличие от других вакцин, случаев тромбоза венозного синуса головного мозга не было зарегистрировано» .
4 июня поздно вечером Anvisa одобрила импорт и ограниченное применение российской вакцины «Спутник V» .
Фальшивые сайты, продающие фальсифицированные препараты против COVID, и склады с поддельной вакциной были обнаружены в 2020—2021 годах в нескольких странах: Нигерии , Мексике , Китае и других. В марте 2021 года Организация экономического сотрудничества и развития опубликовала отчёт , в котором сообщалось, что в 2016 году мировая торговля поддельными лекарствами, по разным оценкам, составляет от 4,4 до 20 миллиардов долларов, что объясняется низкой ответственностью за продажу поддельных препаратов. Фальсифицированную вакцину предполагалось реализовывать под маркой известных препаратов американского, английского, китайского и российского производства . В марте 2021 года в аэропорту мексиканского города Кампече при обыске частного самолёта власти обнаружили и изъяли подготовленную к перевозке в Гондурас партию поддельной вакцины «Спутник V» (1155 флаконов, 5775 доз) в упаковке, имитирующей настоящую .
Примеры афер и способов заработка путём мошенничества с фальсифицированными вакцинами, зафиксированные за рубежом, опубликованы в СМИ . Генеральный секретарь Интерпола Юрген Шток считает, что фальсифицированная вакцина, найденная в Мехико и Южной Африке , лишь « верхушка айсберга » и, вероятно, в обращении находится много партий поддельных вакцин, которые пока не обнаружены , так как производство лекарств часто представляет собой глобальную сеть, когда разные этапы производственной цепочки выполняются в разных странах, и затем могут перепаковываться, чтобы снизить таможенные расходы, при этом есть много мест для введения подделок в схемы поставок. В 2021 году вакцины стали «жидким золотом», которое «приносит миллиарды», и рынок поддельных лекарств образует параллельную легальному рынку криминальную сеть с низкими рисками и большими доходами .
{{
cite news
}}
:
Проверьте значение даты:
|date=
(
справка
)
;
Внешняя ссылка в
|title=
(
справка
)
;
Проверьте значение
|url=
(
справка
)
{{
cite news
}}
:
Указан более чем один параметр
|author=
and
|last=
(
справка
)