The Call
- 1 year ago
- 0
- 0

Лёд — вода в твёрдом агрегатном состоянии .
Льдом иногда называют некоторые вещества в твёрдом агрегатном состоянии, которым свойственно иметь жидкую или газообразную форму при комнатной температуре; в частности, сухой лёд , аммиачный лёд или метановый лёд.
В настоящее время известны три аморфных разновидности и 17 кристаллических модификаций льда. Фазовая диаграмма на рисунке справа показывает, при каких температурах и давлениях существуют некоторые из этих модификаций (более полное описание).
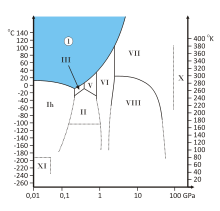
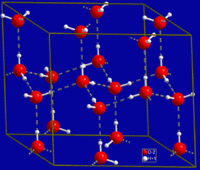
В природных условиях Земли вода образует кристаллы одной кристаллической модификации — гексагональной сингонии ( лёд I h ). Во льду I h каждая молекула Н 2 O окружена четырьмя ближайшими к ней молекулами, находящимися на одинаковых расстояниях от неё, равных 2,76 Å и размещённых в вершинах правильного тетраэдра .
Новые исследования формирования водяного льда на ровной поверхности меди при температурах от −173 °C до −133 °C показали, что сначала на поверхности возникают цепочки молекул шириной около 1 нм не гексагональной, а пентагональной структуры .
Ажурная кристаллическая структура такого льда приводит к тому, что его плотность , равная 916,7 кг/м³ при 0 °C, меньше плотности воды (999,8 кг/м³) при той же температуре. Поэтому вода, превращаясь в лёд, увеличивает свой объём примерно на 9 % . Лёд, будучи легче жидкой воды, образуется на поверхности водоёмов, что препятствует дальнейшему замерзанию воды.
Высокая удельная теплота плавления льда, равная 330 кДж /кг, (для сравнения — удельная теплотa плавления железа равна 270 кДж/кг), служит важным фактором в обороте тепла на Земле.
Лёд встречается в природе в виде собственно льда (материкового, плавающего,), а также в виде снега , инея , изморози . Под действием собственного веса лёд приобретает пластические свойства и текучесть.
Природный лёд обычно значительно чище, чем вода, так как при кристаллизации воды в первую очередь в решётку встают молекулы воды (см. зонная плавка ). Лёд может содержать — твёрдые частицы, капельки концентрированных растворов , пузырьки газа . Наличием кристалликов соли и капелек объясняется солоноватость морского льда.

Общие запасы льда на Земле около 30 млн км³. Основные запасы льда на Земле сосредоточены в полярных шапках (главным образом, в Антарктиде , где толщина слоя льда достигает 4 км).
Вода в мировом океане солёная и это препятствует образованию льда, поэтому лёд образуется только в полярных и субполярных широтах, где зима долгая и очень холодная. Замерзают некоторые неглубокие моря, расположенные в умеренном поясе. Различают однолетние и многолетние льды. Морской лёд может быть неподвижным, если связан с сушей, или плавучим, то есть дрейфующим. В океане встречаются льды, отколовшиеся от ледников суши и спустившиеся в океан в результате абляции — айсберги .
Имеются данные о наличии льда на планетах Солнечной системы (например, на Марсе ), их спутниках , на карликовых планетах и в ядрах комет .

Ледяная гидросмесь. В конце 1980-х годов американская лаборатория Аргонн разработала технологию изготовления ледяной гидросмеси (ice slurry), способной свободно течь по трубам различного диаметра, не собираясь в ледяные наросты, не слипаясь и не забивая системы охлаждения . Солёная водяная суспензия состояла из множества очень мелких ледяных кристалликов округлой формы. Благодаря этому сохраняется подвижность воды и, одновременно, с точки зрения теплотехники она представляет собой лёд, который в 5—7 раз эффективнее простой холодной воды в системах охлаждения зданий. Кроме того, такие смеси перспективны для медицины. Опыты на животных показали, что микрокристаллы смеси льда прекрасно проходят в довольно мелкие кровеносные сосуды и не повреждают клетки. «Ледяная кровь» удлиняет время, в течение которого можно спасти пострадавшего. Скажем, при остановке сердца это время удлиняется, по осторожным оценкам, с 10—15 до 30—45 минут . Использование льда в качестве конструкционного материала широко распространено в приполярных регионах для строительства жилищ — иглу . Лёд входит в состав предложенного материала пайкерит , из которого предлагалось сделать самый большой в мире авианосец . Использование льда для постройки искусственных островов описывается в фантастическом романе « Ледяной остров ».


| Фаза | Характеристики |
|---|---|
| Аморфный лёд | Аморфный лёд не обладает кристаллической структурой. Он существует в трёх формах: аморфный лёд низкой плотности (LDA), образующийся при атмосферном давлении и ниже, аморфный лёд высокой плотности (HDA) и аморфный лёд очень высокой плотности (VHDA), образующийся при высоких давлениях. Лёд LDA получают очень быстрым охлаждением жидкой воды («сверхохлаждённая стекловидная вода», HGW), или конденсацией водяного пара на очень холодной подложке («аморфная твёрдая вода», ASW), или путём нагрева высокоплотностных форм льда при нормальном давлении («LDA»). |
| Лёд I h | Обычный гексагональный кристаллический лёд. Почти весь лёд на Земле относится ко льду I h , и только очень малая часть — ко льду I c . |
| Лёд I c |
Метастабильный
кубический
кристаллический лёд. Атомы кислорода расположены как в
кристаллической решётке алмаза
.
Его получают при температуре в диапазоне от −133 °C до −123 °C, он остаётся устойчивым до −73 °C, а при дальнейшем нагреве переходит в лёд I h . Он изредка встречается в верхних слоях атмосферы . |
| Лёд II | Тригональный кристаллический лёд с высокоупорядоченной структурой. Образуется изо льда I h при сжатии и температурах от −83 °C до −63 °C. При нагреве он преобразуется в лёд III. |
| Лёд III | Тетрагональный кристаллический лёд, который возникает при охлаждении воды до −23 °C и давлении 300 МПа . Его плотность больше, чем у воды, но он наименее плотный из всех разновидностей льда в зоне высоких давлений. |
| Лёд IV | Метастабильный тригональный лёд. Его трудно получить без нуклеирующей затравки. |
| Лёд V | Моноклинный кристаллический лёд. Возникает при охлаждении воды до −20 °C и давлении 500 МПа. Обладает самой сложной структурой по сравнению со всеми другими модификациями. |
| Лёд VI | Тетрагональный кристаллический лёд. Образуется при охлаждении воды до −3 °C и давлении 1,1 ГПа. В нём проявляется . |
| Лёд VII | Кубическая модификация. Нарушено расположение атомов водорода; в веществе проявляется . Водородные связи образуют две взаимопроникающие решётки. |
| Лёд VIII | Более упорядоченный вариант льда VII, где атомы водорода занимают, очевидно, фиксированные положения. Образуется изо льда VII при его охлаждении ниже 5 °C. |
| Лёд IX | Тетрагональная метастабильная модификация. Постепенно образуется изо льда III при его охлаждении от −65 °C до −108 °C, стабилен при температуре ниже −133 °C и давлениях между 200 и 400 МПа. Его плотность 1,16 г/см³, то есть, несколько выше, чем у обычного льда. |
| Лёд X | Симметричный лёд с упорядоченным расположением протонов. Образуется при давлениях около 70 ГПа. |
| Лёд XI | Ромбическая низкотемпературная равновесная форма гексагонального льда. Является сегнетоэлектриком . |
| Лёд XII | Тетрагональная метастабильная плотная кристаллическая модификация. Наблюдается в фазовом пространстве льда V и льда VI. Можно получить нагреванием аморфного льда высокой плотности от −196 °C до примерно −90 °C и при давлении 810 МПа. |
| Лёд XIII | Моноклинная кристаллическая разновидность. Получается при охлаждении воды ниже −143 °C и давлении 500 МПа. Разновидность льда V с упорядоченным расположением протонов. |
| Лёд XIV | Ромбическая кристаллическая разновидность. Получается при температуре ниже −155 °C и давлении 1,2 ГПа. Разновидность льда XII с упорядоченным расположением протонов. |
| Лёд XV | Псевдоромбическая кристаллическая разновидность льда VI с упорядоченным расположением протонов. Можно получить путём медленного охлаждения льда VI примерно до −143 °C и давлении 0,8-1,5 ГПа . |
| Лёд XVI | Кристаллическая разновидность льда с наименьшей плотностью (0,81 г/см 3 ) среди всех экспериментально полученных . Имеет строение топологически эквивалентное полостной структуре КС-II ( англ. sII) газовых гидратов . |
| Кристаллическая разновидность льда с меньшей кристаллографической плотностью (0,85 г/см 3 ) , чем у других экспериментально полученных . Его структура, как и у льда XVI , сходна с клатратной структурой газовых гидратов . Получается при температуре 280 К и давлении ~ 400 МПа . Его номинальный состав (Н 2 О) 2 Н 2 с тремя формульными единицами на элементарную ячейку. | |
| Лёд XVIII | Лёд XVIII, так же известный как "суперионная вода", представляет собой фазу воды, которая существует при чрезвычайно высоких температурах и давлениях при которых молекулы воды распадаются на ионы кислорода и водорода. Ионы кислорода кристаллизуются и формируют равномерно распределённую решётку, а ионы водорода свободно плавают по образовавшейся решётке из кислорода. |
| Лёд XIX это вторая упорядоченная форма льда VI, которая возникает при медленном охлаждении воды до температуры 100 К при давлении около 2 ГПа . |







