Jus sanguinis
- 1 year ago
- 0
- 0
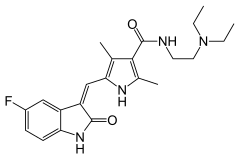
Сунитини́б — противоопухолевое средство , низкомолекулярный ингибитор различных (более 80) тирозинкиназ , участвующих в процессах роста опухолей, патологического ангиогенеза и образования метастазов .
Применяется для лечения почечно-клеточного рака , резистентных гастроинтестинальных стромальных опухолей и тяжёлых случаев рака поджелудочной железы .
В качестве средства, применяемого при терапии почечно-клеточного рака и гастроинтестинальных стромальных опухолей, сунитиниб был зарегистрирован в США в январе 2006 года (одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов , FDA ) . В России зарегистрирован для лечения больных раком почки в августе 2007 года , а в 2012 году включён в Перечень ЖНВЛП .
Сунитиниб составляет основу противоопухолевого препарата , выпускаемого под торговым названием Сутент ( Sutent ) фармацевтической компанией Pfizer, Inc. (США) и предназначенного для перорального приёма. Лекарственная форма — желатиновые капсулы; в роли действующего вещества выступает малат сунитиниба .
Основной мишенью сунитиниба являются α- и β-рецепторы тромбоцитарного фактора роста ( PDGFR ) . Кроме того, он угнетает:
Сунитиниб применяется перорально в форме малата , в желатиновых капсулах, независимо от приёма пищи . После приёма препарата максимальная концентрация сунитиниба в плазме крови достигается примерно через 6—12 часов после приёма; приём пищи на биодоступность сунитиниба не влияет. Равновесные концентрации сунитиниба и его основного метаболита в плазме крови достигаются через 10—14 дней после начала приёма препарата. Связь сунитиниба и его метаболита с белками плазмы — 95 и 90 % соответственно .
Метаболизм сунитиниба происходит в основном в печени — за счёт окисления, опосредуемого изоферментом CYP3A4 , в результате чего происходит образование основного активного метаболита (который дальше метаболизируется тем же изоферментом CYP3A4 ). Активность основного метаболита сходна с активностью самого сунитиниба. Доля циркулирующего в плазме активного метаболита составляет 23—37 % от величины площади под кривой «концентрация-время» .
Сунитиниб имеет период полувыведения 40—60 часов, его основной активный метаболит — 80—110 часов; выводится из организма преимущественно вместе с калом (60 %) .
Сунитиниб показан при :
Ниже приводится перечень (неполный) основных нежелательных явлений, выявленных при применении сунитиба . В зависимости от их характера и степени выраженности принимает решение: о продолжении лечения данным препаратом с использованием стандартной либо сниженной дозировки (и применением — при необходимости — местной симптоматической терапии); о приостановке приёма препарата на 7 или более дней; о прекращении терапии сунитинибом.
| Перечень побочных эффектов |
|---|
| В перечне упоминание каждого из данных нежелательных побочных эффектов сопровождается: пометкой «очень часто» — если частота возникновения эффекта больше 10 %; пометкой «часто» — если она лежит в пределах от 1 до 10 %; пометкой «нечасто» — если она лежит в пределах от 0,1 до 1 %. |
|
Основным противопоказанием является повышенная чувствительность к сунитинибу. Препарат не должны применять беременные женщины, поскольку для плода препарат потенциально опасен, обладая тератогенным действием и (в экспериментах на животных выявлена способность сунитиниба вызывать пороки развития ). Не установлены эффективность и безопасность применения препарата для детей и кормящих матерей. Следует проявлять осторожность пациентам с артериальной гипертензией , кожными заболеваниями, наличием кровотечений в анамнезе, заболеваниями сердца, при почечной или печёночной недостаточности .
Рекомендуется избегать одновременного приёма препарата с потенциальными ингибиторами изофермента CYP3A4 ( кетоконазол , ритонавир , итраконазол , эритромицин , кларитромицин , грейпфрутовый сок), способными повышать концентрацию сунитиниба в плазме крови ; если этого сделать нельзя, может потребоваться уменьшение суточной дозы. Рекомендуется также избегать одновременного приёма с потенциальными индукторами изофермента CYP3A4 ( рифампицин , дексаметазон , фенитоин , карбамазепин , фенобарбитал , зверобой продырявленный ), способными понижать концентрацию сунитиниба в плазме крови ; если этого сделать нельзя, может потребоваться поэтапное увеличение суточной дозы с тщательным мониторингом его переносимости .
Сунитиниб проявил себя — наряду с сорафенибом — как одно из наиболее многообещающих средств таргетной терапии почечно-клеточного рака . Эффективность данного средства изучалась, в частности, в двух исследованиях II фазы соответственно у 63 и 105 пациентов с метастатическим раком почки, которые не получили до этого положительного эффекта от терапии цитокинами . Частота частичных регрессий в данных исследованиях составила 40—43 %, стабилизации более чем на 3 месяца — 22—27 %. В исследованиях III фазы было показано, что применение сунитиниба приводило к более длительной безрецидивной выживаемости больных, чем терапия интерфероном-альфа .
Токсичность сунитиниба расценивается как умеренно выраженная; в то же время вопрос о профилактике и эффективной терапии токсических проявлений при терапии данным средством стоит весьма остро, поскольку (в отличие от рутинной терапии цитостатическими препаратами , которая осуществляется в ограниченные отрезки времени) лечение сунитинибом (и другими ингибиторами тирозинкиназ) носит непрерывный и длительный характер и продолжается иногда несколько лет. В этих условиях для врача весьма важны знание побочных эффектов применения сунитиниба, способов их профилактики и лечения, возможностей изменения дозы и режима назначения препарата, что позволяет минимизировать потребность в вынужденных перерывах таргетной терапии (чреватых бурным прогрессированием заболевания) .