Аденозинтрифосфатазы
- 1 year ago
- 0
- 0
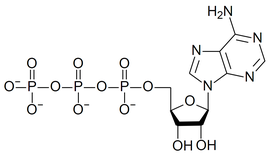

Аденозинтрифосфа́т (ион), Аденозинтрифосфорная кислота , АТФ ( англ. АТР ) — нуклеозидтрифосфат , играющий основную роль в обмене энергии в клетках живых организмов. Это универсальный источник энергии для всех биохимических процессов, протекающих в живых системах .
Хотя в биохимических процессах используются и другие фосфорилированные нуклеотиды с запасом энергии в молекуле, только АТФ является универсальной молекулой для всех процессов накопления и использования энергии в клетках .
Аденозинтрифосфорная кислота была выделена в 1929 году группой немецких учёных Карлом Ломаном , и Йеллапрагадой Суббарао .
В 1941 году Фриц Липман показал, что АТФ является основным переносчиком энергии в клетке .
В 2018–2022 годах группа биохимиков под руководством британского учёного Ника Лейна ( англ. Nick Lane ) выяснила, что синтез АТФ из аденозиндифосфата (АДФ) и ацетилфосфата возможен в предбиологических условиях, в которых синтезируется и сам ацетилфосфат, причём это единственная «энергетическая» молекула биохимических процессов, синтез которой не требует ферментов .
АТФ состоит из аденина , присоединенного 9-атомом азота к 1'-атому углерода сахара ( рибозы ), который, в свою очередь, присоединен к 5'-атому углерода сахара к трифосфатной группе . Во многих реакциях, связанных с метаболизмом, адениновые и сахарные группы остаются неизменными, но трифосфат превращается в ди- и монофосфат, давая соответственно производные АДФ и АМФ . Три фосфорильные группы помечены как альфа (α), бета (β) и, для концевого фосфата, гамма (γ).
В нейтральном растворе ионизированный АТФ существует в основном в виде ATP 4− , с небольшой долей ATP 3− .
Будучи полианионной и содержащей потенциально хелатирующую полифосфатную группу, АТФ связывает катионы металлов с высоким сродством. Константа связывания для Mg 2+ равна (9 554) . Связывание двухвалентного катиона, почти всегда магния, сильно влияет на взаимодействие АТФ с различными белками. Из-за силы взаимодействия АТФ-Mg 2+ АТФ существует в клетке в основном в виде комплекса с Mg 2+ , связанного с фосфатно-кислородными центрами .
Второй ион магния имеет решающее значение для связывания АТФ в домене киназы . Присутствие Mg 2+ регулирует активность киназы .
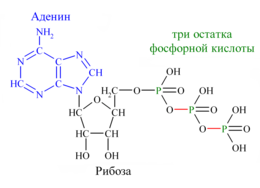
Систематическое наименование АТФ:
Химически АТФ представляет собой трифосфорный эфир аденозина, который является производным аденина и рибозы .
Пуриновое азотистое основание — аденин — соединяется β-N-гликозидной связью с 1'-углеродом рибозы. К 5'-углероду рибозы последовательно присоединяются три молекулы фосфорной кислоты , обозначаемые соответственно буквами: α, β и γ.
АТФ относится к так называемым макроэргическим соединениям , то есть к химическим соединениям, содержащим связи, при гидролизе которых происходит освобождение значительного количества энергии. Гидролиз макроэргических связей молекулы АТФ, сопровождаемый отщеплением 1 или 2 остатков фосфорной кислоты, приводит к выделению, по различным данным, от 40 до 60 кДж/моль .
Высвобождённая энергия используется в разнообразных процессах, протекающих с затратой энергии.
Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов. Всё это реакции синтеза сложных веществ в организме: осуществление активного переноса молекул через биологические мембраны , в том числе и для создания трансмембранного электрического потенциала; осуществления мышечного сокращения .
Помимо энергетической, АТФ выполняет в организме ещё ряд других не менее важных функций:
В организме АТФ синтезируется путём фосфорилирования АДФ :
Фосфорилирование АДФ возможно тремя способами:
В первых двух способах используется энергия окисляющихся веществ. Основная масса АТФ образуется на мембранах митохондрий в ходе окислительного фосфорилирования H-зависимой АТФ-синтазой . Субстратное фосфорилирование АДФ не требует участия мембранных ферментов, оно происходит в цитоплазме в процессе гликолиза или путём переноса фосфатной группы с других макроэргических соединений .
Одно из таких соединений — ацетилфосфат. При синтезе АТФ из АДФ и ацетилфосфата фосфорильную группу из ацетилфосфата на АДФ переносит фермент ацетаткиназа .
Реакции фосфорилирования АДФ и последующего использования АТФ в качестве источника энергии образуют циклический процесс, составляющий суть энергетического обмена .
В организме АТФ является одним из самых часто обновляемых веществ; так, у человека продолжительность жизни одной молекулы АТФ менее 1 мин. В течение суток одна молекула АТФ проходит в среднем 2000—3000 циклов ресинтеза (человеческий организм синтезирует около 40 кг АТФ в день, но содержит в каждый конкретный момент примерно 250 г), то есть запаса АТФ в организме практически не создаётся, и для нормальной жизнедеятельности необходимо постоянно синтезировать новые молекулы АТФ.
Вне организма синтез АТФ из ацетилфосфата через АДФ идёт в кислой среде в присутствии ионов трёхвалентного железа, которое в реакции работает катализатором, и такая реакция, вероятно, происходила на древней Земле в предбиологическое время .
Каталитическое действие трёхвалентного железа в реакции
ацетилфосфат + АДФ → АТФ
состоит в том, что Fe
3+
связывается с атомом азота N
7
пуринового кольца АДФ, одновременно «подтягивая» к нему ацетилфосфат (уменьшает силу отталкивания между молекулами)
.
|
Для улучшения этой статьи
желательно
:
|