Красная ртуть
- 1 year ago
- 0
- 0

| 80 |
Ртуть
|
|
|
|
| 4f 14 5d 10 6s 2 | |
Ртуть ( Hg , от лат. Hydrargyrum) — элемент шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 80, относящийся к подгруппе цинка , 12-й группе (по устаревшей классификации — побочной подгруппе II группы). Простое вещество ртуть — переходный металл , при комнатной температуре представляющий собой тяжёлую серебристо-белую жидкость , пары которой чрезвычайно ядовиты , контаминант . Ртуть — один из двух химических элементов (и единственный металл ), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй такой элемент — бром ).
Ртуть — один из семи металлов, известных с древнейших времён. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом её основного минерала — киновари . Киноварная краска применялась на территории современной Турции с 8 тыс. лет до н. э., киноварные месторождения юго-восточных провинций современного Китая разрабатывались с 4 тыс. лет до н. э. В древнем Египте киноварь и металлическую ртуть использовали с 3-го тысячелетия до н. э., в древней Индии — с 1—2 тысячелетий до н. э. В Египте был найден сосуд с ртутью, датированный XV−XVI веками до н. э. В Египте, Месопотамии и Китае был известен способ получения ртути из киновари при помощи меди и уксуса. В VII веке до н. э. ассирийские ремесленники применяли ртуть для золочения металлических поверхностей ( амальгамирование ). Aмальгамирование было известно древним грекам и римлянам, они знали и о токсичности самой ртути и её соединений, в частности сулемы . Ртуть и киноварь упоминаются в «Естественной истории» Плиния Старшего .
В надписях во дворце древнеперсидских царей Ахеменидов (VI—IV века до н. э.) в Сузах упоминается, что ртутную киноварь доставляли сюда с Зеравшанских гор и использовали в качестве краски .
На протяжении многих столетий в Европе основным и единственным месторождением ртути был Альмаден в Испании [ источник не указан 3554 дня ] . В Новое время с ним стала конкурировать Идрия во владениях Габсбургов (современная Словения ). Там же появилась первая лечебница для поражённых отравлением парами ртути рудокопов.
С XV века ртуть применялась в качестве лекарственного средства, в 1530 году её медицинское применение описал Парацельс . С XVI века ртуть применялась в Мексике для извлечения серебра из руды, а извлечение золота ртутью известно издревле .
Составной частью всех металлов ртуть стал считать арабский алхимик Джабир (Гебер) в IX веке . Алхимики вслед полагали, что если жидкой ртути возвратить твёрдость при помощи серы или мышьяка , то получится золото . Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 году. Для представления элемента как у алхимиков, так и в настоящее время используется символ планеты Меркурий : название планеты алхимиками широко использовалось метонимией ртути (иногда как двойной меркурий ). Твёрдая ртуть впервые была получена российскими учеными Ломоносовым и Брауном , которые 24 декабря 1759 года благодаря державшимся две недели сорокаградусным морозам смогли заморозить ртуть и установить её металлические свойства в твёрдом состоянии: ковкость, электропроводность и др.; было показано, что ртуть и в жидком, и в твёрдом состоянии проводит электрический ток .
Русское название ртути происходит от праслав. *rьtǫtь , связанного с лит. rìsti «катиться» .
В 350 году Аристотель назвал ртуть «жидким серебром» (хютос аргюрон), в I веке н. э. Диоскорид называет её «серебряной водой» (хюдраргюрон). Латинское название впервые встречается у Плиния , и химический знак Hg происходит от него .
Из-за легкоподвижности капелек ртути на гладкой поверхности алхимики называли её меркурием в честь греко-римского бога Гермеса (Меркурия) — быстро перемещающегося вестника богов .
Ртуть — относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами . Основная форма нахождения ртути в природе — рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути — 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации . Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — (HgSe) и (смесь тиманита и сфалерита ).
Ртуть является одним из наиболее чувствительных индикаторов скрытого оруденения не только ртутных, но и различных сульфидных месторождений, поэтому ореолы ртути обычно выявляются над всеми скрытыми сульфидными залежами и вдоль дорудных разрывных нарушений. Эта особенность, а также незначительное содержание ртути в породах, объясняются высокой упругостью паров ртути, возрастающей с увеличением температуры и определяющей высокую миграцию этого элемента в газовой фазе.

В обычных условиях киноварь и металлическая ртуть не растворимы в воде, но в присутствии некоторых веществ (Fe 2 (SO 4 ) 3 , озон, пероксид водорода) растворимость в воде этих минералов достигает десятков мг/л. Особенно хорошо растворяется ртуть в сульфидах щелочных металлов с образованием, например, комплекса HgS•nNa 2 S. Ртуть легко сорбируется глинами, гидроксидами железа и марганца, глинистыми сланцами и углями .
В природе известно около 20 минералов ртути, но главное промышленное значение имеет киноварь HgS (86,2 % Hg). В редких случаях предметом добычи является самородная ртуть, метациннабарит HgS и блёклая руда — шватцит (до 17 % Hg). На единственном месторождении Гуитцуко (Мексика) главным рудным минералом является ливингстонит HgSb 4 S 7 . В зоне окисления ртутных месторождений образуются вторичные минералы ртути. К ним относятся, прежде всего, самородная ртуть, реже метациннабарит, отличающиеся от таких же первичных минералов большей чистотой состава. Относительно распространена каломель Hg 2 Cl 2 . На месторождении Терлингуа (Техас) распространены и другие гипергенные галоидные соединения — терлингуаит Hg 2 ClO, Hg 6 Cl 4 O (по другим данным Hg 6 OCl 3 (OH) , Hg 6 HCl 3 O 2 ).

Ртуть считается редким металлом. Среднее содержание в земной коре — 0,08 миллионной доли , но в рудных месторождениях ртуть уже сконцентрирована в десятки тысяч раз: наибольшее содержание доходит до 2,5 %, 0,1 % руды считаются бедными . Часто ртутные месторождения связаны с вулканической активностью .
Одно из крупнейших в мире ртутных месторождений находится в Испании ( Альмаден ), которое наряду с рудниками Словении (Идрия), Италии, США и Мексике было закрыто из-за выработки или падения цен на ртуть. Цены на ртуть были весьма волатильны, в 2006 году они составляли $650 за стандартную в индустрии упаковку 76 фунтов (34 кг) . В 2012 году ЮНЕСКО объявило промышленную инфраструктуру Альмадена и Идрии памятником Всемирного наследия человечества .
Китай является крупнейшим в мире производителем ртути, на долю него в 2012 году приходилось более 72 % мирового объёма производства. Другими крупнейшими производителями ртути являются Кыргызстан , Чили , Россия и Перу . Наибольшими запасами ртути располагает Мексика .
В Российской Империи добыча киновари в незначительных количествах начата в 1759 году на Ильдикайском месторождении в Забайкалье . В небольших количествах россыпная киноварь добывалась в Приамурье. В XIX веке разрабатывались месторождения Бирксуйского рудного поля (Южная Фергана ) и Хпека (Южный Дагестан ). В 1887 году вступило в строй Никитовское ртутное месторождение (на Украине), где до 1908 года годовое производство варьировалось в пределах 47,3-615,9 тонн, существенная часть ртути шла на экспорт. К XXI веку добыча руды и производство первичной ртути на Никитовском месторождении прекратились .
К XXI веку в России, согласно Государственному балансу запасов полезных ископаемых, есть 24 месторождения ртутных руд низкого качества, в большинстве своём киноварных с запасами не более 2 тыс. тонн ртути. Четыре сравнительно крупных месторождения — Тамватнейское (14 тыс. т), Западнопалянское (10,1 тыс. т), Чаган-Узунское (14 тыс. т), «Звездочка» (3 тыс. т) . Единственное российское предприятие по производству ртути находится в Акташе ( Республика Алтай ) [ источник не указан 140 дней ]
В бывшем СССР наибольшее производство ртути — в Киргизии ( Хайдаркан — Айдаркен), с десятикратным отставанием за ней следует Таджикистан . Незначительные количества ртути получают попутно с цинком в Казахстане .

До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограммов на 1 кубический дециметр льда. Природные источники, такие как вулканы , составляют примерно половину всех выбросов атмосферной ртути. Причиной появления остальной половины является деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля (главным образом в тепловых электростанциях ) — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6,8 %, производство цемента — 6,4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1,4 %, ртути (в основном для батареек) — 1,1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1950-е годы , что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата .
Природная ртуть состоит из смеси 7 стабильных изотопов: 196 Hg (распространённость 0,155 %), 198 Hg (10,04 %), 199 Hg (16,94 %), 200 Hg (23,14 %), 201 Hg (13,17 %), 202 Hg (29,74 %), 204 Hg (6,82 %) . Искусственным путём получены радиоактивные изотопы ртути с массовыми числами 171—210 . Из них наиболее устойчива ртуть-194 (период полураспада 444 года).
Прочие радиоактивные изотопы имеют период полураспада менее года.
Ртуть получают обжигом киновари ( сульфида ртути(II) ) на воздухе :
Метод основан на неустойчивости оксида ртути (II), который при нагревании разлагается. Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности .
Полученная ртуть очень загрязнена. Сначала её фильтрованием через отверстие избавляют от механических примесей, затем мелкими каплями пропускают сквозь колонку, заполненную азотной кислотой, высушивают концентрированной серной кислотой и перегоняют в вакууме .


Электронная оболочка атома ртути обладает заполненными электронными подуровнями, последние из которых — 4f 14 5d 10 6s 2 . Главное отличие ртути от двух других металлов с аналогичной структурой электронного облака, цинка (3d 4s) и кадмия (4d 5s) — заполненность f-подуровня, находящегося по энергии ниже 6s-подуровня. Орбитали f-электронов имеют сложную форму и большой размер, они плохо экранируют заряд ядра. Поэтому удерживающие силы, действующие на 6s-электроны, относительно велики, и 6s-подуровень намного более стабилен, чем у любых других металлов. Этим обусловлены уникальные физические и химические свойства ртути. Так, ртуть — единственный металл, который находится в жидком состоянии при комнатной температуре. Температура плавления составляет 234,32 K (−38,83 °C) , кипит при 629,88 K (356,73 °C) , критическая точка — 1750 K (1477 °C), 152 МПа (1500 атм). Обладает свойствами диамагнетика . Образует со многими металлами жидкие и твёрдые сплавы — амальгамы . Стойкие к амальгамированию металлы: V , Fe , Mo , Cs , Nb , Ta , W , Co .
Плотность ртути при нормальных условиях — 13 596 кг/м 3 .
| t , °С |
ρ, г/см
3
(10 3 кг/м 3 ) |
t , °С |
ρ, г/см
3
(10 3 кг/м 3 ) |
|---|---|---|---|
| 0 | 13,5950 | 50 | 13,4725 |
| 5 | 13,5827 | 55 | 13,4601 |
| 10 | 13,5704 | 60 | 13,4480 |
| 15 | 13,5580 | 65 | 13,4358 |
| 20 | 13,5457 | 70 | 13,4237 |
| 25 | 13,5335 | 75 | 13,4116 |
| 30 | 13,5212 | 80 | 13,3995 |
| 35 | 13,5090 | 90 | 13,3753 |
| 40 | 13,4967 | 100 | 13,3514 |
| 45 | 13,4845 | 300 | 12,875 |
| t , °C | P , мм рт. ст. | t , °C | P , мм рт. ст. | t , °C | P , мм рт. ст. | t , °C | P , мм рт. ст. |
|---|---|---|---|---|---|---|---|
| −89 | 10 −10 | −42 | 10 −6 | 46 | 10 −2 | 254 | 100 |
| −79 | 10 −9 | −25 | 10 −5 | 82 | 10 −1 | 357 | 760 |
| −68 | 10 −8 | −6 | 10 −4 | 125 | 1,0 | ||
| −55 | 10 −7 | 17 | 10 −3 | 202 | 10 |
Почти все соединения ртути, кроме киновари, в большей или меньшей степени летучи .
Растиранием с жиром получают серую ртутную мазь , длительным встряхиванием — очень мелкие капельки, похожие на чёрный порошок .
| Степень окисления | Оксид | Гидроксид | Характер | Примечания |
|---|---|---|---|---|
| +1 | Hg 2 O | ⟨Hg 2 (OH) 2 ⟩ | Слабоосновный | Склонность к диспропорционированию . Гидроксид не получен, существуют только соответствующие соли. |
| +2 | HgO | ⟨Hg(OH) 2 ⟩ | Очень слабое основание, иногда — амфотерный | Гидроксид существует только в очень разбавленных (<10 −4 моль/л) растворах. |
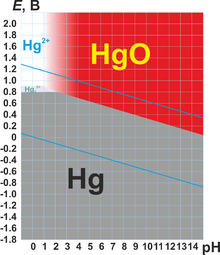
Для ртути характерны две степени окисления: +1 и +2. В степени окисления +1 ртуть представляет собой двухъядерный катион Hg 2 2+ с ковалентной связью металл — металл. Ртуть — один из немногих металлов, способных формировать такие катионы, и у ртути они — самые устойчивые.
В степени окисления +1 ртуть склонна к диспропорционированию. При нагревании, подщелачивании среды общая электронная пара остаётся у одного атома — происходит диспропорционирование :
подщелачивании:
добавлении лигандов, стабилизирующих степень окисления ртути +2.
Из-за диспропорционирования и гидролиза гидроксид ртути (I) получить не удаётся.
На холоде ртуть +2 и металлическая ртуть, наоборот, конпропорционируют . Поэтому, в частности, при реакции нитрата ртути (II) со ртутью получается нитрат ртути (I) :
В степени окисления +2 ртуть образует катионы Hg 2+ , которые очень легко гидролизуются. При этом гидроксид ртути Hg(OH) 2 существует только в очень разбавленных (<10 −4 моль/л) растворах. В более концентрированных растворах он дегидратируется:
В очень концентрированной щёлочи оксид ртути частично растворяется с образованием гидроксокомплекса:
Ртуть в степени окисления +2 образует уникально прочные комплексы со многими лигандами, причём как жёсткими, так и мягкими по теории ЖМКО . С иодом (−1), серой (−2) и углеродом она образует очень прочные ковалентные связи. По устойчивости связей металл — углерод ртути нет равных среди других металлов, поэтому получено огромное количество ртутьорганических соединений .
Из элементов группы 12 именно у ртути появляется возможность разрушения очень устойчивой электронной оболочки 6d 10 , что приводит к возможности существования соединений ртути(IV), но они крайне малоустойчивы, поэтому эту степень окисления скорее можно отнести к курьёзной, чем к характерной. В частности, сообщалось, что при взаимодействии атомов ртути и смеси неона и фтора при температуре 4 К получен HgF 4 . Однако более новые исследования не подтвердили его существование .
Ртуть — малоактивный металл . В сухом воздухе не изменяется .
При нагревании до 300 °C ртуть вступает в реакцию с кислородом :
При этом образуется оксид ртути(II) красного цвета. Эта реакция обратима: при нагревании выше 340 °C оксид разлагается до простых веществ:
Реакция разложения оксида ртути исторически является одним из первых способов получения кислорода.
При нагревании ртути с серой образуется сульфид ртути(II) :
С хлором реагирует при комнатной температуре достаточно энергично :
Ртуть также реагирует с другими галогенами (причём на холоде — медленно). [ источник не указан 350 дней ]
С одноатомным водородом при температуре жидкого азота образуется соединение , разлагающееся выше −100 °C .
В электрохимическом ряду ртуть стоит близ благородных металлов и вытесняет их из растворов солей. Сама ртуть вытесняется даже медью .
В ряду Бекетова ртуть стоит правее водорода, поэтому она не взаимодействует с кислотами с вытеснением водорода и не растворяется в растворах кислот, не обладающих окислительными свойствами (например, разбавленной серной или соляной) , но растворяется в царской водке :
При растворении в разбавленной азотной кислоте на холоде образуется нитрат диртути Hg 2 (NO 3) 2 и смесь окислов азота :
в при растворении в горячей и концентрированной азотной кислоте образуется нитрат ртути (II) :
На холоде ртуть под слоем серной кислоты хранится месяцами, взаимодействует с нею только при нагревании, с образованием сульфата ртути (II) :
При растворении ртути в концентрированной хлорной кислоте образуется растворимый перхлорат [ источник не указан 232 дня ] .
Со щелочами ртуть не взаимодействует .
Ртуть можно окислить также щелочным раствором перманганата калия :
и различными хлорсодержащими отбеливателями. Эти реакции используют для удаления металлической ртути .
Амальгамы (от греч. «малагма» — мягкое тело, по-русски сортучки, сортутки) — растворы металлов в ртути. На кривых плавкости систем металл-ртуть находят определённые химические соединения . Например, в амальгамах калия найдено 5: , в амальгамах натрия — 6: . Нагревание амальгам натрия и калия оставляет пирофорные кристаллы соответственно. Водой амальгамы натрия и калия разлагаются медленно .
В ртути легко растворяются золото, серебро и медь, что является основанием одного из методов добычи серебра и золота. Также амальгама золота при нагревании испаряет ртуть, оставляя огневую позолоту . Амальгама олова использовалась для изготовления зеркал .
В целом растворимость металлов в ртути при движении вниз по группам периодической системы возрастает . Весьма малорастворимы в ртути железо и никель (0,0007 и 0,00014) .
В связи с высокой токсичностью ртуть почти полностью вытеснена из медицинских препаратов. Её соединения (в частности, мертиолят ) иногда используются в малых количествах как консервант для вакцин . Сама ртуть сохраняется в ртутных медицинских термометрах (один медицинский термометр содержит до 2 г ртути).
Однако вплоть до 1960-х годов соединения ртути использовались в медицине очень активно :
При завороте кишок больному вливали в желудок стакан ртути. По мнению древних врачевателей, предлагавших такой метод лечения, ртуть благодаря своей тяжести и подвижности должна была пройти по кишечнику и под своим весом расправить его перекрутившиеся части .

Препараты ртути применяли с XVI века (в СССР — вплоть до 1963 года, в США — до конца 1970-х годов) для лечения сифилиса . Это было обусловлено тем, что бледная трепонема , вызывающая сифилис, обладает высокой чувствительностью к органическим и неорганическим соединениям, блокирующим сульфгидрильные группы тиоловых ферментов — соединениям ртути, мышьяка , висмута и иода . Однако такое лечение было недостаточно эффективно и весьма токсично для организма больного, приводя к полному выпадению волос и высокому риску развития серьёзных осложнений; причём возможности повышения дозы препаратов ртути или мышьяка при недостаточной противосифилитической активности стандартных доз ограничивались именно токсичностью для организма больного . Также применялись методики общей меркуризации организма, при которой больной помещался в нагревающуюся ёмкость, куда подавались пары ртути. Данная методика, хотя и была относительно эффективна, несла риск смертельного отравления ртутью, что привело к вытеснению её из клинической практики.
Амальгаму серебра применяют в стоматологии в качестве материала зубных пломб . Но после появления светоотверждаемых материалов это применение стало редким.
Радиоактивный изотоп ртуть-203 ( T 1/2 = 53 с ) используется в [ источник не указан 3554 дня ] .
Высокотоксичные соединения ртути — каломель , сулему , мертиолят и другие — используют для протравливания семенного зерна и в качестве пестицидов .
Ртуть и многие её соединения ядовиты . Воздействие ртути — даже в небольших количествах — может вызывать серьёзные проблемы со здоровьем и представляет угрозу для внутриутробного развития плода и развития ребёнка на ранних стадиях жизни. Ртуть может оказывать токсическое воздействие на нервную, пищеварительную и иммунную системы, а также на лёгкие, почки, кожу и глаза. ВОЗ рассматривает ртуть в качестве одного из десяти основных химических веществ или групп химических веществ, представляющих значительную проблему для общественного здравоохранения .
Наиболее ядовиты пары́ и растворимые соединения ртути. Сама металлическая ртуть менее опасна , однако она постепенно испаряется даже при комнатной температуре . Пары могут вызвать тяжёлое отравление , для чего достаточно, например, ртути из одного разбитого медицинского термометра. Ртуть и её соединения ( сулема , каломель , киноварь , цианид ртути ) поражают нервную систему, печень, почки, желудочно-кишечный тракт, при вдыхании — дыхательные пути (а проникновение ртути в организм чаще происходит именно при вдыхании её паров, не имеющих запаха). По классу опасности ртуть относится к первому классу (чрезвычайно опасное химическое вещество). Опасный загрязнитель окружающей среды, особенно опасны выбросы в воду, поскольку в результате деятельности населяющих дно микроорганизмов происходит образование растворимой в воде и токсичной метилртути , накапливающейся в рыбе . Ртуть — типичный представитель кумулятивных ядов.
Органические соединения ртути ( диметилртуть и др.) в целом намного токсичнее, чем неорганические, прежде всего из-за их липофильности и способности более эффективно взаимодействовать с элементами ферментативных систем организма.
В норме общее количество ртути в организме человека массой 70 кг составляет около 6 мг . В большинстве тканей организма её относительное содержание 0,2—0,7 мг/кг , в костях 0,5 мг/кг , в крови 0,008 мг/кг .
| Среда | место |
продолжительность
воздействия |
концентрация | единицы |
|---|---|---|---|---|
| Воздух | в населённых пунктах и в жилых помещениях | среднесуточная | 0,0003 | мг / м 3 |
| воздуха в рабочей зоне | макс. разовая | 0,01 | ||
| среднесменная | 0,005 | |||
| Вода | сточная, для неорганических соединений в пересчёте на Hg (II) | 0,005 | мг/ л | |
| хозяйственно-питьевого и культурного водопользования | 0,0005 | |||
| рыбохозяйственных водоёмов | 0,00001 | |||
| морских водоёмов | 0,0001 | |||
Демеркуризацией называется очистка помещений и предметов от загрязнений металлической ртутью и источников ртутных паров. В быту самой частой ситуацией для демеркуризации является ртуть, вылившаяся из разбитого ртутного термометра, что не представляет серьёзной опасности, но требует аккуратности и соблюдения правил безопасности. Необходимо связаться с экстренными службами и выяснить, что делать. Необходимо проветривать помещение. Выбрасывать ртуть в бытовой мусор или сливать в канализацию нельзя. Также нельзя использовать пылесос для сбора ртути — он разобьёт ртуть на мельчайшие капли и ускорит её испарение, таким образом концентрация паров ртути повысится вплоть до опасного уровня .
С 2020 года международная конвенция , названная в память массового отравления ртутью и подписанная многими странами, запрещает производство, экспорт и импорт нескольких различных видов ртутьсодержащих продуктов, применяемых в быту, в том числе электрических батарей, электрических выключателей и реле, некоторых видов компактных люминесцентных ламп (КЛЛ), люминесцентных ламп с холодным катодом или с внешним электродом, ртутных термометров и приборов измерения давления . Конвенция вводит регулирование использования ртути и ограничивает ряд промышленных процессов и отраслей, в том числе горнодобывающую (особенно непромышленную добычу золота), производство цемента .