Interested Article - Карбаминовая кислота

- 2021-07-06
- 2
Карбаминовая кислота (аминокарбоновая, аминометановая или аминомуравьиная кислота, моноамид угольной кислоты) — органическая кислота с химической формулой NH 2 COOH. В свободном состоянии очень неустойчива и при температуре выше 250 K (-23 °C) разлагается на аммиак и углекислый газ , а в присутствии воды также образуется карбонат аммония . Её соли и сложные эфиры систематически называют карбаматами, сложные эфиры часто также называют уретанами .
В чистом виде не выделена. При пропускании сухих СО 2 и NH 3 через абсолютный спирт при охлаждении осаждается карбаминово-аммиачная соль NH 2 COONH 4 в виде кристаллического порошка, которая тоже весьма неустойчива и разлагается при температурах заметно ниже 0 °C, хотя её и можно выделить с свободном виде . Побочным продуктом в этой же реакции получается и сама карбаминовая кислота. В твёрдой фазе она, по-видимому, состоит из димеров, причем две молекулы соединены водородными связями между двумя карбоксильными группами -COOH, а не посредством взаимодействия групп -NH 2 и -COOH, как в аминокислотах .

Строение
Карбаминовую кислоту можно рассматривать как молекулу, содержащую в своём составе аминогруппу и , и, следовательно, как аминокислоту ; однако присоединение карбоксильной группы -COOH непосредственно к атому азота без какой-либо промежуточной углеродной цепи заставляет ее вести себя совсем не так, как аминокислоты с промежуточной углеродной цепью. Поэтому простейшей аминокислотой считается глицин NH 2 CH 2 COOH. Гидроксильная группа -ОН, присоединенная к углероду, также исключает ее из класса амидов .
Термин «карбаминовая кислота» также используется в общем для любых соединений формы RR’NCOOH, где R и R' представляют собой органические группы или водород .
Структура
Карбаминовая кислота представляет собой плоскую молекулу .
Аминогруппа карбаминовой кислоты, в отличие от большинства аминов, не протонируется до аммонийной группы NH
+
3
-.
Цвиттер-ионная
форма H
3
N
+
−COO
−
очень нестабильна и быстро разлагается на аммиак и диоксид углерода
, однако есть сообщение о его обнаружении во льдах, облученных
протонами
высокой энергии
.
Производные
Известны соли с неорганическим катионом, в частности аммонийная соль, соли щелочных и щёлочноземельных элементов .
Хлорангидрид карбаминовой кислота кислоты CO(NH 2 )Cl получается при действии сухого хлороводорода на циановокислые соли:
AgCNO + 2HCl = AgCl + CO(NH 2 )Cl
или при действии фосгена на нашатырь при нагревании:
COCl 2 + NH 4 Cl = CO(NH 2 )Cl + 2HCl.
Хлорангидрид представляет собой жидкость с резким запахом, иногда образует призматические кристаллы с температурой плавления 50 °С и температурой кипения 60-62 °С, разлагаясь при кипении на хлороводород и циановую кислоту , которые при охлаждении вновь соединяются, но лишь отчасти, так как главная масса циановой кислоты превращается при этом в . Постепенное превращение в циамелид с потерей HCl происходит и при хранении при комнатной температуре. Водой хлорангидрид энергично разлагается на углекислоту и нашатырь .
Карбаминовая кислота формально является исходным соединением для нескольких важных семейств органических соединений:
-
карбаминовые кислоты
-
карбамат-анионы
-
карбаматы или уретаны
-
карбамоилхлориды
Карбаминовые кислоты
Многие замещенные карбаминовые кислоты (RHNCOOH или RR’NCOOH) можно легко синтезировать путем пропускания диоксида углерода через раствор соответствующего амина (RNH 2 или RR’NH, соответственно) в соответствующем растворителе, таком как диметилсульфоксид или сверхкритический диоксид углерода . Эти карбаминовые кислоты обычно нестабильны при комнатной температуре и превращаются в исходный амин и двуокись углерода .
Уретаны
В отличие от карбаминовых кислот, сложные эфиры карбаминовой кислоты обычно стабильны при комнатной температуре. Их получают реакцией карбамоилхлоридов со спиртами, добавлением спиртов к изоцианатам и реакцией карбонатных эфиров с аммиаком . Метилкарбамат и этилкарбамат являются одними из простейших примеров и исторически использовались в текстильной промышленности, оба в настоящее время считаются канцерогенами. Также известен бензилкарбамат.
Нахождение в природе
Фермент карбаматкиназа, участвующий в нескольких метаболических путях живых организмов, катализирует образование карбамоилфосфата H 2 N−C(=O)−O−PO 3 2− :
Одна молекула гемоглобина может переносить четыре молекулы углекислого газа в легкие в виде карбаматных групп, образующихся в результате реакции CO 2 с четырьмя концевыми аминогруппами дезоксиформы . Полученное соединение называется карбгемоглобин .
Он играет роль метаболита кишечной палочки .
Образование метаболитов карбаматглюкуронидов было описано для многих фармацевтических препаратов, и они были идентифицированы у всех видов, обычно используемых в исследованиях метаболизма лекарств (крыса, собака, мышь, кролик, морская свинка и человек). Не было выявлено явной видовой специфичности их образования и предпочтения аминов 1-й или 2-й степени. В литературе также описано много биологических реакций, включающих реакцию СО 2 с аминогруппами биомолекул. Например, СО 2 , образующийся при клеточном дыхании, частично выводится за счет обратимого образования карбамата между СО 2 и -аминогруппами альфа- и бета-цепей гемоглобина .
Имеются предпосылки к её наличию в молекулярных облаках межзвёздной среды .
Применение
Промышленность
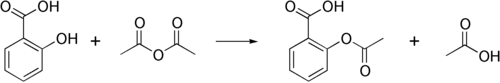
Карбаминовая кислота является промежуточным продуктом в промышленном производстве мочевины, которая включает реакцию двуокиси углерода и аммиака .
- CO 2 + NH 3 → H 2 NCOOH
- H 2 NCOOH + NH 3 → CO(NH 2 ) 2 + H 2 O
Медицина
Некоторые сложные эфиры карбаминовой кислоты используются в качестве миорелаксантов , в том числе эмилкамат, фенпробамат, стирамат и другие. Они связываются с барбитуратным участком рецептора ГАМК A .
Инсектициды
Было разработано несколько инсектицидов на основе карбаминовой кислоты; например, алдикарб, севин , карбофуран .
Органический синтез
Аминогруппа может быть защищена от нежелательных реакций путём образования карбаматной защитной группы -NHC(=O)-OR. При гидролизе сложноэфирной связи образуется карбаминовая кислота -NHC(= O)OH, которая затем теряет двуокись углерода с получением желаемого амина.
Токсичность
Карбаминовая кислота иногда обнаруживается в виде карбамата у рабочих, подвергшихся воздействию пестицидов. Карбаматы, особенно карбофуран, по-видимому, больше связаны с обильной и разнообразной симптоматикой воздействия пестицидов, чем органофосфаты. Неврологические симптомы возникают у фермеров, подвергающихся профессиональному воздействию инсектицидов, ингибирующих ацетилхолинэстеразу , таких как карбаматы. Продукты карбаминовой кислоты нескольких аминов, таких как бета-N-метиламино-L-аланин (БМАА), этилендиамин и L-цистеин , были причастны к токсичности. Исследования показали, что значительная часть аминосоединений в биологических образцах (которые естественным образом содержат CO 2 /бикарбонат) могут присутствовать в виде карбаминовой кислоты .
Примечания
- ↑ PubChem. (англ.) . pubchem.ncbi.nlm.nih.gov . Дата обращения: 2 апреля 2023. 2 апреля 2023 года.
- ↑ Benno Krieg. . — 7. Aufl. mit CD-ROM. — Berlin, 2004. — С. 281. — XV, 393 S с. — ISBN 978-3-11-017999-6 , 3-11-017999-7.
- ↑ www.brocgaus.ru . Дата обращения: 2 апреля 2023. 2 апреля 2023 года.
- ↑ J. B. Bossa, P. Theulé, F. Duvernay, F. Borget, T. Chiavassa. (англ.) // Astronomy & Astrophysics. — 2008-12. — Vol. 492 , iss. 3 . — P. 719–724 . — ISSN . — doi : .
- ↑ Z.J. Dijkstra, A.R. Doornbos, H. Weyten, J.M. Ernsting, C.J. Elsevier, J.T.F. Keurentjes. (англ.) // The Journal of Supercritical Fluids. — 2007-05. — Vol. 41 , iss. 1 . — P. 109–114 . — doi : . 15 ноября 2022 года.
- ↑ R. K. Khanna, M. H. Moore. (англ.) // Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy. — 1999-05-01. — Vol. 55 , iss. 5 . — P. 961–967 . — ISSN . — doi : .
- Y.-J. Chen, M. Nuevo, J.-M. Hsieh, T.-S. Yih, W.-H. Sun, W.-H. Ip, H.-S. Fung, S.-Y. Chiang, Y.-Y. Lee, J.-M. Chen, C.-Y. R. Wu. // Astronomy & Astrophysics. — 2007-03. — Т. 464 , вып. 1 . — С. 253–257 . — ISSN . — doi : .
- Thomas L. Lemke. . — 4th ed. — Baltimore, MD: Lippincott Williams & Wilkins, 2003. — С. 63. — x, 156 pages с. — ISBN 0-7817-4381-8 , 978-0-7817-4381-5.
- Peter Jäger, Costin N. Rentzea, Heinz Kieczka. . — Sixth edition. — Weinheim, Germany, 2002. — 1 online resource (40 volumes) с. — ISBN 978-3-527-30673-2 , 3-527-30673-0. 2 апреля 2023 года.
- Jozef H. Meessen, Harro Petersen. (англ.) // Ullmann's Encyclopedia of Industrial Chemistry / Wiley-VCH Verlag GmbH & Co. KGaA. — Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA, 2000-06-15. — P. a27_333 . — ISBN 978-3-527-30673-2 . — doi : . 2 апреля 2023 года.
- Charles Owens Wilson, Ole Gisvold. . — Lippincott Williams & Wilkins, 2004. — С. 495. — 1016 с. — ISBN 978-0-7817-3481-3 .
- J F Risher, F L Mink, J F Stara. // Environmental Health Perspectives. — 1987-06. — Т. 72 . — С. 267–281 . — ISSN . 2 апреля 2023 года.
- 2021-07-06
- 2