Interested Article - Бромид золота(III)

- 2021-05-13
- 2
Бромид золота(III) ( трибромид золота ) — бинарное неорганическое химическое соединение золота с бромом .
История
Первые упоминания об исследованиях галогенидов золота встречаются в начале XIX века .
Физические свойства
Кристаллическое вещество, тёмно-коричневые блестящие пластинки , цвет — от тёмно-красного до черного.
Растворим в воде, эфире , броме, бромоформе , метилацетате и SbCl 3 .
Мало растворим в сероуглероде и четыреххлористом углероде .
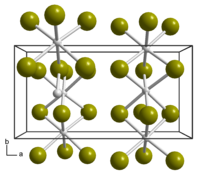
Структура
Эмпирическая формула AuBr 3 , но представляет собой димер состава Au 2 Br 6 .

Химические свойства
При нагревании разлагается на бромид золота (I) и бром .
Бромид золота(III) является кислотой Льюиса и легко образует комплексы. Например, в бромистоводородной кислоте димер Au 2 Br 6 растворяется с образованием кислоты HAuBr 4 .
Во влажном воздухе AuBr 3 быстро гидролизуется , горячей водой разлагается.
Синтез
Бромид золота(III) может быть получен:
- прямым синтезом из простых веществ при 140° С и избытке брома (жидкого, паров или бромной воды):
- 2Au + 3Br 2 → Au 2 Br 6 (реакция начинается уже при обычной температуре )
- обменной реакцией:
- Au 2 Cl 6 + 6HBr → 6HCl + Au 2 Br 6
Применение
Бромид золота(III) используется в качестве катализатора в различных реакциях, интересный вариант использования — в реакции Дильса-Альдера . В частности, соединение катализирует реакцию между енильными и карбонильными соединениями с образованием шестичленных циклов:

Другой пример использования AuBr 3 в качестве катализатора — в реакциях нуклеофильного замещения :

Токсичность
Как и другие соединения золота, при длительном контакте бромид золота (III) вызывает у человека специфические аллергические дерматиты и экземы , проявляющиеся в виде рецидивирующих папулезных высыпаниях на кистях, предплечьях и лице .
Источники
- И. Л. Кнунянц . Краткая химическая энциклопедия т. 2, М.: Советская энциклопедия, 1963, с. 119
- И. Л. Кнунянц . Краткая химическая энциклопедия т. 2, М.: Советская энциклопедия, Москва, 1990, с. 170
Ссылки
- (англ.)
Примечания
- Lengefield, F. American Chemical Journal 1901 , vol. 26, pp. 324 (англ.)
- Thomsen, J. J. prakt. Chem. 1876 , vol. 13, pp. 337 (англ.)
- Schottländer, Ann. Chem. (Liebig) , vol. 217, pp. 312 (нем.)
- Krüss, G. Ber. d. chem. Ges. 1887 , vol. 20, pp. 2634 (нем.)
- ↑ . Дата обращения: 20 января 2012. Архивировано из 4 февраля 2013 года.
- Лазарев Н. В. Вредные вещества в промышленности, Л., «Химия», 1977, т. III, с. 342
- 2021-05-13
- 2