Interested Article - Анаммокс

- 2021-05-26
- 1

Анаммо́кс (сокр. от англ. an aerobic ammo nium ox idation — анаэробное окисление аммония ) — один из ключевых микробных процессов в круговороте азота . Бактерии , осуществляющие этот процесс, были открыты в 1999 году, и в своё время описание этого процесса стало большим сюрпризом для научного сообщества . Уравнение процесса:
- NH 4 + + NO 2 − → N 2 + 2H 2 O.
Этот процесс происходит во многих природных сообществах.
Общая характеристика процесса
В ходе анаммокса нитрит - ион и ион аммония превращаются непосредственно в молекулярный азот :
- NH 4 + + NO 2 − → N 2 + 2H 2 O.
В масштабах планеты этот процесс даёт начало 30—50 % молекулярного азота, образующегося в океанах . В ходе анаммокса утилизируются соединения фиксированного азота в усваиваемой растениями форме и переводятся в неусваиваемую молекулярную форму, поэтому этот процесс ограничивает первичную продуктивность океана .

Бактерии, осуществляющие анаммокс, относятся к типу планктомицетов . На данный момент анаммокс описан у представителей 5 родов бактерий: , , , (все пресноводные виды), а также (морские представители) . Для бактерий, осуществляющих анаммокс, характерно несколько отличительных черт: в их клетках всегда содержится единственная — окружённый мембраной компартмент, в котором и происходит процесс анаммокса. Кроме того, их мембраны содержат особые липиды , обнаруженные лишь у этих организмов . Особый интерес представляет образование гидразина как промежуточного соединения (это вещество используется как ракетное топливо и ядовито для большинства организмов) . Наконец, эти бактерии отличаются поразительно низкой скоростью роста: время удвоения численности составляет 7—22 дней . Они способны осуществлять превращения субстратов анаммокса даже при очень низкой их концентрации (менее микромолярных); иными словами, они отличаются очень высоким сродством к аммонию и нитриту . Клетки, осуществляющие анаммокс, содержат очень много белков типа цитохрома с , которые составляют до 30 % всех клеточных белков. К их числу относятся и ферменты, осуществляющие ключевые катаболические реакции анаммокса; они придают клеткам характерный красный цвет . Изначально считалось, что анаммокс происходит только при температурах 20—43 °C , однако в недавнее время анаммокс был описан в горячих источниках при температурах 36—52 °C и в гидротермальных источниках вдоль Срединно-Атлантического хребта при температурах 60–85 °C .
История

В 1932 году появились сообщения об образовании азота в ходе неизвестного процесса при брожении , которое происходило в иловых отложениях в (штат Висконсин , США ) . Более чем через 40 лет назад Ричардс заметил, что большая часть аммония, которая должна была бы образоваться при реминерализации органических остатков, пропадала . Поскольку никаких биологических путей для осуществления таких превращений известно не было, поначалу биологическое анаэробное окисление получило мало внимания . Тридцать лет назад при помощи термодинамических расчётов было предсказано существование двух хемолитоавтотрофных организмов, способных окислять аммиак до азота . Долгое время, впрочем, считали, что биологическое окисление аммиака невозможно, поскольку многие предшествующие попытки найти биологическую основу этих реакций не увенчались успехом. В 1990-х годах наблюдения Арнольда Мадлера ( англ. Arnold Mulder ) подтвердили заключение Ричардса . Эти учёные наблюдали, что в лишённой кислорода среде, содержащей бактерии, ионы аммония исчезают с видимым образованием азота. Этот процесс получил название анаммокс, и стало понятно, что он имеет огромное значение для разложения невостребованного аммония. Об открытии анаммокса было публично объявлено на Пятом биотехнологическом европейском конгрессе . В середине 1990-х было сообщено об открытии анаммокса в ( англ. fluidized bed reactor ) . В нём наибольшая скорость анаммокса составила 0,4 кг N/м 3 /d. Было показано, что для поглощения 1 моля аммония был необходимы 0,6 моля нитрата , в результате чего образовывалось 0,8 моля газообразного N 2 . В том же году была определена биологическая природа анаммокса . Эксперименты с применением радиоактивных изотопов показали, что при использовании 15 NH 4 + и 14 NO 3 − доминирующим продуктом был 14-15 N 2 , который составлял 98,2 % всего меченного N 2 . Стало понятно, что в качестве агента, окисляющего аммиак, в анаммоксе использовался нитрит, а не нитрат. На основании предшествующих исследований Strous и коллеги, используя баланс взаимодействующих масс, рассчитали стехиометрию анаммокса , и их результаты получили широкую известность в других группах учёных. Позднее было определено, что бактерии, осуществляющие анаммокс, относятся к типу планктомицетов , и первый известный осуществляющий анаммокс организм получил название Candidatus Brocadia anammoxidans . До 2002 года считалось, что анаммокс играет лишь небольшую роль в круговороте азота в природных экосистемах . Однако в 2002 году установили, что анаммокс играет важную роль в биологическом цикле азота, на его долю приходится от 24 до 67 % общей продукции азота в осадочном слое континентальных шельфов . Из-за этого представление об общем виде круговорота азота в природе несколько изменилось, как показано на рисунке.
Возможный механизм реакции


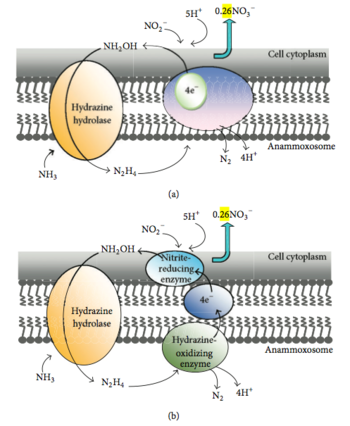
Согласно экспериментам с 15 N, проведённым в 1997 году, в ходе анаммокса аммоний биологически окисляется до гидроксиламина , а в качестве возможного акцептора электронов выступает нитрит . Считается, что электронные эквиваленты, необходимые для восстановления нитрита до гидроксиламина, образуются при превращении гидразина в молекулярный азот . Предложено два возможных механизма этих реакций . Согласно первому механизму, мембраносвязанный ферментный комплекс осуществляет превращение аммония и гидроксиламина в гидразин, который в периплазме окисляется до азота. В этот же момент цитоплазматическая сторона того же самого комплекса, который окисляет гидразин, и осуществляет внутренний перенос электронов. Второй механизм утверждает следующее. Аммоний и гидроксиламин превращает в гидразин мембраносвязанный ферментный комплекс, после чего гидразин окисляется до молекулярного азота в периплазматическом пространстве, а высвобожденные электроны через электронтранспортную цепь доставляются в цитоплазму к ферменту, восстанавливающему нитрит до гидроксиламина. Ещё нет ясности относительно того, происходит ли восстановление нитрита и окисление гидроксиламина в разных сайтах одного и того же фермента, или же эти реакции осуществляются двумя различными ферментными системами, соединёнными электронтранспортной цепью . Микроорганизмы редко используют гидразин как промежуточное соединение в метаболизме азота . Возможно, в нитрогеназной реакции именно он является связанным с ферментом промежуточным соединением .
Hooper и коллеги предположили, что, возможно, в анаммоксе принимают участие оксид азота NO и HNO: NO или HNO конденсируется с аммонием под действием фермента, родственного ферментам семейства аммониймонооксигеназ . Выделяющийся гидразин или имин может впоследствии превратиться в молекулярный азот под действием , а образующиеся необходимы для реакции между NO или HNO с аммонием или же для восстановления нитрита до NO. Геномный анализ вида Candidatus Kuenenia stuttgartiensis показал, что у этого организма промежуточным соединением является не гидроксиламмоний, а NO; таким образом, у него имеет место близкий, но слегка отличающийся метаболический механизм . Однако эта гипотеза не противоречит тому, что важным промежуточным соединением анаммокса является гидразин. С гидразином работают два фермента, уникальных для бактерий, осуществляющих анаммокс: гидразингидролаза (hh) и гидразиндегидрогеназа (hd). Hh образует гидразин из нитрита и аммония, а hd переносит электроны с гидразина на ферредоксин . Были определены несколько генов , которые участвуют в биосинтезе жирных кислот и S-аденозилметионина , которые содержат каталитические домены и домены, имеющие электрон-транспортную цепь .
Аэрация и добавление органических субстратов (обычно метанола ) показало, что две стадии анаммокса, во-первых, являются чрезвычайно энергозатратными процессами, во-вторых, связаны с образованием излишков илистых отложений и, в-третьих, дают начало большим объёмам парниковых газов , таких как СО 2 , N 2 O и NO, поглощающий озон . Поскольку анаммокс-бактерии непосредственно превращают аммоний и нитрит в N 2 в анаэробных условиях, этот процесс не нуждается в аэрации и добавлении других доноров электронов. Тем не менее, кислород необходим для образования нитрита бактериями, окисляющими аммоний. Однако в системах анаммокса с частичной нитрификацией потребность в кислороде значительно снижена, потому что только половина аммония окисляется до нитрита вместо полного превращения в нитрат .
Разнообразие видов

К настоящему моменту описано 10 видов , представители которых могут осуществлять анаммокс, причём семь из них могут быть выращены в лабораторной культуре . Все они пока имеют таксономический статус Candidatus , поскольку ни один из них не удалось получить в чистой культуре. Известные виды распределены по 5 родам: Kuenenia ( Kuenenia stuttgartiensis ) , Brocadia (три вида: B. anammoxidans , и B. sinica ) , Anammoxoglobus ( A. propionicus ) , Jettenia ( J. asiatica ) и Scalindua ( S. brodae , S. sorokinii , и S. profunda ) . Представители первых четырёх видов были выделены из осадков, покрывающих растения, использующиеся для очищения сточных вод. K. stuttgartiensis , B. anammoxidans , B. fulgida и A. propionicus были выделены из одной и той же посевной культуры. Scalindua населяет преимущественно морские воды, однако встречается также в пресноводных экосистемах и на растениях, очищающих сточные воды . Эти 10 видов, судя по всему, представляют лишь малую долю биоразнообразия видов, осуществляющих анаммокс. Например, в базе данных GenBank в настоящее время содержится более 2000 генов 16S рРНК , выделенных из бактерий, осуществляющих анаммокс. Они принадлежат различным видам, подвидам и штаммам , которые сумели найти свою собственную видовую нишу среди различных сред обитания, населяемых бактериями, проводящими анаммокс. Видовое микроразнообразие особенно выражено у морского рода Scalindua .
Доля совпадения последовательностей 16S рРНК у анаммокс-бактерий составляет от 87 до 99 %, и филогенетические данные заставляют отнести их к филуму Planctomycetes , который образует суперфилум PVC вместе с филумами Verrucomicrobia и Chlamydiae . В пределах Planctomycetes анаммокс-бактерии формируют рано отделившуюся монофилетическую кладу. Их филогенетические особенности вместе со специфическими клеточными, физиологическими и молекулярными свойствами заставляют выделить анаммокс-бактерии в порядок Brocadiales .
Применение
Анаммокс применяется для удаления аммония из сточных вод при их очистке и включает два раздельных процесса. Первый из них заключается в частичной нитрификации половины аммония до нитрита бактериями, окисляющими аммиак.
- 2NH 4 + + 3O 2 → 2NO 2 − + 4H + + 2H 2 O
Далее остатки аммония и нитрит в ходе анаммокса, осуществляемого второй группой бактерий, превращаются в нитрат и молекулярный азот (выход около 15 %, не показано):
- NH 4 + + NO 2 − → N 2 + 2H 2 O
Оба процесса могут происходить в одном и том же реакторе, где бактерии двух разных групп формируют компактные гранулы .
Для получения гранулярной биомассы или биоплёнки из бактерий, осуществляющих анаммокс, необходимы специальные реакторы, причём в оптимальных условиях необходимый объём культуры может быть достигнут за 20 дней. Для выращивания анаммокс-бактерий подходят такие системы, как реактор переменного действия ( англ. sequencing batch reactors, SBR ), движущийся реактор с кипящим слоем ( англ. moving bed reactor ) и реакторы типа gas-lift-loop. Первый крупномасштабный реактор, предназначенный для выращивания анаммокс-бактерий, был построен в Нидерландах в 2002 году .
Анаммокс — торговое наименование технологии удаления аммиака, основанной на его анаэробном окислении и разработанной Делфтским техническим университетом .
Примечания
- ↑ Arrigo K. R. (англ.) // Nature. — 2005. — Vol. 437, no. 7057 . — P. 349—355. — doi : . — .
- ↑ Strous M. , Fuerst J. A. , Kramer E. H. , Logemann S. , Muyzer G. , van de Pas-Schoonen K. T. , Webb R. , Kuenen J. G. , Jetten M. S. (англ.) // Nature. — 1999. — Vol. 400, no. 6743 . — P. 446—449. — doi : . — .
- Reimann, Joachim; Jetten, Mike S.M.; Keltjens, Jan T. Chapter 7 Metal Enzymes in “Impossible” Microorganisms Catalyzing the Anaerobic Oxidation of Ammonium and Methane // Sustaining Life on Planet Earth: Metalloenzymes Mastering Dioxygen and Other Chewy Gases (англ.) / Peter M.H. Kroneck and Martha E. Sosa Torres. — Springer, 2015. — Vol. 15. — P. 257—313. — (Metal Ions in Life Sciences). — doi : .
- Devol A. H. (англ.) // Nature. — 2003. — Vol. 422, no. 6932 . — P. 575—576. — doi : . — .
- ↑ Kartal B. , de Almeida N. M. , Maalcke W. J. , Op den Camp H. J. , Jetten M. S. , Keltjens J. T. (англ.) // FEMS microbiology reviews. — 2013. — Vol. 37, no. 3 . — P. 428—461. — doi : . — .
- Jetten M. S. , Niftrik Lv , Strous M. , Kartal B. , Keltjens J. T. , Op den Camp H. J. (англ.) // Critical reviews in biochemistry and molecular biology. — 2009. — Vol. 44, no. 2-3 . — P. 65—84. — doi : . — .
- Boumann H. A. , Longo M. L. , Stroeve P. , Poolman B. , Hopmans E. C. , Stuart M. C. , Sinninghe Damst J. S. , Schouten S. (англ.) // Biochimica et biophysica acta. — 2009. — Vol. 1788, no. 7 . — P. 1444—1451. — doi : . — .
- ↑ Schalk J. , Oustad H. , Kuenen J. G. , Jetten M. S. (англ.) // FEMS microbiology letters. — 1998. — Vol. 158, no. 1 . — P. 61—67. — .
- ↑ Strous M. , Kuenen J. G. , Jetten M. S. (англ.) // Applied and environmental microbiology. — 1999. — Vol. 65, no. 7 . — P. 3248—3250. — .
- Yan J. , Haaijer S. C. , Op den Camp H. J. , van Niftrik L. , Stahl D. A. , Könneke M. , Rush D. , Sinninghe Damst J. S. , Hu Y. Y. , Jetten M. S. (англ.) // Environmental microbiology. — 2012. — Vol. 14, no. 12 . — P. 3146—3158. — doi : . — .
- Kartal B. , Maalcke W. J. , de Almeida N. M. , Cirpus I. , Gloerich J. , Geerts W. , Op den Camp H. J. , Harhangi H. R. , Janssen-Megens E. M. , Francoijs K. J. , Stunnenberg H. G. , Keltjens J. T. , Jetten M. S. , Strous M. (англ.) // Nature. — 2011. — Vol. 479, no. 7371 . — P. 127—130. — doi : . — .
- Jaeschke A. , Op den Camp H. J. , Harhangi H. , Klimiuk A. , Hopmans E. C. , Jetten M. S. , Schouten S. , Sinninghe Damst J. S. (англ.) // FEMS microbiology ecology. — 2009. — Vol. 67, no. 3 . — P. 343—350. — doi : . — .
- Byrne N. , Strous M. , Crépeau V. , Kartal B. , Birrien J. L. , Schmid M. , Lesongeur F. , Schouten S. , Jaeschke A. , Jetten M. , Prieur D. , Godfroy A. (англ.) // The ISME journal. — 2009. — Vol. 3, no. 1 . — P. 117—123. — doi : . — .
- R. J. Allgeier, W. H. Peterson, C. Juday, E. A. // International Review of Hydrobiology. — 1932. — Vol. 26, № 5—6 . — P. 444—461. — doi : . 7 марта 2016 года.
- F. A. Richards. Anoxic basins and fjordsin // Chemical Oceanography / J.P. Ripley and G. Skirrow, Eds.. — London, UK: Academic Press, 1965. — P. 611—645.
- Broda E. (англ.) // Zeitschrift fur allgemeine Mikrobiologie. — 1977. — Vol. 17, no. 6 . — P. 491—493. — .
- Kuenen J. G. (англ.) // Nature reviews. Microbiology. — 2008. — Vol. 6, no. 4 . — P. 320—326. — doi : . — .
- A. A. van de Graaf, A. Mulder, H. Slijkhuis, L. A. Robertson, J. G. Kuenen. Anoxic ammonium oxidation // Proceedings of the 5th European Congress on Biotechnology. — Copenhagen, Denmark: C. Christiansen, L. Munck, and J. Villadsen, Eds., 1990. — P. 338—391.
- A. Mulder, A. A. Van De Graaf, L. A. Robertson, J. G. Kuenen. // FEMS Microbiology Ecology. — 1995. — Vol. 16, № 3 . — P. 177—184. — doi : . 24 сентября 2015 года.
- van de Graaf A. A. , Mulder A. , de Bruijn P. , Jetten M. S. , Robertson L. A. , Kuenen J. G. (англ.) // Applied and environmental microbiology. — 1995. — Vol. 61, no. 4 . — P. 1246—1251. — .
- M. Strous, J. J. Heijnen, J. G. Kuenen, M. S. M. Jetten. (англ.) // . — Springer , 1998. — Vol. 50, no. 5 . — P. 589—596. — doi : . 20 июля 2017 года.
- J. G. Kuenen, M. S. M. Jetten. Extraordinary anaerobic ammonium oxidising bacteria // ASM News. — 2001. — Vol. 67. — P. 456—463.
- Francis C. A. , Beman J. M. , Kuypers M. M. (англ.) // The ISME journal. — 2007. — Vol. 1, no. 1 . — P. 19—27. — doi : . — .
- Thamdrup B. , Dalsgaard T. (англ.) // Applied and environmental microbiology. — 2002. — Vol. 68, no. 3 . — P. 1312—1318. — .
- Van De Graaf, A. A. et al. // Microbiology. — 1997. — Vol. 143, № 7 . — P. 2415—2412. (недоступная ссылка)
- ↑ Ni S. Q. , Zhang J. (англ.) // BioMed research international. — 2013. — Vol. 2013. — P. 469360. — doi : . — .
- Dilworth M. J. , Eady R. R. (англ.) // The Biochemical journal. — 1991. — Vol. 277 ( Pt 2). — P. 465—468. — .
- Hooper A. B. , Vannelli T. , Bergmann D. J. , Arciero D. M. (англ.) // Antonie van Leeuwenhoek. — 1997. — Vol. 71, no. 1-2 . — P. 59—67. — .
- ↑ Strous M. , Pelletier E. , Mangenot S. , Rattei T. , Lehner A. , Taylor M. W. , Horn M. , Daims H. , Bartol-Mavel D. , Wincker P. , Barbe V. , Fonknechten N. , Vallenet D. , Segurens B. , Schenowitz-Truong C. , Médigue C. , Collingro A. , Snel B. , Dutilh B. E. , Op den Camp H. J. , van der Drift C. , Cirpus I. , van de Pas-Schoonen K. T. , Harhangi H. R. , van Niftrik L. , Schmid M. , Keltjens J. , van de Vossenberg J. , Kartal B. , Meier H. , Frishman D. , Huynen M. A. , Mewes H. W. , Weissenbach J. , Jetten M. S. , Wagner M. , Le Paslier D. (англ.) // Nature. — 2006. — Vol. 440, no. 7085 . — P. 790—794. — doi : . — .
- Hu Z. , Lotti T. , de Kreuk M. , Kleerebezem R. , van Loosdrecht M. , Kruit J. , Jetten M. S. , Kartal B. (англ.) // Applied and environmental microbiology. — 2013. — Vol. 79, no. 8 . — P. 2807—2812. — doi : . — .
- Kartal B. , van Niftrik L. , Rattray J. , van de Vossenberg J. L. , Schmid M. C. , Sinninghe Damst J. , Jetten M. S. , Strous M. (англ.) // FEMS microbiology ecology. — 2008. — Vol. 63, no. 1 . — P. 46—55. — doi : . — .
- Oshiki M. , Shimokawa M. , Fujii N. , Satoh H. , Okabe S. (англ.) // Microbiology (Reading, England). — 2011. — Vol. 157, no. Pt 6 . — P. 1706—1713. — doi : . — .
- Kartal B. , Rattray J. , van Niftrik L. A. , van de Vossenberg J. , Schmid M. C. , Webb R. I. , Schouten S. , Fuerst J. A. , Damsté J. S. , Jetten M. S. , Strous M. (англ.) // Systematic and applied microbiology. — 2007. — Vol. 30, no. 1 . — P. 39—49. — doi : . — .
- Quan Z. X. , Rhee S. K. , Zuo J. E. , Yang Y. , Bae J. W. , Park J. R. , Lee S. T. , Park Y. H. (англ.) // Environmental microbiology. — 2008. — Vol. 10, no. 11 . — P. 3130—3139. — doi : . — .
- Hu B. L. , Rush D. , van der Biezen E. , Zheng P. , van Mullekom M. , Schouten S. , Sinninghe Damst J. S. , Smolders A. J. , Jetten M. S. , Kartal B. (англ.) // Applied and environmental microbiology. — 2011. — Vol. 77, no. 3 . — P. 966—971. — doi : . — .
- ↑ Schmid M. , Walsh K. , Webb R. , Rijpstra W. I. , van de Pas-Schoonen K. , Verbruggen M. J. , Hill T. , Moffett B. , Fuerst J. , Schouten S. , Damsté J. S. , Harris J. , Shaw P. , Jetten M. , Strous M. (англ.) // Systematic and applied microbiology. — 2003. — Vol. 26, no. 4 . — P. 529—538. — .
- ↑ Woebken D. , Lam P. , Kuypers M. M. , Naqvi S. W. , Kartal B. , Strous M. , Jetten M. S. , Fuchs B. M. , Amann R. (англ.) // Environmental microbiology. — 2008. — Vol. 10, no. 11 . — P. 3106—3119. — doi : . — .
- van de Vossenberg J. , Woebken D. , Maalcke W. J. , Wessels H. J. , Dutilh B. E. , Kartal B. , Janssen-Megens E. M. , Roeselers G. , Yan J. , Speth D. , Gloerich J. , Geerts W. , van der Biezen E. , Pluk W. , Francoijs K. J. , Russ L. , Lam P. , Malfatti S. A. , Tringe S. G. , Haaijer S. C. , Op den Camp H. J. , Stunnenberg H. G. , Amann R. , Kuypers M. M. , Jetten M. S. (англ.) // Environmental microbiology. — 2013. — Vol. 15, no. 5 . — P. 1275—1289. — doi : . — .
- Schubert C. J. , Durisch-Kaiser E. , Wehrli B. , Thamdrup B. , Lam P. , Kuypers M. M. (англ.) // Environmental microbiology. — 2006. — Vol. 8, no. 10 . — P. 1857—1863. — doi : . — .
- Hamersley M. R. , Woebken D. , Boehrer B. , Schultze M. , Lavik G. , Kuypers M. M. (англ.) // Systematic and applied microbiology. — 2009. — Vol. 32, no. 8 . — P. 571—582. — doi : . — .
- Ligi T. et al. // Ecol. Eng.. — 2015. — Vol. 80. — P. 181—190. 24 сентября 2015 года.
- Schmid M. C. , Risgaard-Petersen N. , van de Vossenberg J. , Kuypers M. M. , Lavik G. , Petersen J. , Hulth S. , Thamdrup B. , Canfield D. , Dalsgaard T. , Rysgaard S. , Sejr M. K. , Strous M. , den Camp H. J. , Jetten M. S. (англ.) // Environmental microbiology. — 2007. — Vol. 9, no. 6 . — P. 1476—1484. — doi : . — .
- Dang H. , Chen R. , Wang L. , Guo L. , Chen P. , Tang Z. , Tian F. , Li S. , Klotz M. G. (англ.) // Applied and environmental microbiology. — 2010. — Vol. 76, no. 21 . — P. 7036—7047. — doi : . — .
- Hong Y. G. , Li M. , Cao H. , Gu J. D. (англ.) // Microbial ecology. — 2011. — Vol. 62, no. 1 . — P. 36—47. — doi : . — .
- Hong Y. G. , Yin B. , Zheng T. L. (англ.) // Applied microbiology and biotechnology. — 2011. — Vol. 89, no. 4 . — P. 1233—1241. — doi : . — .
- Li M. , Cao H. , Hong Y. , Gu J. D. (англ.) // Applied microbiology and biotechnology. — 2011. — Vol. 89, no. 4 . — P. 1243—1254. — doi : . — .
- Fuerst J. A. , Sagulenko E. (англ.) // Nature reviews. Microbiology. — 2011. — Vol. 9, no. 6 . — P. 403—413. — doi : . — .
- Wagner M. , Horn M. (англ.) // Current opinion in biotechnology. — 2006. — Vol. 17, no. 3 . — P. 241—249. — doi : . — .
- Jetten MSM, Op den Camp HJM, Kuenen JG & Strous M. Description of the order Brocadiales // Bergey’s Manual of Systematic Bacteriology. — Springer, Heidelberg, 2010. — Vol. 4. — P. 596—603.
- B. Kartal, G.J. Kuenen, M.C.M van Loosdrecht. (англ.) // Science. — 2010. — Vol. 328. — P. 702—3. 24 сентября 2015 года.
-
Knight, Helen (2010-05-07).
.
New Scientist
.
из оригинала
23 апреля 2015
. Дата обращения:
май 2010
.
{{ cite news }}: Проверьте значение даты:|accessdate=( справка ) - van der Star WRL, Abma WR, Blommers D, Mulder J-W, Tokutomi T, Strous M, Picioreanu C, Van Loosdrecht MCM. Startup of reactors for anoxic ammonium oxidation: experiences from the first full-scale anammox reactor in Rotterdam // Water Res. — 2007. — Vol. 41. — P. 4149—4163.
- Jetten Michael Silvester Maria, Van Loosdrecht Marinus Corneli; Technische Universiteit Delft, 25 февраля 2012 года.
Литература
- Нетрусов А. И., Котова И. Б. Микробиология. — 4-е изд., перераб. и доп.. — М. : Издательский центр «Академия», 2012. — С. 179. — 384 с. — ISBN 978-5-7695-7979-0 .
- 2021-05-26
- 1