Interested Article - Индольные алкалоиды

- 2020-05-28
- 1

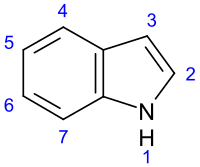
Индо́льные алкало́иды — класс алкалоидов , содержащих в своей структуре ядро индола или его производных . Один из наиболее многочисленных классов алкалоидов (наряду с изохинолиновыми ). Известно более 4100 индольных алкалоидов . Значительная часть индольных алкалоидов содержит также изопреноидные структурные элементы. Многие индольные алкалоиды обладают физиологической активностью, некоторые из них находят применение в медицине. Биогенетическим предшественником индольных алкалоидов является аминокислота триптофан .
История

С действием некоторых индольных алкалоидов человечество знакомо давно. Ацтеки в древности использовали галлюциногенные грибы рода Псилоцибе , содержащие алкалоиды псилоцибин и псилоцин . Раувольфия змеиная , содержащая резерпин , ещё за 1000 лет до н. э. использовалась в Индии в качестве лекарственного средства. Корни ибоги , содержащей ибогаин , использовались народами Африки в качестве стимулятора ЦНС . Физостигма ядовитая использовалась народами Нигерии для установления вины : подсудимому давали настойку её семян, после чего, если она выходила со рвотой , его оправдывали, в противном случае он умирал от паралича сердца и дыхания . Действующим веществом физостигмы является физостигмин (эзерин) .
Поражение спорыньёй посевов злаков в древние времена и в средневековье неоднократно приводила к эпидемиям эрготизма . Связь между спорыньёй и эрготизмом была установлена только в 1717 г., а алкалоид эрготамин , одно из основных действующих веществ спорыньи, был выделен в 1918 г.
Первый изолированный индольный алкалоид, стрихнин , был выделен Пеллетье и Каванту в 1818 г. из растений рода Стрихнос ( лат. Strychnos ). Правильная структурная формула стрихнина была определена только в 1947 г., хотя факт присутствия в структуре стрихнина индольного ядра был установлен несколько раньше .
Сам индол был впервые получен Байером в 1866 г. в процессе расщепления индиго .
Классификация
В зависимости от путей биосинтеза различают неизопреноидные и изопреноидные индольные алкалоиды. Последние включают в себя терпеноидные структурные элементы, синтезируемые живыми организмами из ( англ. ) (DMAPP) и/или ( англ. ) (IPP) :
-
Неизопреноидные:
- простые производные индола ;
- простые производные β-карболина ;
- пирролоиндольные алкалоиды.
-
Изопреноидные
:
- гемитерпеноиды : алкалоиды спорыньи;
- монотерпеноиды .
Существуют также чисто структурные классификации, основанные на наличии в углеродном скелете молекулы алкалоида элементов карбазола , β-карболина и т. п.
Кроме того, известно около 200 димерных индольных алкалоидов (бисиндольных алкалоидов), молекулы которых содержат по два индольных ядра .
Неизопреноидные индольные алкалоиды
Число известных неизопреноидных индольных алкалоидов невелико по сравнению с общим числом известных индольных алкалоидов .
Простые производные индола
Одними из простейших и вместе с тем широко распространённых природных производных индола являются биогенные амины триптамин и 5-гидрокситриптамин ( серотонин ) . Хотя отнесение их к алкалоидам не является общепринятым , оба этих соединения встречаются как в растительном , так и в животном мире . Скелет триптамина входит в структуру подавляющего большинства индольных алкалоидов .
N,N-диметилтриптамин ( ДМТ ), псилоцин и его фосфорилированное производное псилоцибин также относятся к простейшим производным триптамина .
Некоторые простые индольные алкалоиды не содержат структурного элемента триптамина, в частности, грамин и гликозолин (последний является производным карбазола ) .
Простые производные β-карболина
Распространённость β-карболиновых алкалоидов связана с простотой формирования ядра β-карболина из триптамина в процессе внутримолекулярной реакции Манниха . К простым (неизопреноидным) производным β-карболина относятся, например, гармин , гармалин и , а также чуть более сложного строения кантинон .
Гармалин был впервые выделен Гёбелем в 1841 г., гармин — Фритче в 1847 г.
Пирролоиндольные алкалоиды
Пирролоиндольные алкалоиды — сравнительно малочисленная группа производных триптамина, образующихся посредством метилирования индольного ядра в позиции 3 и последующей нуклеофильной атаки на атом углерода в позиции 2 с замыканием этиламинной группы в кольцо. Типичным представителем этой группы является физостигмин (эзерин) .
Физостигмин был открыт Йобстом и Гессе в 1864 г.
Изопреноидные индольные алкалоиды

Изопреноидные индольные алкалоиды включают в себя как остатки триптофана или триптамина, так и изопреноидные структурные элементы, производные от ( англ. ) и ( англ. ) .
Алкалоиды спорыньи
Алкалоиды спорыньи (эргоалкалоиды, англ. Ergot alkaloids ) представляют собой класс гемитерпеноидных индольных алкалоидов, родственных лизергиновой кислоте , которая, в свою очередь, образуется в процессе многоступенчатой реакции, вовлекающей триптофан и диметилаллилпирофосфат (DMAPP).
Многие алкалоиды спорыньи представляют собой амиды лизергиновой кислоты, простейшим из которых является эргин (лизергамид). Более сложные можно подразделить на две группы :
- Производные аминоспиртов , растворимые в воде, например, эргометрин (другие названия: эргоновин и эргобазин) и его изомер эргометринин (эргоновинин, эргобазинин);
-
Производные
полипептидов
, нерастворимые в воде, делящиеся на группы:
- группа эрготамина : собственно эрготамин, эргозин, а также их изомеры;
- группа эргоксина: эргостин, эргоптин, эргонин и их изомеры;
- группа эрготоксина: эргокристин, α-эргокриптин, β-эргокриптин, эргокорнин и их изомеры.
Эрготинин, открытый в 1875 г., и эрготоксин (1906 г.) впоследствии оказались смесями нескольких алкалоидов. В чистом виде первые алкалоиды спорыньи, эрготамин и его изомер эрготаминин, были выделены Штоллем в 1918 г.
Монотерпеноиды
Большинство монотерпеноидных алкалоидов включают в состав остаток C 9 или C 10 , происходящий от секологанина. В зависимости от структуры этого остатка такие алкалоиды подразделяют на три типа: тип Corynanthe , тип Iboga и тип Aspidosperma (по названиям типичных родов или видов растений, в которых содержатся такие алкалоиды). Ниже представлены углеродные скелеты монотерпеноидной части на примере алкалоидов аймалицина, катарантина и таберсонина. Кружком обозначены атомы углерода, отсутствующие в молекулах алкалоидов, включающих терпеноидный остаток C 9 (в отличие от C 10 ) .

Алкалоиды типа Corynanthe включают в себя скелет секологанина в неизменном виде, а алкалоиды типов Iboga и Aspidosperma — в перегруппированном виде . Некоторые представители монотерпеноидных индольных алкалоидов :
| Тип | Атомов углерода в монотерпеноидной части | |
|---|---|---|
| C 9 | C 10 | |
| Corynanthe | Аймалин , акуамицин, стрихнин , бруцин | Аймалицин (раубазин), йохимбин , резерпин , сарпагин, вобазин, митрагинин |
| Iboga | Ибогаин , ибогамин | Катарантин, воакангин |
| Aspidosperma | Эбурнамин | Таберсонин, виндолин, винкамин |
Существует также небольшая группа алкалоидов Аристотелии (около 30 соединений, важнейшим из которых является педункуларин), содержащих монотерпеноидную часть (C 10 ), происходящую не от секологанина .
Бисиндольные алкалоиды
Известно более 200 димерных индольных (бисиндольных) алкалоидов, получаемых в живых организмах посредством димеризации мономерных индольных оснований. Бисиндольные алкалоиды обычно образуются в процессе следующих реакций :
- Реакция Манниха (плейомутин, воакамин);
- Реакция Михаэля (виллальстонин);
- конденсация альдегидов с аминами — токсиферин, калебассин;
- Окислительное сочетание триптаминов (каликантин);
- Расщепление функциональной группы одного из мономеров (винбластин, винкристин ).
Помимо бисиндольных алкалоидов существуют димерные алкалоиды, образующиеся в процессе димеризации индольного мономера с алкалоидом другого типа. Примером является тубулозин, состоящий из индольного и изохинолинового структурных элементов .
Распространение в природе
Среди растений, богатых неизопреноидными индольными алкалоидами, можно выделить гармалу ( лат. Peganum harmala ), содержащую , гармин и гармалин , а также физостигму ядовитую ( лат. Physostigma venenosum ), содержащую физостигмин . Некоторые представители семейства Вьюнковые ( лат. Convolvulaceae ), в частности, утреннее сияние ( лат. Ipomoea violacea ) и Rivea corymbosa , содержат производные лизергиновой кислоты .
Индольные алкалоиды найдены в растениях из 39 семейств . Несмотря на значительное структурное многообразие, большая часть монотерпеноидных индольных алкалоидов локализована в трёх семействах двудольных : Кутровые ( лат. Apocynaceae ) — 73 вида , в частности, роды Альстония ( лат. Alstonia ), Аспидосперма ( лат. Aspidosperma ), Раувольфия ( лат. Rauvolfia ) и Катарантус ( лат. Catharanthus ); Мареновые ( лат. Rubiaceae ) — 72 вида , в частности, род Коринанте ( лат. Corynanthe ), и Логаниевые ( лат. Loganiaceae ) — 40 видов , в частности, род Стрихнос ( лат. Strychnos ) . Довольно богато индольными алкалоидами и семейство Бобовые ( Fabaceae ), в котором 63 вида содержат алкалоиды этой группы, но здесь они в основном простые по строению .
Среди грибов, содержащих индольные алкалоиды, можно выделить род Псилоцибе ( лат. Psilocybe ), представители которого содержат простые производные триптамина, а также род Спорынья ( лат. Claviceps ), представители которого богаты производными лизергиновой кислоты .
Индольные алкалоиды играют роль также и в организмах животных . В коже многих видов жаб рода Bufo обнаружено производное триптамина — буфотенин , а в коже колорадской жабы Bufo alvarius — 5-MeO-DMT . Серотонин , важный нейромедиатор у млекопитающих, также может быть отнесён к простейшим индольным алкалоидам.
-
Гармала , содержащая β-карболиновые алкалоиды
-
содержит алкалоиды типа Corynanthe
-
Раувольфия змеиная содержит алкалоиды типа Corynanthe
-
Катарантус розовый содержит монотерпеноидные индольные алкалоиды
-
 Спорынья содержит производные лизергиновой кислоты
Спорынья содержит производные лизергиновой кислоты
Биосинтез
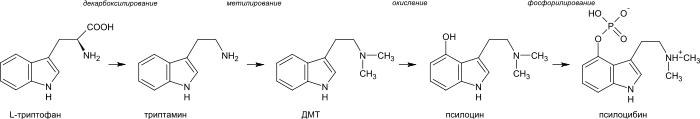
Биогенетическим предшественником всех индольных алкалоидов является аминокислота триптофан . Для большинства из них первым шагом является декарбоксилирование триптофана с образованием триптамина . Диметилтриптамин (ДМТ) образуется из триптамина посредством метилирования при участии кофермента S-аденозилметионина (SAM). Псилоцин образуется из диметилтриптамина посредством окисления и в дальнейшем фосфорилируется до псилоцибина .

При биосинтезе серотонина промежуточным соединением является не триптамин, а 5-гидрокситриптофан , который уже в свою очередь декарбоксилируется с образованием 5-гидрокситриптамина (серотонина) .

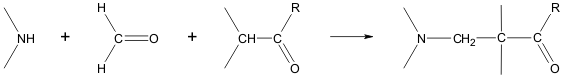
Биосинтез β-карболиновых алкалоидов происходит посредством образования основания Шиффа из триптамина и альдегида (или кетокислоты ) и последующей внутримолекулярной реакции Манниха , где атом углерода C 2 индольного ядра выступает в роли нуклеофила . После этого ароматичность восстанавливается с потерей протона при атоме углерода C 2 . Получившийся тетрагидро-β-карболиновый скелет затем последовательно окисляется до дигидро-β-карболинового и β-карболинового. При образовании простых β-карболиновых алкалоидов, таких как гармин и гармалин роль кетокислоты выполняет пировиноградная кислота . При синтезе монотерпеноидных индольных алкалоидов в качестве альдегида участвует . Пирролоиндольные алкалоиды синтезируются в живых организмах аналогичным способом .

Биосинтез алкалоидов спорыньи начинается с алкилирования триптофана ( англ. ), при этом атом углерода C 4 индольного ядра играет роль нуклеофила. Образовавшийся 4-диметилаллил-L-триптофан подвергается N-метилированию. Дальнейшими ступенями биосинтеза являются ханоклавин-I и агроклавин. Последний гидроксилируется до элимоклавина, который в свою очередь окисляется до . В процессе паспаловая кислота преобразуется в лизергиновую кислоту .

Биосинтез монотерпеноидных индольных алкалоидов начинается реакцией Манниха с участием триптамина и секологанина, в результате которой образуется , преобразуемый в дальнейшем в 4,21-дегидрогейсошизин. Далее биосинтез большинства алкалоидов с неперегруппированной монотерпеноидной частью (типа Corynanthe) продолжается посредством циклизации с образованием катенамина и последующего восстановления до аймалицина в присутствии никотинамидадениндинуклеотидфосфата (NADPH). При биосинтезе других алкалоидов 4,21-дегидрогейсошизин сначала преобразуется в преакуамицин, алкалоид подтипа Strychnos типа Corynanthe, из которого в свою очередь образуются другие алкалоиды подтипа Strychnos, а также алкалоиды типов Iboga и Aspidosperma. Бисиндольные алкалоиды винбластин и винкристин получаются в процессе реакции, вовлекающей катарантин (алкалоид типа Iboga) и виндолин (алкалоид типа Aspidosperma) .

Физиологическая активность
Многие индольные алкалоиды обладают заметной физиологической активностью. Большая часть физиологических эффектов индольных алкалоидов связана с их действием на центральную и периферическую нервные системы. Кроме того, бисиндольные алкалоиды винбластин , винкристин и фаскаплизин обладают противоопухолевым эффектом .
Действие на аминергические системы

Благодаря структурному сходству с серотонином многие триптамины способны взаимодействовать с серотониновыми (5-HT) рецепторами . Так, основной эффект классических галлюциногенов , таких как ДМТ , псилоцин и псилоцибин , связан с тем, что эти вещества являются агонистами по отношению к 5-HT 2A рецепторам . Галлюциногенные эффекты ибогаина также связывают с подобным действием . Грамин , напротив, является антагонистом 5-HT 2A -рецепторов .
Производные лизергиновой кислоты включают в свой состав структурные элементы как триптамина , так и фенилэтиламина , что позволяет им действовать как на 5-HT рецепторы, так и на адренорецепторы (в основном типа α) и дофаминовые рецепторы (главным образом типа D 2 ) . Так, эрготамин является частичным агонистом α-адренорецепторов и 5-HT 2 -рецепторов, благодаря чему обладает сосудосуживающим действием и стимулирует сокращения матки . Дигидроэрготамин обладает большей селективностью в отношении α-адренорецепторов и меньшим действием на серотониновые рецепторы. Эргометрин является агонистом α-адренорецепторов и 5-HT 2 -рецепторов и частичным агонистом D 2 -рецепторов . По сравнению с другими алкалоидами спорыньи эргометрин обладает большей селективностью в отношении стимуляции матки . ЛСД , синтетическое производное лизергиновой кислоты, является агонистом 5-HT 2A - и 5-HT 1A -рецепторов, а также, в меньшей степени, D 2 -рецепторов и обладает мощным галлюциногенным эффектом .
Некоторые монотерпеноидные индольные алкалоиды также взаимодействуют с адренорецепторами. Например, аймалицин (раубазин) является селективным антагонистом α 1 -адренорецепторов, благодаря чему обладает антигипертензивным эффектом . Йохимбин же более селективен в отношении α 2 -адренорецепторов . Благодаря блокированию пресинаптических α 2 -адренорецепторов йохимбин увеличивает выброс норадреналина , что приводит к повышению кровяного давления. Йохимбин применялся для лечения эректильной дисфункции у мужчин до появления более совершенных препаратов .
Некоторые алкалоиды влияют на оборот моноаминов косвенным образом. Так, гармин и гармалин являются обратимыми селективными ингибиторами моноаминоксидазы-A . Резерпин опустошает запасы моноаминов в пресинаптических нейронах, уменьшая их концентрацию в синапсе , следствием чего является его антигипертензивное и антипсихотическое действия .
Действие на другие системы
Некоторые индольные алкалоиды взаимодействуют и с другими типами рецепторов. Так, митрагинин является агонистом μ-опиоидных рецепторов . Алкалоиды гармалы являются антагонистами к ГАМК А -рецепторам , а ибогаин — к NMDA-рецепторам .
Физостигмин является обратимым ингибитором ацетилхолинэстеразы .
Применение
Применения индольных алкалоидов и их синтетических аналогов связаны с их физиологической активностью.
Медицинское применение
Растения и грибы, содержащие индольные алкалоиды, имеют давнюю историю применения в народной медицине . Раувольфия змеиная , действующим веществом которой является резерпин , на протяжении более 3000 лет применялась в Индии в качестве средства от змеиных укусов и для лечения сумасшествия . В средневековой Европе микстуры , содержащие рожки спорыньи , использовались для медикаментозных абортов .
Позднее чистые препараты индольных алкалоидов также стали использоваться в медицине. Уже упоминавшийся резерпин был вторым (после хлорпромазина ) принятым к применению антипсихотиком , однако его использование для этой цели было ограничено низким терапевтическим индексом и сильно выраженными побочными эффектами. В настоящее время в качестве антипсихотика резерпин не применяется , но иногда используется в качестве антигипертензивного средства, чаще в комбинации с другими действующими веществами .
К другим препаратам, влияющим на сердечно-сосудистую систему относятся аймалин , являющийся антиаритмическим средством класса I , и аймалицин (раубазин), используемый в Европе в качестве антигипертензивного средства . Физостигмин, ингибитор ацетилхолинэстеразы , используется для уменьшения глазного давления при глаукоме , а его синтетические аналоги применяются при болезни Альцгеймера ( ривастигмин ) и миастении ( неостигмин , пиридостигмин , дистигмин ) .
Алкалоиды спорыньи эргометрин (эргобазин, эргоновин) и эрготамин , а также их синтетические производные, такие как метилэргометрин применяются при маточных кровотечениях . Бисиндольные алкалоиды винбластин и винкристин используются в качестве противоопухолевых средств .
Исследования на животных показали, что ибогаин может быть эффективен при лечении героиновой , кокаиновой и алкогольной зависимостей , а также облегчать симптомы отмены опиоидов . Это действие связывают в основном с антагонизмом ибогаина по отношению к NMDA-рецепторам . Медицинскому применению ибогаина в значительной степени препятствует его юридический статус (во многих странах он запрещён как мощный галлюциноген с опасными последствиями передозировки), однако в Европе и США существуют «подпольные» сети, предоставляющие медицинские услуги наркоманам .
Немедицинское применение

Природные источники некоторых индольных алкалоидов с древних времён используются в качестве галлюциногенов . К ним относятся, в частности, галлюциногенные грибы рода Псилоцибе , употреблявшиеся ещё ацтеками . Другим давно применяемым галлюциногеном является айяуаска — южноамериканский психотропный чай, приготовляемый из растений Psychotria viridis и Banisteriopsis caapi . Первое из них богато диметилтриптамином (ДМТ), являющимся галлюциногеном, а второе содержит большое количество β-карболиновых алкалоидов ( гармин , гармалин , тетрагидрогармин) — ингибиторов моноаминоксидазы . Считается, что основное действие β-карболинов в айяуаске сводится к предотвращению метаболизации ДМТ в пищеварительном тракте и печени , благодаря чему он получает возможность преодолеть гематоэнцефалический барьер . Прямое действие β-карболинов на центральную нервную систему минимально . Яд жаб Bufo Alvarius , содержащий 5-MeO-DMT , также используется с целью испытания галлюцинаций .
Из полусинтетических триптаминов широко применяется диэтиламид лизергиновой кислоты ( ЛСД ) — сильный галлюциноген, эффективный в дозах 30—40 мкг при пероральном употреблении .
Примечания
- ↑ Кнунянц И. Л. Индольные алкалоиды // . — М. : Советская энциклопедия, 1988. — 623 с. 27 июля 2011 года.
- David S. Seigler. . — Springer, 2001. — С. 628. — 776 с. — ISBN 0412019817 .
- Paul M Dewick. . — Wiley, 2002. — С. 348—367. — 515 с. — ISBN 0471496405 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 333—335. — 414 с. — ISBN 978-3-906390-24-6 .
- ↑ Manfred Hesse. . — Wiley-VCH, 2002. — С. 316. — 414 с. — ISBN 978-3-906390-24-6 .
- Орехов А. П. Химия алкалоидов. — Изд.2. — М. : АН СССР, 1955. — С. 616. — 859 с.
- Л. Эльдерфилд. Гетероциклические соединения. — М. : Издательство иностранной литературы, 1954. — Т. 3. — С. 5.
- Paul M Dewick. . — Wiley, 2002. — С. 346—376. — 515 с. — ISBN 0471496405 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 14—30. — 414 с. — ISBN 978-3-906390-24-6 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 91—92. — 414 с. — ISBN 978-3-906390-24-6 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 15. — 414 с. — ISBN 978-3-906390-24-6 .
- Leland J. Cseke et al. . — CRC, 2006. — С. 30. — 569 с. — ISBN 0-8493-2976-0 .
- ↑ Paul M Dewick. . — Wiley, 2002. — С. 347. — 515 с. — ISBN 0471496405 .
- ↑ Paul M Dewick. . — Wiley, 2002. — С. 350. — 515 с. — ISBN 0471496405 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 16. — 414 с. — ISBN 978-3-906390-24-6 .
- Paul M Dewick. . — Wiley, 2002. — С. 349. — 515 с. — ISBN 0471496405 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 22. — 414 с. — ISBN 978-3-906390-24-6 .
- Орехов А. П. Химия алкалоидов. — Изд.2. — М. : АН СССР, 1955. — С. 565. — 859 с.
- Paul M Dewick. . — Wiley, 2002. — С. 365—366. — 515 с. — ISBN 0471496405 .
- Орехов А. П. Химия алкалоидов. — Изд.2. — М. : АН СССР, 1955. — С. 601. — 859 с.
- Paul M Dewick. . — Wiley, 2002. — С. 370—372. — 515 с. — ISBN 0471496405 .
- ↑ Орехов А. П. Химия алкалоидов. — Изд.2. — М. : АН СССР, 1955. — С. 627. — 859 с.
- Paul M Dewick. . — Wiley, 2002. — С. 351. — 515 с. — ISBN 0471496405 .
- ↑ Paul M Dewick. . — Wiley, 2002. — С. 350—359. — 515 с. — ISBN 0471496405 .
- ↑ Hiromitsu Takayama. // Chem. Pharm. Bull. — 2004. — Т. 52 , № 8 . — С. 916—928 . 4 марта 2009 года.
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 30. — 414 с. — ISBN 978-3-906390-24-6 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 91—105. — 414 с. — ISBN 978-3-906390-24-6 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 99. — 414 с. — ISBN 978-3-906390-24-6 .
- ↑ Monika Waksmundzka-Hajnos, Joseph Sherma, Teresa Kowalska. . — CRC Press, 2008. — С. 625—626. — 865 с. — ISBN 978-1-4200-4677-9 .
- Tadeusz Aniszewski. . — Amsterdam: Elsevier, 2007. — С. 39. — 335 с. — ISBN 978-0-444-52736-3 .
- ↑ Блинова К. Ф. и др. / Под (недоступная ссылка) ред. К. Ф. Блиновой, Г. П. Яковлева. — М. : Высш. шк., 1990. — С. 10. — ISBN 5-06-000085-0 . 20 апреля 2014 года. . Дата обращения: 31 марта 2012. Архивировано 20 апреля 2014 года.
- Monika Waksmundzka-Hajnos, Joseph Sherma, Teresa Kowalska. . — CRC Press, 2008. — С. 626. — 865 с. — ISBN 978-1-4200-4677-9 .
- Tadeusz Aniszewski. . — Amsterdam: Elsevier, 2007. — С. 37—39. — 335 с. — ISBN 978-0-444-52736-3 .
- Michael E. Peterson, Patricia A. Talcott. . — Saunders, 2005. — С. 1086. — 1190 с. — ISBN 0721606393 .
- Monika Waksmundzka-Hajnos, Joseph Sherma, Teresa Kowalska. . — CRC Press, 2008. — С. 625. — 865 с. — ISBN 978-1-4200-4677-9 .
- Paul M Dewick. . — Wiley, 2002. — С. 349, 365. — 515 с. — ISBN 0471496405 .
- Paul M Dewick. . — Wiley, 2002. — С. 369—370. — 515 с. — ISBN 0471496405 .
- Tadhg P. Begley. . — Wiley, 2009. — С. —7. — 3188 с. — ISBN 978-0-471-75477-0 .
- Paul M Dewick. . — Wiley, 2002. — С. 356. — 515 с. — ISBN 0471496405 .
- Deborah M. Roll, Chris M. Ireland, Helen S. M. Lu, Jon Clardy. (англ.) // The Journal of Organic Chemistry. — 1988-07. — Vol. 53 , iss. 14 . — P. 3276–3278 . — ISSN . — doi : . 26 мая 2021 года.
- Richard A. Glennon. Strategies for the Development of Selective Serotonergic Agents // . — Humana Press, 2006. — С. 96. — 618 с. — ISBN 1-58829-568-0 .
- Richard A. Glennon. Neurobiology of Hallucinogens // . — American Psychiatric Publishing, 2008. — С. 183. — 616 с. — ISBN 978-1-58562-276-4 .
- Kenneth R. Alper. Ibogaine: a Review // The Alkaloids. — Academic Press, 2001. — С. 8. — ISBN 0120532069 .
- Froldi Guglielmina; Silvestrin Barbara; Dorigo Paola; Caparrotta Laura. // Planta medica. — 2004. — Т. 70 , № 4 . — С. 373—375 . 11 сентября 2012 года.
- Paul M Dewick. . — Wiley, 2002. — С. 374—375. — 515 с. — ISBN 0471496405 .
- ↑ B. T. Larson et al. // J Anim Sci. — 1995. — Т. 73 . — С. 1396—1400 . (недоступная ссылка)
- ↑ Bertram G. Katzung. . — McGraw-Hill Medical, 2009. — С. 272. — 1200 с. — ISBN 0071604057 . (недоступная ссылка)
- Torsten Passie et al. // CNS Neuroscience & Therapeutics. — 2008. — Т. 14 . — С. 295—314 . 5 марта 2014 года.
- Philip Seeman. (англ.) (9 июля 2004). Дата обращения: 31 октября 2009. 14 августа 2011 года.
- ↑ Paul M Dewick. . — Wiley, 2002. — С. 353. — 515 с. — ISBN 0471496405 .
- ↑ P. Demichel et al. // J Pharmacol. — 1982. — Т. 77 , № 3 . — С. 449—454 .
- Bertram G. Katzung. . — McGraw-Hill Medical, 2009. — С. 145. — 1200 с. — ISBN 0071604057 . (недоступная ссылка)
- Andreas Moser. . — Braun-Brumfield, 1998. — С. 138. — ISBN 3-7643-3993-4 .
- Andreas Moser. . — Braun-Brumfield, 1998. — С. 131. — ISBN 3-7643-3993-4 .
- Kenneth R. Alper. Ibogaine: a Review // The Alkaloids. — Academic Press, 2001. — С. 7. — ISBN 0120532069 .
- Paul M Dewick. . — Wiley, 2002. — С. 367. — 515 с. — ISBN 0471496405 .
- Paul M Dewick. . — Wiley, 2002. — С. 352. — 515 с. — ISBN 0471496405 .
- Manfred Hesse. . — Wiley-VCH, 2002. — С. 332—333. — 414 с. — ISBN 978-3-906390-24-6 .
- Alan F. Schatzberg, Charles B. Nemeroff. . — The American Psychiatric Publishing, 2009. — С. 533. — 1648 с. — ISBN 9781585623099 .
- . Энциклопедия лекарств и товаров аптечного ассортимента . РЛС Патент. — Инструкция, применение и формула.
- . Энциклопедия лекарств и товаров аптечного ассортимента . РЛС Патент. — Инструкция, применение и формула.
- Paul M Dewick. . — Wiley, 2002. — С. 367—368. — 515 с. — ISBN 0471496405 .
- . Энциклопедия лекарств и товаров аптечного ассортимента . РЛС Патент. — Инструкция, применение и формула.
- . Энциклопедия лекарств и товаров аптечного ассортимента . РЛС Патент. — Инструкция, применение и формула.
- Kenneth R. Alper. Ibogaine: a Review // The Alkaloids. — Academic Press, 2001. — С. 2—19. — ISBN 0120532069 .
- Paul M Dewick. . — Wiley, 2002. — С. 357. — 515 с. — ISBN 0471496405 .
- Paul M Dewick. . — Wiley, 2002. — С. 348. — 515 с. — ISBN 0471496405 .
- Jordi Riba et al. // Journal of Pharmacology And Experimental Therapeutics. — 2003. — Т. 306 , № 1 . — С. 73—83 . 13 февраля 2009 года.
- Weil AT, Davis W. // J Ethnopharmacol. — 1994. — Т. 41 , № 1—2 . — С. 1—8 . 29 октября 2012 года.
- Paul M Dewick. . — Wiley, 2002. — С. 376. — 515 с. — ISBN 0471496405 .
Литература
- Орехов А. П. Химия алкалоидов. — 2-е изд. — М. : АН СССР, 1955. — 859 с.
- Племенков В. В. Введение в химию природных соединений. — Казань, 2001. — 376 с.
- Tadeusz Aniszewski. Alkaloids — secrets of life. — Amsterdam: Elsevier, 2007. — 335 с. — ISBN 978-0-444-52736-3 .
- Manfred Hesse. . — Wiley-VCH, 2002. — 414 с. — ISBN 978-3-906390-24-6 .
- Paul M Dewick. . — Wiley, 2002. — 515 с. — ISBN 0471496405 .
- 2020-05-28
- 1