Interested Article - Xist

- 2021-02-01
- 1
Xist ( англ. X-inactive specific transcript) — ген , кодирующий РНК и локализованный на Х-хромосоме плацентарных млекопитающих , является ключевым эффектором в инактивации Х-хромосомы . Он входит в состав комплекса Xic ( англ. X-chromosome inactivation centre) , наряду с двумя другими РНК-кодирующими генами ( и ) и двумя белоккодирующими генами ( Tsx и Cnbp2 ) . Продукт гена Xist — Xist-РНК — представляет собой крупный транскрипт (17 кб у человека ) , который экспрессируется на неактивной хромосоме и не экспрессируется на активной. Процессинг этого транскрипта напоминает процессинг мРНК и тоже включает этапы сплайсинга (в т. ч. альтернативного ) и полиаденилирования , однако он остаётся в ядре и не транслируется . Было высказано предположение, что ген Xist по крайней мере частично образовался как часть белоккодирующего гена, который впоследствии стал псевдогеном . Инактивированная Х-хромосома покрыта Xist-РНК, который необходим для процесса инактивации . Х-хромосома, лишённая гена Xist, не будет инактивирована, однако дупликация этого гена на другой хромосоме вызывает инактивацию и первой хромосомы тоже .
Инактивация Х-хромосомы, которая происходит на ранних стадиях развития самок плацентарных млекопитающих, обеспечивает сайленсинг на уровне транскрипции одной из двух Х-хромосом, что обеспечивает дозовое равенство (т. е. по количеству активных вариантов одного гена) самок и самцов (см. подробнее « Дозовая компенсация »). Функциональная роль Xist-РНК была наглядно продемонстрирована на эмбриональных стволовых клетках самок мышей . В ходе этих экспериментов введение в клетки антисмысловой РНК длиной 19 нуклеотидов, мишенью которой была Xist-РНК, предотвращало образование Xic и цис -сайленсинг Х-связанных генов. Впрочем, в дальнейшем было показано, что инактивация Х-хромосомы у мышей всё-таки происходит даже в отсутствие гена Xist посредством эпигенетической регуляции, но Xist-РНК необходима для стабилизации такого сайленсинга .
Было показано, что ген Xist взаимодействует с геном BRCA1 , связанным с раком молочной железы .
Организация гена
У человека ген Xist локализован на длинном (q) плече Х-хромосомы. Он включает в себя большое количество повторов и состоит из А-региона, содержащего 8 повторов , разделённых U- спейсерами . А-регион содержит две крупные шпильки , в каждую из которых входит по 4 повтора . Ортолог гена Xist у человека был идентифицирован у мыши, его длина составляет 15 кб, однако он не содержит консервативных повторов .
Организация транскрипта
Xist-РНК состоит из двух регионов: А и С. Консервативный А-регион содержит до 9 повторяющихся элементов . Недавно было показано, что у мыши и человека А-регион Xist-РНК состоит из двух длинных шпилек, в состав каждой из которых входит по 4 повтора . Хотя конкретная функция А-региона неизвестна, было показано, что он необходим для эффективного связывания с белком .
Связывание Xist-РНК с инактивированной Х-хромосомой осуществляется через хроматин -связывающий участок, расположенный на самом транскрипте. Впервые такой участок на Xist-РНК был описан в фибробластах самки мыши. Он оказался локализованным в области С-повтора. Вышеописанные эксперименты по введению в клетки 19-нуклеотидной антисмысловой РНК, комплементарной Xist, нарушали связывание этого транскрипта с гистоном .
Регуляция Xist
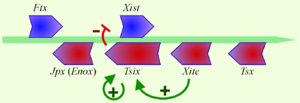
Как упоминалось выше, ген Xist-РНК входит в состав инактивационного центра Xic ( англ. X Inactivation Center) . Xic локализуется на q-плече Х-хромосомы (Xq13). Ключевую роль в инактивации Х-хромосомы играет промотор Xist, входящий в состав Xiс . Кроме гена Xist, в Xic входит также ген , антисмысловой по отношению к Xist. Антисмысловые транскрипты гена Xist действуют как цис -регуляторы транскрипции Xist, понижая экспрессию этого гена. Механизм такой цис -регуляции экспрессии Xist с помощью Tsix пока плохо понятен, хотя существует несколько объясняющих гипотез. Согласно одной из них, Tsix участвует в модификации хроматина в локусе Xist (подробнее об этом см. ниже).
Предполагается, что антисмысловой транскрипт Tsix активирует ДНК-метилтрансферазы , которые метилируют промотор Xist, что приводит к подавлению этого промотора и, следовательно, экспрессии гена Xist . Показана роль ацетилирования гистонов в регуляции Xist .
Возможно, двуцепочечные РНК и интерферирующие РНК также играют роль в регуляции промотора Xist. По-видимому, фермент Dicer , специализирующийся на разрезании двуцепочечных РНК, разрезает дуплекс Xist и Tsix в начале процесса инактивации Х-хромосомы, в результате чего образуются короткие РНК длиной около 30 нуклеотидов (xiРНК). Предполагается, что эти xiРНК репрессируют Xist на той Х-хромосоме, которая останется активной. Это предположение подтверждается экспериментом, в ходе которого в недифференцированных клетках количество эндогенного Dicer было снижено на 5 %, что привело к увеличению Xist в этих клетках .
По-видимому, транскрипционные факторы плюрипотентных клеток Nanog , Oct4 и играют роль в сайленсинге гена Xist. В отсутствие Tsix в плюрипотентных клетках Xist, тем не менее, тоже репрессирован. Возможным объяснением этому может быть то, что вышеперечисленные факторы вызывают сплайсинг по интрону 1 в сайте связывания этих факторов в гене Xist, в результате чего сайт разрушается и экспрессия Xist подавляется . В плюрипотентных клетках, лишённых Nanog или Oct4, уровень экспрессии Xist повышался .
Была показана роль ( англ. Polycomb Repressor Complex 2 (PRC2)) в сайленсинге Xist независимо от Tsix, хотя конкретные механизмы этого неизвестны. PRC2 — это класс белков группы polycomb , которые вызывают три метилирование гистона по остатку лизина 27 (К27), что подавляет транскрипцию путём перестройки хроматина. Вышеупомянутый белок Suz12 входит в группу PRC2 и имеет домен цинкового пальца , который, по-видимому, связывается с молекулой РНК .
Значение и механизмы инактивации
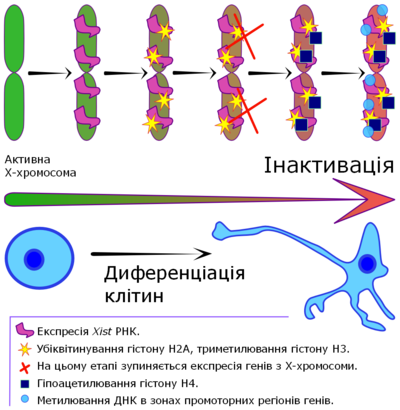
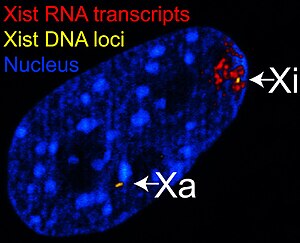
Процесс инактивации Х-хромосомы начинается с распространением Xist-РНК от Xic по всей хромосоме , где Xist-РНК, по-видимому, индуцирует образование и расширение области гетерохроматина . Гетерохроматин инактивированной Х-хромосомы характеризуется не только связью с Xist-РНК, но также наличием особого варианта гистона Н2А (macroH2A), гипо гистонов Н3 и , убиквитинированием гистона H2А и метилированием специфических позиций на гистоне Н3, а также метилирования ДНК. Именно комбинация подобных модификаций обусловливает большую часть инактивированной Х-хромосомы чрезвычайно невосприимчивой к транскрипции. Кроме того, способность этих модификаций к самораспространению обеспечивает поддержание инактивированного состояния Х-хромосомы в течение многих клеточных делений . Впрочем, стоит отметить, около 10 % генов на Х-хромосоме остаются транскрипционно активными .
Экспрессия Xist и инактивация Х-хромосомы изменяются в процессе эмбрионального развития . У мыши в раннем эмбриональном развитии существует две волны инактивации Х-хромосомы. Первая волна происходит до образования бластоцисты, и является неслучайной — в клетках зародыша инактивируется Х-хромосома, полученная от отца, то есть инактивация Х-хромосомы на этом этапе носит импринтированный характер. На стадии бластоцисты , в клетках внутренней клеточной массы , из которой формируются в дальнейшем все органы и ткани будущего организма, этот импринтинг снимается, экспрессия Xist исчезает, инактивация отцовской Х-хромосомы отменяется, и обе Х-хромосомы становятся транскрипционно активными. Недавно полученные данные показали, что в процессе реактивации Х-хромосомы участвуют антисмысловые транскрипты . В формирующихся далее клетках эпибласта начинается процесс дифференцировки , и наступает вторая волна инактивации, в которой выбор инактивируемой Х-хромосомы носит случайный характер. На одной из Х-хромосом начинает экспрессироваться Xist, и эта Х-хромосома вступает в процесс инактивации. Вследствие случайного выбора инактивируемой Х-хромосомы каждый женский организм представляет собой мозаику из клональных групп клеток, у которых либо инактивирована Х-хромосома, доставшаяся от отца, либо Х-хромосома, оставшаяся от матери. Инактивация Х-хромосомы поддерживается в течение тысячи клеточных делений , и только в развивающихся гоноцитах экспрессия Xist снижается и Х-хромосома вновь реактивируется . В экстраэмбриональных тканях у мыши импринтированная инактивация отцовской Х-хромосомы, установившаяся во время первой волны инактивации, сохраняется в течение всего эмбрионального развития.
Инактивация Х-хромосомы играет ключевую роль в механизме дозовой компенсации , благодаря которому обеспечивается равенство доз генных продуктов Х-хромосомы у обоих полов . У различных видов дозовая компенсация обеспечивается различными путями, но во всех таких путях имеет место регуляции экспрессии Х-хромосомы у одного из двух обоих полов . Если одна из двух Х-хромосом не будет инактивирована или будет частично экспрессироваться, то получающаяся в результате избыточная экспрессия Х-хромосомы может быть летальной .
Клиническое значение
У человека мутации в промоторе Xist обусловливают семейную .
В 2013 году было показано, что внедрение гена Xist в одну из 21-х хромосом стволовой клетки с трисомией по 21-ой хромосоме (причина синдрома Дауна ) позволяет инактивировать эту хромосому. Таким образом, ген Xist может лечь в основу нового подхода к лечению синдрома Дауна .
Примечания
- ↑ - Ensembl , May 2017
- ↑ - Ensembl , May 2017
- (неопр.) Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- (неопр.) Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ↑ (неопр.) . 5 декабря 2010 года.
- Chow J. C. , Yen Z. , Ziesche S. M. , Brown C. J. (англ.) // Annual review of genomics and human genetics. — 2005. — Vol. 6. — P. 69—92. — doi : . — . [ ]
- Chureau C. , Prissette M. , Bourdet A. , Barbe V. , Cattolico L. , Jones L. , Eggen A. , Avner P. , Duret L. (англ.) // Genome research. — 2002. — Vol. 12, no. 6 . — P. 894—908. — doi : . — . [ ]
- ↑ Brown C. J. , Hendrich B. D. , Rupert J. L. , Lafrenière R. G. , Xing Y. , Lawrence J. , Willard H. F. (англ.) // Cell. — 1992. — Vol. 71, no. 3 . — P. 527—542. — . [ ]
- Duret L. , Chureau C. , Samain S. , Weissenbach J. , Avner P. (англ.) // Science (New York, N.Y.). — 2006. — Vol. 312, no. 5780 . — P. 1653—1655. — doi : . — . [ ]
- Ng K. , Pullirsch D. , Leeb M. , Wutz A. (англ.) // EMBO reports. — 2007. — Vol. 8, no. 1 . — P. 34—39. — doi : . — . [ ]
- Penny G. D. , Kay G. F. , Sheardown S. A. , Rastan S. , Brockdorff N. (англ.) // Nature. — 1996. — Vol. 379, no. 6561 . — P. 131—137. — doi : . — . [ ]
- Kalantry S. , Purushothaman S. , Bowen R. B. , Starmer J. , Magnuson T. (англ.) // Nature. — 2009. — Vol. 460, no. 7255 . — P. 647—651. — doi : . — . [ ]
- Ganesan S. , Silver D. P. , Drapkin R. , Greenberg R. , Feunteun J. , Livingston D. M. (англ.) // Philosophical transactions of the Royal Society of London. Series B, Biological sciences. — 2004. — Vol. 359, no. 1441 . — P. 123—128. — doi : . — . [ ]
- Ganesan S. , Silver D. P. , Greenberg R. A. , Avni D. , Drapkin R. , Miron A. , Mok S. C. , Randrianarison V. , Brodie S. , Salstrom J. , Rasmussen T. P. , Klimke A. , Marrese C. , Marahrens Y. , Deng C. X. , Feunteun J. , Livingston D. M. (англ.) // Cell. — 2002. — Vol. 111, no. 3 . — P. 393—405. — . [ ]
- ↑ Maenner S. , Blaud M. , Fouillen L. , Savoye A. , Marchand V. , Dubois A. , Sanglier-Cianférani S. , Van Dorsselaer A. , Clerc P. , Avner P. , Visvikis A. , Branlant C. (англ.) // Public Library of Science Biology. — 2010. — Vol. 8, no. 1 . — P. e1000276. — doi : . — . [ ]
- Brockdorff N. , Ashworth A. , Kay G. F. , McCabe V. M. , Norris D. P. , Cooper P. J. , Swift S. , Rastan S. (англ.) // Cell. — 1992. — Vol. 71, no. 3 . — P. 515—526. — . [ ]
- Beletskii A. , Hong Y. K. , Pehrson J. , Egholm M. , Strauss W. M. (англ.) // Proceedings of the National Academy of Sciences of the United States of America. — 2001. — Vol. 98, no. 16 . — P. 9215—9220. — doi : . — . [ ]
- Herzing L. B. , Romer J. T. , Horn J. M. , Ashworth A. (англ.) // Nature. — 1997. — Vol. 386, no. 6622 . — P. 272—275. — doi : . — . [ ]
- Lee J. T. , Davidow L. S. , Warshawsky D. (англ.) // Nature genetics. — 1999. — Vol. 21, no. 4 . — P. 400—404. — doi : . — . [ ]
- ↑ Senner C. E. , Brockdorff N. (англ.) // Current opinion in genetics & development. — 2009. — Vol. 19, no. 2 . — P. 122—126. — doi : . — . [ ]
- Nesterova T. B. , Popova B. C. , Cobb B. S. , Norton S. , Senner C. E. , Tang Y. A. , Spruce T. , Rodriguez T. A. , Sado T. , Merkenschlager M. , Brockdorff N. (англ.) // Epigenetics & chromatin. — 2008. — Vol. 1, no. 1 . — P. 2. — doi : . — . [ ]
- Csankovszki G. , Nagy A. , Jaenisch R. (англ.) // The Journal of cell biology. — 2001. — Vol. 153, no. 4 . — P. 773—784. — . [ ]
- Ogawa Y. , Sun B. K. , Lee J. T. (англ.) // Science (New York, N.Y.). — 2008. — Vol. 320, no. 5881 . — P. 1336—1341. — doi : . — . [ ]
- Navarro P. , Chambers I. , Karwacki-Neisius V. , Chureau C. , Morey C. , Rougeulle C. , Avner P. (англ.) // Science (New York, N.Y.). — 2008. — Vol. 321, no. 5896 . — P. 1693—1695. — doi : . — . [ ]
- de Napoles M. , Mermoud J. E. , Wakao R. , Tang Y. A. , Endoh M. , Appanah R. , Nesterova T. B. , Silva J. , Otte A. P. , Vidal M. , Koseki H. , Brockdorff N. (англ.) // Developmental cell. — 2004. — Vol. 7, no. 5 . — P. 663—676. — doi : . — . [ ]
- ↑ , с. 729.
- Mak W. , Nesterova T. B. , de Napoles M. , Appanah R. , Yamanaka S. , Otte A. P. , Brockdorff N. (англ.) // Science (New York, N.Y.). — 2004. — Vol. 303, no. 5658 . — P. 666—669. — doi : . — . [ ]
- Nesterova T. B. , Mermoud J. E. , Hilton K. , Pehrson J. , Surani M. A. , McLaren A. , Brockdorff N. (англ.) // Differentiation; research in biological diversity. — 2002. — Vol. 69, no. 4-5 . — P. 216—225. — doi : . — . [ ]
- ↑ Nguyen D. K. , Disteche C. M. (англ.) // Nature genetics. — 2006. — Vol. 38, no. 1 . — P. 47—53. — doi : . — . [ ]
- Jiang J. , Jing Y. , Cost G. J. , Chiang J. C. , Kolpa H. J. , Cotton A. M. , Carone D. M. , Carone B. R. , Shivak D. A. , Guschin D. Y. , Pearl J. R. , Rebar E. J. , Byron M. , Gregory P. D. , Brown C. J. , Urnov F. D. , Hall L. L. , Lawrence J. B. (англ.) // Nature. — 2013. — Vol. 500, no. 7462 . — P. 296—300. — doi : . — . [ ]
Литература
- Б. Альбертс, А. Джонсон, Д. Льюис и др. Молекулярная биология клетки / Перевод с английского - А.Н. Дьяконовой, А.В. Дюбы и А.А. Светлова. Под ред. - Е.С. Шилова, Б.П. Копнина, М.А. Лагарьковой, Д.В. Купраша.. — М.—Ижевск: НИЦ «Регулярная и хаотическая динамика», 2013. — Т. 1. — С. 1213. — 1052 с. — ISBN 978-5-4344-0112-8 .
- Шевченко А. И., Захарова И. С., Закиян С. М. // Acta Naturae. — 2013. — Т. 5 , № 2 . — С. 40-54 .
Ссылки
- Кочанова, Наталья. (неопр.) . // Сайт Biomolecula.ru (21 октября 2013). Дата обращения: 21 марта 2018.
- 2021-02-01
- 1
















