Interested Article - Тиосульфат аммония

- 2021-07-13
- 1
Тиосульфа́т аммо́ния ( гипосульфит аммония , аммоний серноватистокислый ) — неорганическое соединение , соль аммония и тиосерной кислоты с формулой (NH 4 ) 2 SO 3 S, бесцветные кристаллы, растворимые в воде. Применяется в фотографии как основной компонент быстрых фиксажей .
Получение
- Медленная реакция суспензии серы с раствором гидрата аммония :
- Медленное окисление на воздухе гидросульфида аммония :
- Слияние горячих растворов гидросульфида аммония и гидросульфита аммония :
Физические свойства
Тиосульфат аммония образует бесцветные кристаллы с запахом аммиака, хорошо растворимые в воде, слабо растворимые в ацетоне , не растворяются в этаноле .
Химические свойства
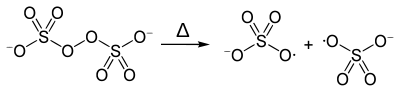
- Разлагается при нагревании с образованием смеси продуктов:
- Медленно разлагается в разбавленных растворах:
- Разлагается концентрированными кислотами:
- и горячими разбавленными кислотами:
- Реагирует с галогенами :
Как и тиосульфат натрия , реагирует с галогенидами серебра, образуя растворимые комплексы, что позволяет осуществлять процесс фиксирования при обработке фотографических материалов. В отличие от тиосульфата натрия, который позволяет достигать концентрации 6 г. серебра на литр раствора, тиосульфат аммония позволяет почти удвоить это количество, снижая тем самым расход реактивов. Процесс фиксирования также происходит значительно быстрее (на 50 % для некоторых эмульсий), чем для фиксажей с тиосульфатом натрия .
Однако слишком длительная обработка в фиксажах приводит к растворению металлического серебра в областях низкой плотности и потере деталей на изображении. Эффект особенно сильно выражен на мелкозернистых эмульсиях и быстрых фиксажах на тиосульфате аммония (из-за их большей активности), что требует точного соблюдения температурно-временно́го регламента процесса обработки. Также, для уменьшения этого эффекта, быстрые фиксажи применяются в различных степенях разбавления для плёнок и для фотобумаг; при этом для фотобумаг, имеющих более мелкозернистую эмульсию, требуется применять примерно в два раза более сильное разбавление .
Применение
Используется как компонент фиксирующих растворов в фотографии вместо тиосульфата натрия для ускорения процесса фиксирования. Так как имеет плохую сохранность в кристаллической форме, то часто непосредственно перед применением для этой цели его готовят в растворе, смешивая тиосульфат натрия с хлоридом аммония .
Примечания
- ↑ , с. 82.
- , с. 285.
Литература
- Гурлев Д. С. Справочник по фотографии (обработка фотоматериалов). — К. : Тэхника, 1988.
- Лидин Р. А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0 .
- Справочник химика / Редкол.: Никольский Б. П. и др.. — 3-е изд., испр. — Л. : Химия, 1971. — Т. 2. — 1168 с.
- Eaton G. (неопр.) . — second edition. — N. Y. : Morgan & Morgan, Inc., Publishers Hastings-on-Hudson, 1965.
- 2021-07-13
- 1

![{\displaystyle {\mathsf {NH_{4}HS\ {\xrightarrow[{-NH_{3}}]{O_{2}}}\ S,(NH_{4})_{2}S_{n},(NH_{4})_{2}SO_{3}S}}}](/images/006/035/6035591/4.jpg?rand=996281)