Спирты
- 1 year ago
- 0
- 0


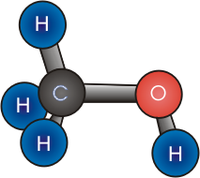
Спирты́ (от лат. spiritus — дух; устар. алкого́ли , от араб. الكحول аль-кухуль — порошок ) — органические соединения , содержащие одну или более гидроксильных групп (гидроксил, − O H ), непосредственно связанных с насыщенным (находящимся в состоянии sp ³-гибридизации ) атомом углерода . Спирты можно рассматривать как производные воды (H−O−H) , в которых один атом водорода замещён на органическую функциональную группу : R−O−H .
В номенклатуре ИЮПАК для соединений, в которых гидроксильная группа связана с ненасыщенным ( sp ²-гибридным ) атомом углерода, рекомендуются названия « енолы » (гидроксил связан с винильной C=C-связью) и « фенолы » (гидроксил связан с бензольным или другим ароматическим циклом) .
Спирты представляют собой обширный и разнообразный класс соединений: они весьма распространены в природе и часто выполняют важные функции в живых организмах . Спирты являются важными соединениями с точки зрения органического синтеза , не только представляя интерес как целевые продукты, но и как промежуточные вещества, имеющие ряд уникальных химических свойств . Кроме того, спирты являются промышленно важными продуктами и находят широчайшее применение как в промышленности, так и в повседневных приложениях .
Слово алкого́ль происходит от араб. الكحل ( al-kuḥl ) — «порошкообразная сурьма ». Понятие берёт начало от алхимической методики восстановления химических веществ до «порошка», являющегося, как предполагалось, чистой эссенцией вещества. Подобным образом, и этиловый спирт является эссенцией вина, от чего и произошло его название . В русский язык слово пришло через нем. Alkohol , нидерл. alkohol или порт. , исп. alcohol . Однако в русском языке сохранился в виде архаизма , по всей видимости, и омоним слова «алкоголь» в значении «мелкий порошок» .
Слово спирт появилось в русском языке во времена Петра I через английское слово spirit , которое, в свою очередь, произошло от латинского spīritus — «дыхание, дух, душа» .
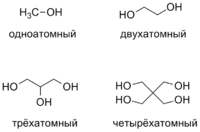


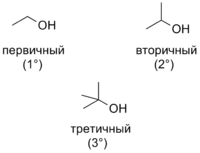
Спирты классифицируются следующим образом (в скобках приведены примеры) :
По номенклатуре ИЮПАК названия простых спиртов образуются от названий соответствующих алканов с добавлением суффикса «-ол», положение которого указывается арабской цифрой.
Правила построения названий спиртов :
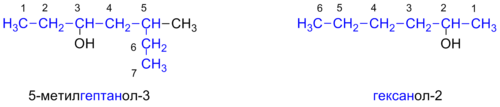
Хмельной растительный напиток, содержащий этанол , был известен человечеству с глубокой древности. Считается, что не менее чем за 8000 лет до нашей эры люди были знакомы с действием перебродивших фруктов, а позже — с помощью брожения получали хмельные напитки, содержащие этанол, из фруктов и мёда . Археологические находки свидетельствуют, что в Западной Азии виноделие существовало ещё в 5400—5000 годах до н. э. , а на территории современного Китая , провинция Хэнань , найдены свидетельства производства ферментированных смесей из риса , мёда, винограда и, возможно, других фруктов, в эпоху раннего неолита : от 6500 до 7000 гг. до н. э.
Важное открытие, о котором впервые свидетельствует одно из произведений, приписываемых Джабиру ибн Хайяну (IX век н. э.), заключалось в том, что увеличивает вина, и может повысить воспламеняемость образующихся паров .
Впервые спирт из вина получили в VI—VII веках арабские химики; способ получения спирта содержится в записях персидского алхимика Ар-Рази . В Европе этиловый спирт был получен из продуктов брожения в XI—XII веке , в Италии .
В Россию спирт впервые попал в 1386 году, когда генуэзское посольство привезло его с собой под названием «аква вита» и презентовало великокняжескому двору .
В 1661 году английский химик Роберт Бойль впервые получил метанол перегонкой древесины . Абсолютированный этанол из его водного раствора был впервые получен в 1796 году русским химиком Т. Е. Ловицем при перегонке над поташом .
В 1842 году немецкий химик Я. Г. Шиль открыл, что спирты образуют гомологический ряд , отличаясь на некоторую постоянную величину. Однако, он ошибся, описав её как C 2 H 2 . Спустя два года, другой химик Шарль Жерар установил верную гомологическую разницу CH 2 и предсказал формулу и свойства неизвестного в те годы пропилового спирта . В 1850 году английский химик Александр Вильямсон , исследуя реакцию алкоголятов с этилиодидом , установил, что этиловый спирт является производным воды с одним замещённым атомом водорода, экспериментально подтвердив формулу C 2 H 5 OH . Впервые синтез этанола действием серной кислоты на этилен осуществил в 1854 году французский химик Марселен Бертло .
Первое исследование метилового спирта было сделано в 1834 году французскими химиками Жаном-Батистом Дюма и Эженом Пелиго . Они назвали его «метиловым или древесным спиртом», так как он был обнаружен в продуктах сухой перегонки древесины . Синтез метанола из метилхлорида осуществил французский химик Марселен Бертло в 1857 году . Им же в 1855 году был открыт изопропиловый спирт , полученный действием серной кислоты на пропилен .
Впервые третичный спирт ( 2-метилпропанол-2 ) синтезировал в 1863 году известный русский химик А. М. Бутлеров , положив начало целой серии экспериментов в этом направлении .
Двухатомный спирт этиленгликоль впервые был синтезирован французским химиком А. Вюрцем в 1856 году . Глицерин был обнаружен в природных жирах ещё в 1783 году шведским химиком Карлом Шееле , однако его состав был открыт только в 1836 году, а синтез осуществлён из ацетона в 1873 году Шарлем Фриделем .

Спирты широко распространены в природе как в свободном виде, так и в составе сложных эфиров .
Метиловый спирт в небольшом количестве содержится в некоторых растениях, например: борщевике ( Heracleum ) .
Этиловый спирт является естественным продуктом анаэробного брожения органических продуктов, содержащих углеводы , под действием дрожжей рода Saccharomyces и бактерий и часто образуется в прокисших ягодах и фруктах. При этом углеводы через последовательность ферментативных реакций, именуемую гликолизом , превращаются в пируват , который далее под действием переходит в ацетальдегид . Последний затем в присутствии алкогольдегидрогеназы акцептирует восстановительный эквивалент от восстановленной формы NAD (восстановление NAD происходит на одной из стадий гликолиза), что даёт этанол в качестве конечного продукта. Данный процесс не только является причиной накопления этанола в природных объектах, но и активно используется в виноделии, пивоварении и хлебопекарной промышленности . В ходе брожения могут образовываться также и другие спирты, например, изопропанол , бутанол-1 , бутандиол-2,3 .
В эфирных маслах зелёных частей многих растений содержится ( Z )-гексен-3-ол-1 («спирт листьев»), придающий им характерный запах . Также в растительном мире очень широко представлены терпеновые спирты , многие из которых являются душистыми веществами , например: борнеол (компонент древесины борнеокамфорного дерева), ментол (в мяте , герани ) , гераниол и цитронеллол (компоненты цветочных эфирных масел ), фенхол (в смоле хвойных деревьев и плодах фенхеля ) и др.
В животном и растительном мире распространены конденсированные тетрациклические спирты (производные гонана ), обладающие высокой биологической активностью и входящие в класс стероидов , например, холестерин , содержащийся в клетках практически всех живых организмов, особенно животных . Отдельную группу стероидов составляют , находящиеся в жёлчи животных и человека: , , , , , и др.
В природе встречаются разнообразные спиртовые производные углеводов, например, сорбит (содержится в ягодах вишни и рябины ) , маннит (в ясене) и др.
В 1959 году немецким химиком Адольфом Бутенандтом при изучении экстракта самки тутового шелкопряда был открыт половой аттрактант, названный бомбиколом . Дальнейшее изучение феромонов насекомых показало, что значительная часть этих феромонов представлена спиртами .

Многие спирты являются участниками важных биохимических процессов, происходящих в живом организме. Так, некоторые витамины относятся к классу спиртов, например, витамин А (ретинол) , витамин D ( эргокальциферол и др.) . Стероидные гормоны , среди которых имеются и спирты ( эстрадиол , кортизол и др.), участвуют в регуляции обмена веществ и некоторых физиологических функциях организма .
Глицерин является основой более чем половины природных липидов , которые представляют собой его сложные эфиры с жирными кислотами и являются источниками энергии для организма . Также глицерин участвует в глюконеогенезе — процессе образования глюкозы в печени . При этом глицерин под действием ферментов превращается в глицеральдегид-3-фосфат , который далее попадает в метаболический путь глюконеогенеза . Физиологически важным полиолом является мио -инозитол .
Среди низших спиртов с точки зрения физиологии наибольший интерес представляет, несомненно, этанол . В организме человека этанол является естественным метаболитом и в норме присутствует в крови в очень низких концентрациях. Также этанол может поступать в организм с пищей. Этанол в организме человека метаболизируется преимущественно в печени . Под действием цитозольного фермента алкогольдегидрогеназы этанол окисляется в ацетальдегид , который далее перерабатывается митохондриальной альдегиддегидрогеназой в ацетат . Ацетат после активации короткоцепочечной ацил-коэнзим А-синтетазой может далее разрушаться в цикле Кребса . В утилизации этанола второстепенную роль играет также микросомальная этанол-окисляющая система, представленная цитохромом P450 и каталазой . При высокой концентрации алкоголя в крови ферменты не справляются с оксилением ацетальдегида до ацетата, и в организме происходит накопление ацетальдегида, который в 10—30 раз токсичнее этанола , за счёт чего происходит отравление организма, т. н. похмелье . По энергетической ценности для организма этанол (7 ккал/г) занимает промежуточное положение между углеводами (4,1 ккал/г) и жирами (9,3 ккал/г). Вклад этанола в общую калорийность пищи у не страдающих алкоголизмом взрослых людей может достигать 12 %. Однако потребление этанола в качестве пищевого продукта и источника энергии имеет ряд недостатков с биохимической точки зрения. Кроме образования токсичного ацетальдегида, к таким недостаткам следует причислить тот факт, что избыточные калории, поступившие в организм в форме этанола, могут запасаться только в жирах, так как возможность преобразования этанола в углеводы в организме человека отсутствует . Кроме того, этанол нарушает другие метаболические процессы: ингибирует глюконеогенез (это является причиной гипогликемии при приёме больших доз алкоголя), ускоряет производство цитокинов , изменяет концентрацию гормонов . Алкогольные напитки содержат очень мало витаминов и минеральных веществ, что также может оказать негативное влияние на здоровье. Также пищевой этанол сам по себе намного дороже, чем энергетически эквивалентное количество сахара .
Одноатомные предельные спирты вводят организм в наркозоподобное состояние, а также оказывают токсическое действие .
Метиловый спирт — сильный яд (особенно при приёме внутрь) нервного и сердечно-сосудистого действия с выраженным кумулятивным эффектом ; поражает органы зрения вплоть до полной слепоты . В больших дозах (30 г и более) вызывает смерть .
Этиловый спирт обладает токсическим эффектом. Быстро всасывается через слизистую оболочку желудка и тонкого кишечника, достигая максимальной концентрации в крови через 60—90 минут после его приёма . Этанол вызывает сначала возбуждение, а затем резкое угнетение центральной нервной системы (в том числе разрушает мозговую оболочку); его употребление приводит к нарушению важнейших функций организма, тяжёлому поражению органов и систем. Оказывает эмбриотоксическое и тератогенное действие.
Изопропиловый спирт по своему токсическому воздействию напоминает этанол, вызывая угнетение центральной нервной системы и поражая внутренние органы. В высокой концентрации приводит к коме, конвульсиям и летальному исходу (около 3—4 г/кг) .
В связи с широким использованием простейших спиртов в различных отраслях промышленности и, в частности, в качестве растворителей, опасным является их ингаляционное воздействие. Острое токсичное воздействие спиртов, испытанное на крысах, проявилось в следующих ингаляционных концентрациях:
Этиленгликоль очень токсичен при пероральном попадании в организм, поражает ЦНС и почки . Смертельная доза составляет 1,4 г/кг массы тела .

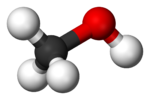
Молекулы спиртов, подобно молекуле воды , имеют угловое строение. Угол R−O−H в молекуле метанола равен 108,5° . Атом кислорода гидроксильной группы находится в состоянии sp ³-гибридизации . Спирты имеют существенно более высокие температуры плавления и кипения, чем можно было бы предполагать на основании физических свойств родственных соединений. Так, из ряда монозамещённых производных метана , метанол имеет необычно высокую температуру кипения, несмотря на относительно небольшую молекулярную массу :
Молекулярные массы и температуры кипения метана и некоторых его производных
|
Метан
CH 4 |
Метанол
CH 3 OH |
Хлорметан
CH 3 Cl |
Нитрометан
CH 3 NO 2 |
Бромметан
CH 3 Br |
|
|---|---|---|---|---|---|
| Молярная масса, г/моль | 16,04 | 32,04 | 50,48 | 61,04 | 94,94 |
| Температура кипения, °С | −161,5 | 64,5 | −24,2 | 101,2 | 3,6 |
Высокие температуры кипения спиртов объясняются наличием межмолекулярных водородных связей . Энергия водородной связи значительно ниже, чем энергия ковалентной химической связи . Так, например, для метанола энергия водородной связи составляет 16,7 кДж / моль , тогда как связи C−H, C−O и O−H имеют энергию 391,7, 383,5 и 428,8 кДж / моль соответственно . Тем не менее, влияние водородных связей на физические свойства спиртов весьма значительное.
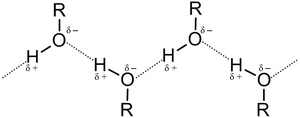
Молекулы спирта, имея две полярных связи C−O и O−H, обладают дипольным моментом (~5,3—6,0⋅10 −30 Кл·м) . Электростатические заряды в молекуле метанола составляют: на атоме углерода 0,297 e ; на атоме гидроксильного водорода 0,431 e ; на атоме кислорода −0,728 e . Вместе с тем, энергия ионизации спиртов ниже, чем у воды (10,88 эВ для метанола против 12,61 эВ для воды) , что объясняется электронодонорным эффектом алкильной группы.
Влияние гидроксильной группы особенно велико на соединения с небольшой углеводородной цепочкой. Так, например, метанол и этанол неограниченно смешиваются с водой и имеют довольно высокие плотности и температуры кипения для своей молекулярной массы, в то время как высшие спирты гидрофобны и мало отличаются по свойствам от соответствующих углеводородов .
| Название | Формула | Т. кип., °С | Т. пл., °С | Плотность, кг/м 3 (20 °С) | Показатель преломления, n D 20 |
|---|---|---|---|---|---|
| Метанол | CH 3 OH | 64,7 | −97,78 | 791,5 | 1,32855 |
| Этанол | C 2 H 5 OH | 78,3 | −114,65 | 789,5 | 1,36139 |
| Пропанол-1 | C 3 H 7 OH | 97,2 | −124,10 | 803,5 | 1,38556 |
| Пропанол-2 | CH 3 CH(CH 3 )OH | 82,5 | −87,95 | 786,2 | 1,37711 |
| Бутанол-1 | C 4 H 9 OH | 117,8 | −88,64 | 808,6 | 1,39929 |
| 2-Метилпропанол-1 | (СН 3 ) 2 СНСН 2 ОН | 108,0 | −101,97 | 802,1 | 1,39549 |
| Бутанол-2 | СН 3 СН 2 СН(ОН)СН 3 | 99,5 | −114,70 | 806,0 | 1,39240 |
| 2-Метилпропанол-2 | (СН 3 ) 2 С(OH)СН 3 | 82,9 | 25,82 | 765,2 | 1,38779 |
| Пентанол-1 | C 5 H 11 OH | 138,0 | −77,59 | 813,3 | 1,40999 |
| C 6 H 13 OH | 157,1 | -47,40 | 821,7 | 1,41816 | |
| C 7 H 15 OH | 176,3 | −32,80 | 824,0 | 1,42351 | |
| Октанол | C 8 H 17 OH | 195,1 | −16,30 | 822,7 | 1,42920 |
| Нонанол | C 9 H 19 OH | 213,5 | −5,00 | 827,0 | 1,43325 |
| Деканол | C 10 H 21 OH | 231,0 | 6,00 | 826,0 | 1,43660 |
| Название | Формула | Т. кип., °С | Т. пл., °С | Плотность, кг/м 3 (20 °С) | Показатель преломления, n D 20 |
|---|---|---|---|---|---|
| Пропен-2-ол-1 | CH 2 =CHCH 2 OH | 96,9 | −129 | 852,0 | 1,4133 |
| Пропин-2-ол-1 | CH≡CCH 2 OH | 113,6 | −48 | 948,5 | 1,4322 |
| Циклогексанол | C 6 H 11 OH | 161,1 | 25,15 | 941,6 | 1,4648 |
| Фенилкарбинол | C 6 H 5 CH 2 OH | 205,0 | −15,3 | 1041,9 | 1,5396 |
| C 6 H 5 CH 2 CH 2 OH | 218,2 | −27,0 | 1020,2 | 1,5325 | |
| C 6 H 5 CH=CHCH 2 OH | 256—258 | 34 | 1044,0 | 1,5819 | |
| (C 4 H 3 O)CH 2 OH | 155 | — | 1131,9 | 1,5324 |
| Название | Формула | Т. кип., °С | Т. пл., °С | Плотность, кг/м 3 (20 °С) | Показатель преломления, n D 20 |
|---|---|---|---|---|---|
| Глицерин | HOCH 2 CH(OH)CH 2 OH | 290 | 20 | 1260,4 | 1,4729 |
| Пентаэритрит | C (CH 2 OH) 4 | 263,5 | 1397 | 1,548 | |
| Этиленгликоль | OHCH 2 CH 2 OH | 197,85 | –12,6 | 1115,5 | 1,432 |
Спирты могут быть получены из самых разных классов соединений, таких как углеводороды , галогеналканы , амины , карбонильные соединения , эпоксиды . В основном, все методы сводятся к реакциям окисления , восстановления , присоединения и замещения .
Спирты получают, окисляя алканы и циклоалканы под действием сильных неорганических окислителей: озона , перманганата калия , оксида хрома (VI) , хромовой кислоты , диоксида селена , пероксида водорода , а также некоторых надкислот. Из-за возможности дальнейшего окисления получаемых спиртов, метод имеет значение только для получения третичных спиртов .
Окисление алкенов значительно более распространено в лабораторной практике, особенно для получения двухатомных спиртов — диолов . В зависимости от выбора реагента окисление можно провести с различной стереоселективностью : при действии на алкены тетраоксида осмия , перманганата калия , хлората натрия , иода с карбоксилатом серебра протекает син -гидроксилирование; для проведения анти -гидроксилирования используют пероксид водорода и надкислоты, оксиды молибдена (VI) и вольфрама (VI), оксид селена (IV) и пр .
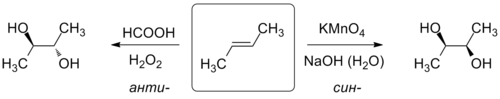
Спирты образуются также при восстановлении альдегидов или кетонов под действием борогидрида натрия в протонном растворителе, а также алюмогидрида лития . Восстановление сложных эфиров и карбоновых кислот также производится под действием комплексных гидридов, обычно, алюмогидрида лития и приводит к спиртам .
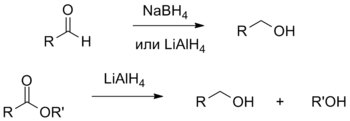
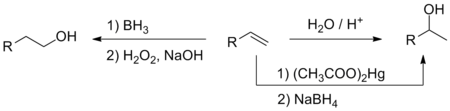
Кислотно-катализируемое присоединение воды к алкенам приводит к образованию спиртов. В соответствии с правилом Марковникова , в данной реакции образуются более замещённые спирты. В лабораторной практике чаще используют аналогичную, но более мягкую реакцию оксимеркурирования — демеркурирования, а также реакцию гидроборирования — окисления, приводящую к продуктам, не согласующимся с правилом Марковникова .
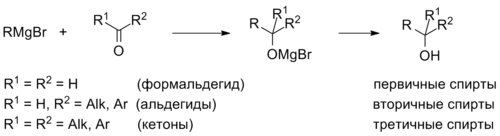
Реакции нуклеофильного присоединения металлорганических соединений ( ацетиленидов , реактивов Гриньяра , медь- и литийорганических соединений и т. д.) к карбонильным соединениям также приводят к спиртам, причём если присоединение происходит к формальдегиду HCHO, то образуются первичные спирты, если к другим альдегидам , то образуются вторичные спирты. Присоединение к кетонам даёт третичные спирты. Третичные спирты можно получить также путём присоединения двух эквивалентов металлорганического соединения к сложным эфирам .
Спирты можно получать при обработке галогеналканов раствором щёлочи . Реакция протекает как нуклеофильное замещение и сопровождается рацемизацией (при мономолекулярном механизме) или обращением конфигурации (при бимолекулярном механизме). Важным препаративным методом является окисление алкилгалогенидов надпероксидом калия .
В промышленности спирты получают при помощи химических методов либо биохимических методов производства.
Единственным промышленно важным методом синтеза метанола является каталитическая реакция между оксидом углерода (II) и водородом . Сырьём в производстве метанола служит природный газ , который на первой стадии процесса подвергают очистке от соединений серы (сера является ядом для катализаторов , используемых на следующей стадии). Далее происходит паровая конверсия природного газа в синтез-газ (смесь СО и водорода ), который после конденсации паров воды превращают в метанол на смешанном медно-цинко-хромовом катализаторе при температуре 250 °С и давлении до 10 МПа. Получаемый таким образом метанол содержит воду и примеси других спиртов (этанола, пропанола и более высших) и может быть очищен ректификацией . Мировое потребление метанола в 2015 году составило порядка 70 млн тонн .
Этанол и пропанол-2 получают методом гидратации соответствующих алкенов — этилена и пропилена . В промышленности используют два варианта гидратации: сернокислотную и каталитическую. Сернокислотная гидратация включает в себя абсорбцию этилена концентрированной серной кислотой (94—98 %) при температуре 80 °С и давлении 1,3—1,5 МПа и последующий гидролиз образующихся сульфоэфиров водой. Второй метод гидратации основан на использовании фосфорной кислоты , нанесённой на силикагель или другую подложку, в качестве катализатора . Смесь деионизированной воды и этилена нагревают до температуры 300 °С под давлением 6—8 МПа, а полученный этанол очищают ректификацией. Данные методы позволяют получить этанол, содержащий 5 % воды по массе. Получение безводного этанола (99,9 %) основано на воды с бензолом . По данным на 2003 год, мировое производство этанола только гидратацией этилена составляет 6 млн тонн в год .
Мировое производство топливного этанола в 2015 году по данным Renewable Fuel Association составило около 77 млн тонн .
Для гидратации пропилена требуются более мягкие условия. Сернокислотный процесс проводят при комнатной температуре и концентрации серной кислоты, равной 70—75 %, а каталитическая гидратация протекает при 180 °С и 4 МПа. Иногда для гидратации пропилена используют вольфрамовый катализатор (WO 3 ·SiO 2 , 250 °C и 25 МПа)). Мировое производство пропанола-2 в 2008 году составляло 1,8 млн тонн .
Также реакцией гидратации в промышленности получают этиленгликоль — один из важнейших продуктов химической промышленности, производимый в количестве 19,9 млн тонн ежегодно и используемый в больших количествах для производства антифриза и волокон . Сырьём для данного синтеза служит окись этилена , получаемая прямым окислением этилена кислородом воздуха. Превращение окиси этилена в этиленгликоль происходит при нагревании её смеси с 20-кратным мольным избытком воды до 200 °С без катализатора. Этиленгликоль затем отделяется от воды и продуктов олигомеризации в результате последовательных ректификаций .
Промышленное получение пропанола-1 основано на реакции гидроформилирования этилена и последующем гидрировании полученного пропаналя . Гидроформилирование проводится при температуре 90—130 °С, общем давлении пропилена, оксида углерода(II) и водорода, равном 2,8 МПа, и в присутствии 500 мд родиевого катализатора. Вторая стадия протекает при 110—150 °С в избытке водорода на различных металлических катализаторах (используются комбинации соединений меди , цинка , никеля и хрома ) . Объёмы мирового производства пропанола-1 на 2003 год составили 0,14 млн тонн .
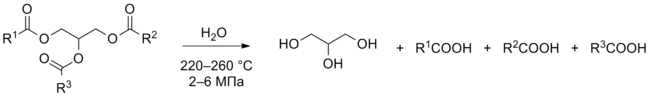
Глицерин получают как побочный продукт превращения жиров в жирные кислоты и метиловые эфиры жирных кислот . Данный процесс лежит в основе получения биодизеля , при этом на каждую тонну биодизеля образуется 100 кг глицерина. Таким методом синтезируют 1,5 млн тонн глицерина ежегодно (2004 год), причём по прогнозам эти объёмы будут расти в связи с увеличением интереса к альтернативным видам топлива. Жиры гидролизуют при 220—260 °С и давлении 2—6 МПа либо переэтерифицируют метанолом. Расщепление жиров под действием щёлочи либо карбонатов применяется в ограниченном масштабе, например, при производстве мыла .
Высшие жирные спирты производят несколькими способами, среди которых метиловых эфиров жирных кислот, получаемых переэтерификацией жиров, а также гидроформилирование алкенов и олигомеризация этилена с последующим окислением (метод Циглера). Ежегодно в мире производится 2,15 млн тонн высших жирных спиртов (2003 год) .
Для некоторых спиртов более важную роль в промышленном синтезе играют биохимические методы. В частности, объёмы производимого биоэтанола значительно превышают объёмы синтетического этанола. В основе биохимического получения этанола лежит кислотный или ферментативный гидролиз растительного сырья с последующей анаэробной спиртовой ферментацией (сбраживанием) образующихся углеводов дрожжевыми грибами ( Saccharomyces ) или некоторыми видами бактерий . В частности, дрожжи являются весьма удобными микроорганизмами для широкого промышленного использования. Ферментация под действием дрожжей характеризуется высокой , низким накоплением побочных продуктов, высоким выходом этанола, высокой скоростью процесса, хорошей толерантностью дрожжей к повышенным концентрациям этанола и субстрата. Сырьём в данном процессе могут служить легко ферментируемые углеводы, а также крахмал и другие органические субстраты, которые необходимо предварительно гидролизовать до ферментируемой формы. Обычно используют сельскохозяйственные культуры ( сахарная свёкла , картофель , зерновые культуры ), продукты лесного хозяйства ( древесина , солома ) либо сельскохозяйственные отходы .
Производство биобутанола основано на ферментации углеводного сырья с использованием бактерий Clostridium acetobutylicum .
Химические свойства спиртов определяются наличием в них гидроксильной группы . Поскольку гидроксильная группа является полярной , она может гетеролитически диссоциировать , особенно, под действием сильных оснований . Таким образом, спирты проявляют свойства слабых кислот . Кроме того, высокая электроотрицательность кислорода обуславливает наличие электрофильного атома углерода и, соответственно, способность спиртов подвергаться реакциям нуклеофильного замещения под действием ряда нуклеофилов. Наконец, атом кислорода гидроксильной группы имеет нуклеофильный характер, поэтому спирты могут выступать нуклеофилами в реакциях замещения и присоединения . Также для спиртов характерны реакции окисления .
Спирты способны проявлять как кислотные, так и основные свойства. Как слабые кислоты , спирты диссоциируют по связи O − H с образованием алкоксид-иона. Кислотные характеристики спиртов оценивают по константе кислотности K a .
В водном растворе кислотность спиртов снижается с увеличением молекулярной массы и разветвлённости углеводородной цепи. Это связывают с увеличением положительного индуктивного эффекта алкильных заместителей в данном ряду и уменьшением устойчивости образующегося алкоксид-иона за счёт локализации отрицательного заряда на атоме кислорода .
В целом, электроноакцепторные заместители (−NO 2 , −CN, −F, −Cl, −Br, −I, −OR и др.) увеличивают кислотность спиртов (уменьшают pK a ). Напротив, электронодонорные заместители (например, алкильные заместители) уменьшают кислотность спиртов (увеличивают pK a ). Так, pK a 2,2,2-трифторэтанола имеет значение 12,43 (против 15,9 у этанола), а полностью фторированного трет -бутанола — 5,4 (против 17,7 у трет -бутанола) . Сравнительная кислотность спиртов и соединений других классов схематически представлена на рисунке .
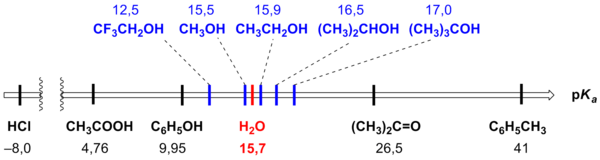
Как слабые кислоты , спирты вступают в реакции с щелочными , щелочноземельными и некоторыми другими металлами, и с сильными основаниями , например, гидридами или амидами металлов, реактивами Гриньяра .
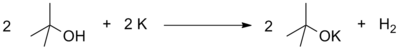
Спирты могут также вести себя как слабые основания Льюиса , образовывая с сильными минеральными кислотами соли алкоксония, а также давая донорно-акцепторные комплексы с кислотами Льюиса . Обычно подобные реакции не останавливаются на указанной стадии и ведут к нуклеофильному замещению гидроксильной группы или отщеплению воды .
Количественно основность спиртов оценивают по константе основности p K b или связанной с ней константе кислотности сопряжённой кислоты p K a H + :
Спирты являются слабыми основаниями, и их основность возрастает с увеличением длины или разветвлённости углеводородного радикала при гидроксильной группе. Данный эффект наблюдается из-за роста положительного индуктивного эффекта радикала в данном ряду, за счёт которого увеличивается отрицательный заряд на атоме кислорода гидроксильной группы .
Атом углерода, непосредственно соединённый с гидроксильной группой , имеет частичный положительный заряд, что делает возможной атаку нуклеофильной частицы ( галогенид -иона, аммиака , спирта и др.) по этому атому углерода с замещением гидроксильной группы на эту частицу. Гидроксильная группа является плохой уходящей группой , поэтому обычно необходима её дополнительная активация.
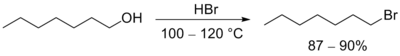
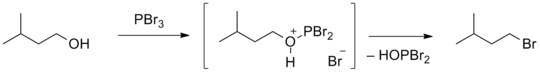
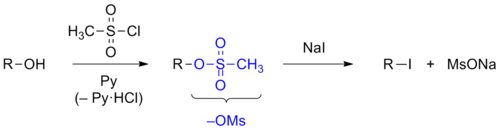
В присутствии кислотных катализаторов ( оксид алюминия , серная кислота , фосфорная кислота и др.) спирты могут подвергаться дегидратации с образованием алкенов . Например, дегидратация этилового спирта приводит к образованию этилена . Реакция протекает в соответствии с правилом Зайцева , согласно которому при дегидратации образуется более устойчивый, более замещённый при двойной связи алкен .
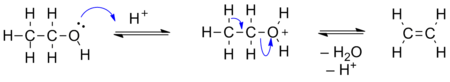

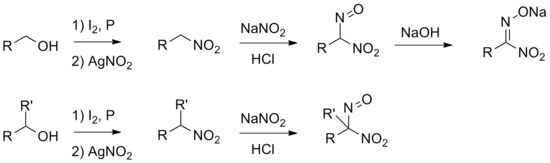
Наличие гидроксильной группы в соединении можно выявить несколькими распространёнными химическими реакциями.

Для количественного анализа спиртов обычно используют методы, основанные на реакции этерификации ангидридами карбоновых кислот, например, уксусным , фталевым , а также пиромеллитовым диангидридом. Содержание спирта определяется титрованием образующейся в результате реакции кислоты гидроксидом натрия .
Другой метод анализа заключается в определении количества гидроксильных групп, способных реагировать с метилмагнийиодидом. В данном случае расчёт ведут по количеству выделившегося метана ( метод Чугаева — Церевитинова ).
Для гликолей применим окислительно-восстановительный метод, где в качестве окислителя используется иодная кислота . Анализ проводят по реакции образующейся иодноватой кислоты HIO 3 с иодидом калия и последующим титрованием выделившегося иода тиосульфатом натрия .
Масс-спектры алифатических спиртов имеют слабые пики молекулярного иона, а для высших и разветвлённых спиртов эти пики практически отсутствуют, поскольку в существенной степени происходит фрагментация молекулы. Фрагментация, как правило, связана с потерей молекулы воды, а также элиминированием этилена . Для длинноцепочечных спиртов преобладает отщепление воды, поэтому их масс-спектры похожи на масс-спектры алкенов . Для первичных спиртов наблюдаются пики m/z 31 , для вторичных — m/z 45, 59, 73, … , для третичных — m/z 59, 73, 87, … .
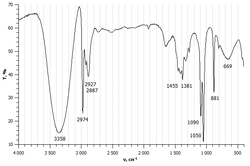
ИК-спектры спиртов характеризуются двумя типами интенсивных характеристических полос поглощения:
Также выделяют полосы поглощения средней интенсивности, как правило, не имеющие определяющего значения: в диапазоне 1450—1250 см −1 (плоскостные деформационные колебания O−H) и 750—650 см −1 (внеплоскостные деформационные колебания O−H) .
Характеристические полосы поглощения спиртов в инфракрасной области
| Типы связей и колебания | Диапазон, см −1 | Описание полосы поглощения |
|---|---|---|
| O−H, валентные колебания | ||
| ROH, неассоциированные | 3650—3580 | Узкая полоса, наблюдаемая в разбавленных растворах или парах |
| ROH···HOR, димеры (водородная связь) | 3550—3400 | Широкая полоса, теряющая интенсивность при разбавлении |
| ROH···HOR···, полимеры | 3400—3200 | Широкая полоса или ряд полос |
| С−O, валентные колебания | ||
| R 3 COH, третичные спирты | 1210—1100 | Полосы высокой интенсивности, уменьшающейся при разбавлении |
| R 2 CHOH, вторичные спирты | 1125—1000 | |
| RCH 2 OH, первичные спирты | 1075—1000 | |
| O−H, деформационные колебания | ||
| ROH |
1450—1250
750—650 |
Широкие полосы средней интенсивности, не имеющие практического значения |
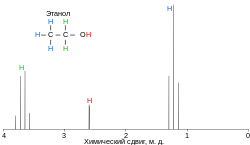
ЯМР-спектроскопия ядер 1 H широко используются для анализа спиртов, однако на величины химических сдвигов протонов гидроксильной группы ( δ , м. д.) существенно влияет природа растворителя и другие внешние факторы. Для алифатических и алициклических спиртов δ составляет 0,5—3,0 (в ДМСО -d 6 : 4—6) .
Также для изучения спиртов применяют спектроскопию на ядрах 17 O. Значительная разница в сдвигах для первичных (этанол: δ 5,9 м д.), вторичных (пропанол-2: δ 39,8 м д.) и третичных спиртов (2-метилпропанол-2: δ 62,3 м д.) относительно воды H 2 17 O позволяет установить или подтвердить структуру исследуемого соединения .
Области использования спиртов многочисленны и разнообразны, особенно учитывая широчайший спектр соединений, относящихся к этому классу. Вместе с тем, с промышленной точки зрения, только небольшой ряд спиртов вносит заметный вклад в глобальную мировую экономику.
В TOP 50 за 2002 год соединений , выпускаемых химической промышленностью США , из спиртов входят только метанол (14-е место) и этиленгликоль (29-е место) . В следующие 50 важнейших химических соединений, по данным за 1999 год, включены изопропиловый спирт , н - бутиловый спирт , синтетический этанол , пропиленгликоль , диэтиленгликоль , , бутандиол-1,4 , сорбит и глицерин .
Самым распространённым и используемым спиртом в мире является этанол . Его мировой объём потребления составляет около 65 млн тонн . Совокупный мировой объём потребления прочих спиртов (кроме этанола) по различным направлениям использования составляет около 70 млн тонн (по состоянию на 2009 год) .
Основная доля метилового спирта используется в промышленном синтезе формальдегида методом высокотемпературного каталитического окисления метанола . Кроме того, из метанола получают трет -бутилметиловый эфир , уксусную кислоту ( (англ.) () , N,N-диметиланилин , метиламины и хлорметан .
Из этанола в промышленности производят диэтиловый эфир (методом дегидратации при 250 °С над Al 2 O 3 ) , хлораль , ацетальдегид и этилацетат .
Изопропиловый спирт при каталитическом жидкофазном дегидрировании на никеле Ренея при 150 °С превращают в ацетон . Основным продуктом, получаемым из бутанола , является .
Для топливных целей в настоящий момент используются в промышленных объёмах три спирта: метанол , этанол и бутанол-1 , что связано, прежде всего, с их коммерческой доступностью и возможностью массового производства из растительного сырья (кроме метанола ). При этом возможно использование спиртов в виде горючего в чистом виде, в виде различных смесей с бензином или дизельным топливом , а также в качестве оксигенирующих добавок (до 10 %) с целью повышения октанового числа и снижения токсичности отработанных газов . Отдельным направлением является использование метанола для переэтерификации жиров в производстве биодизеля .
Преобладающим топливным спиртом является этанол. По оценкам экспертов, на 2009 год 80—90 % всего производимого в мире этилового спирта было использовано в этих целях и составило 73,9 млрд литров (≈ 58 млн тонн) .
Основными причинами, послужившими активному изучению спиртов в качестве альтернативного горючего, являются :
Вместе с тем, массовое использование вышеуказанных спиртов в качестве моторного топлива, помимо чисто экономических причин, имеет ряд недостатков :
Среди растворителей широкое распространение имеют самые разные типы спиртов: одноатомные ( метанол , пропанол-2 ) и многоатомные ( этиленгликоль , глицерин ); алифатические ( этанол , бутанол-1 ) и циклические ( циклогексанол ). Спирты относятся к полярным растворителям и применяются в различных отраслях промышленности . Мировой объём потребления спиртов в качестве растворителей (по данным на 2013 год) составил порядка 6,5 млн тонн .
Самым распространённым спиртом среди растворителей является этанол — его мировой объём потребления для этих целей (по данным на 2009 год) превышает 3,5 млн тонн в год . Другими популярными растворителями являются метанол и изопропанол с объёмами потребления более 1 млн тонн в год.
Использование спиртов в качестве растворителей включает в себя следующие направления :
Важнейшим сырьём в производстве современных поверхностно-активных веществ (ПАВ) для синтетических моющих средств являются высшие жирные спирты , из которых в зависимости от реагента получают неионогенные или .
Мировой объём использования высших жирных спиртов в производстве ПАВ в 2000 году составил 1,68 млн тонн . В 2003 году около 2,5 млн тонн ПАВ было произведено на основе высших жирных спиртов .
Спирты имеют важное применение в качестве исходных мономеров для синтеза полимерных материалов методом поликонденсации . В основном, на основе спиртов синтезируют полиэфиры и полиуретаны . Важнейшими примерами таких синтетических полимеров являются полиэтилентерефталат , полибутилентерефталат , получаемые из терефталевой кислоты и этиленгликоля или 1,4-бутандиола соответственно. Поликонденсацией гликолей , глицерина или пентаэритрита с фталевым ангидридом получают алкидные смолы , которые широко используются для изготовления лаков и красок. Полиуретаны получают поликонденсацией изоцианатов с гликолями или многоатомными спиртами .
Спирты также используются для производства сложноэфирных и диэфирных пластификаторов для полимеров .
Для получения негорючих гидравлических жидкостей применяют водные растворы, содержащие глицерин и этанол . В производстве тормозных жидкостей широко используют этиленгликоль и эфиры на его основе .
Многие современные смазочные материалы имеют в своём составе высшие жирные спирты и их эфиры, благодаря их низкой токсичности, высокой температуре вспышки и бесследному испарению при нагревании. Эти свойства используются для бытового применения, а также для случаев, когда эффект охлаждения поверхности более важен, чем антифрикционные свойства (например, при сверлении, пилении или другой слесарной обработке металлов) .

Несмотря на то, что незамещённые предельные алифатические спирты обладают фунгицидной или гербицидной активностью, их прямое использование в качестве пестицидов не находит широкого практического применения. Одним из немногих направлений является их использование в качестве регулятора роста растений . Подобными свойствами обладают этанол , этиленгликоль и другие гликоли, некоторые высшие жирные спирты .
Галогензамещённые спирты проявляют значительно большую активность и обладают , гербицидной и фунгицидной активностью. Так, например, препарат , представляющий смесь 1,3-дифторпропанола-2 и 1-фтор-3-хлорпропанола-2, используется для борьбы с мышевидными грызунами и сусликами .
Более высокая биологическая активность наблюдается у непредельных и ароматических спиртов. Аллиловый спирт находит применение в качестве гербицида, многие высшие непредельные спирты являются феромонами насекомых. Активными акарицидами являются некоторые ароматические бифениловые спирты: , , .
Многие спирты являются полупродуктами для синтеза различных пестицидов . Например, в производстве глифосата используется метанол , — , пиретроидов третьего поколения — .
Также спирты широко используются в качестве неводного носителя для создания товарных композиций пестицидов .

Основой всех алкогольных напитков является этанол , который получается при сбраживании пищевого сырья — винограда, картофеля, пшеницы и прочих крахмало- или сахаросодержащих продуктов. Кроме того, этиловый спирт используется в качестве компонента некоторых пищевых и ароматических эссенций (ароматизаторов) , широко используемых в кулинарии, при выпечке кондитерских изделий, производстве шоколада, конфет, напитков, мороженого, варений, желе, джемов, конфитюров и пр. Однако этанолом список спиртов, используемых в индустрии продуктов питания, не ограничивается. Спирты можно встретить среди самых разных пищевых добавок , например, глицерин (E422) используется как — влагоудерживающий агент, растворитель, загуститель, разделитель , плёнкообразователь , средство для капсулирования. Ряд спиртов находит применение в качестве сахарозаменителей ( ксилит , маннит , сорбит , эритрит ), ароматизаторов ( ментол ), красителей ( лютеин ) и т. д.
Спирты довольно широко используются в качестве душистых веществ для составления композиций в парфюмерно-косметической промышленности и производстве отдушек для бытовой химии и прочей потребительской продукции ( гераниол , нерол , цитронеллол , ментол и др.). Помимо придания аромата, в парфюмерно-косметической продукции спирты используются и в других целях :
Основным спиртом, применяющимся в медицинских целях, является этанол . Его используют в качестве наружного антисептического и раздражающего средства для приготовления компрессов и обтираний. Ещё более широко применяется этиловый спирт для приготовления различных настоек, разведений, экстрактов и прочих лекарственных форм .
Применение спиртов в качестве собственно лекарственных средств не столь заметно, однако многие препараты по формальному наличию гидроксильной группы можно отнести к рассматриваемому классу органических соединений ( кленбутерол , , маннит , эстрадиол и др.). Например, в перечне 10 наиболее важных рецептурных препаратов США в 2000 году 6-ю строчку занимает альбутерол , содержащий гидроксильную группу .
В настоящее время трудно найти область практической деятельности человека, где бы не использовались спирты в той или иной роли. Можно выделить следующие малозначительные направления использования: