Interested Article - Тучные клетки

- 2020-07-14
- 1

Ту́чные кле́тки (также известные как мастоци́ты или лаброци́ты , тканевые базофилы [ источник не указан 438 дней ] ) — тканевые клетки миелоидного ряда, содержащие в цитоплазме базофильные гранулы с гистамином и гепарином . В отличие от базофилов , также содержащих базофильные гранулы, тучные клетки в норме никогда не выходят в кровоток . Тучные клетки участвуют в развитии воспаления , реакций гиперчувствительности первого (немедленного) типа, защите организма от многоклеточных паразитов и других патогенов , формировании гематоэнцефалического барьера и других процессах . Тучные клетки лежат в основе развития аллергии и анафилаксии.
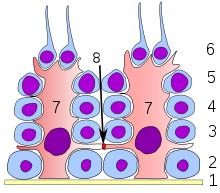
Тучные клетки присутствуют в большинстве тканей и, как правило, располагаются вблизи сосудов и нервов . Они особенно многочисленны в тканях, залегающих на границе организма с внешней или внутренней средой.
Общая характеристика

Морфологически тучные клетки очень близки к базофилам в кровотоке. И тучные клетки, и базофилы содержат базофильные гранулы с гепарином и гистамином. Однако между двумя типами клеток есть и различия в строении: так, у тучных клеток ядро округлое, а у базофилов разделено на доли. Округлое ядро мастоцитов находится центрально, часто замаскировано цитоплазматическими гранулами . Тучные клетки и базофилы связываются с Fc -участками молекул иммуноглобулинов E (IgE), связавшими антиген (кросс-связывание), в результате чего запускается высвобождение содержимого гранул. Из-за сходства с базофилами тучные клетки иногда называют тканевыми базофилами. Кроме того, базофилы и тучные клетки происходят от одного и того же костномозгового предшественника, экспрессирующего CD34 . Базофилы покидают костный мозг зрелыми, в то время как созревание тучных клеток завершается после их оседания в тканях. Место оседания тучных клеток может влиять на некоторые их свойства .
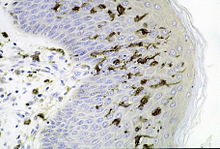
Тучные клетки присутствуют в большинстве тканей и, как правило, располагаются вблизи сосудов и нервов . Они особенно многочисленны в тканях, залегающих на границе организма с внешней или внутренней средой: коже , слизистой лёгких и пищеварительного тракта , а также в ротовой и носовой полостях и конъюнктиве . В подслизистом слое слизистых, дерме , серозных оболочках , селезёнке и периваскулярной соединительной ткани тучные клетки содержатся в количестве 10 4 —10 6 на 1 г ткани. На гистологических препаратах тучные клетки легко визуализируются при помощи окрашивания или . Для тучных клеток характерен эффект метахромазии при окрашивании анилиновыми красителями из-за большого количества кислых радикалов протеогликанов .
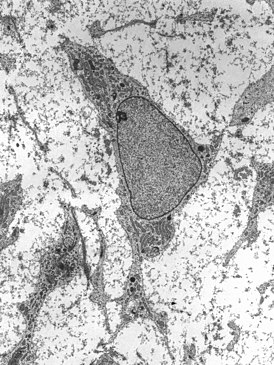
Тучные клетки достигают 10—20 мкм в диаметре и имеют овальную форму с ворсинчатой поверхностью. Композиция молекулярных маркеров на поверхности тучных клеток выглядит как + CD13 + CD29 + CD45 + CD117 + + . FcεRI являются высокоаффинными рецепторами IgE. CD117 представляет собой рецептор для (SCF), а CD123 — рецептор для IL-3 . Именно SCF и IL-3 являются основными факторами роста для зрелых тучных клеток. Также тучные клетки несут на своей поверхности рецепторы для компонентов комплемента и C3d, что свидетельствует об их участии в реакциях врождённого иммунитета . Кроме того, тучные клетки несут MHC обоих классов, и благодаря наличию и CD86 тучные клетки функционируют как антигенпрезентирующие клетки , особенно в отношении Th2-клеток .
Главная морфологическая особенность тучных клеток — наличие в цитоплазме большого количества (от 10 до 150) базофильных гранул, состав которых существенно варьирует между разными видами тучных клеток. У всех мастоцитов в состав гранул входят вазоактивные амины (прежде всего, гистамин), хондроитинсульфаты A и C и/или гепарин (у некоторых видов, например, кроликов , в их состав также входит серотонин ), а также разнообразные ферменты : протеазы , а также дегидрогеназа , , рибонуклеаза , гистидиндекарбоксилаза , и кислые гликозамингликаны . Среди протеиназ тучных клеток выделяют триптазы , близкие к трипсину по специфичности, , сходные с по специфичности, и . Помимо указанных компонентов, в состав гранул тучных клеток могут входить АТФ , лизосомальные ферменты (β- , , ), липидные медиаторы эйкозаноиды ( тромбоксаны , , , фактор активации тромбоцитов ), цитокины ( TNF-α , , интерлейкин 4 (IL-4), фактор стволовых клеток (SCF), хемокины ), активные формы кислорода .
У человека тучные клетки подразделяют на слизистые, или мукозные (тип t) и серозные (тип ct) на основании их локализации и наличия триптазы (t) или химазы (ct) в гранулах. Мукозные тучные клетки находятся в основном в подслизистом слое слизистых оболочек, а серозные — в серозных полостях, дерме, миндалинах . Оба типа мастоцитов образуются в костном мозге, но клетки t-типа в своем развитии зависят от тимуса . Серозные тучные клетки более долговечны, чем мукозные, и крупнее мукозных: их диаметр составляет 10—12 мкм против 5—10 мкм у мукозных . Главным ростовым фактором для обоих типов тучных клеток является SCF, для слизистых тучных клеток в роли кофактора выступают IL-3 и IL-4, для серозных — только IL-3. В слизистых тучных клетках преобладающим протеогликаном является хондроитинсульфат, в серозных — гепарин. Слизистые мастоциты, кроме того, интенсивнее экспрессируют FcεRI и содержат больше IgE в цитоплазме по сравнению с серозными. Преобладающим эйкозаноидом у слизистых тучных клеток являются лейкотриены , а у серозных — простагландины .
Активация

FcεR1 представляет собой высокоаффинный рецептор IgE на поверхности тучных клеток. FcεR1 — тетрамер из одной α-, одной β- и двух γ-цепей, соединённых дисульфидными мостиками . Сайт связывания IgE сформирован внеклеточной частью α-цепи, содержащей два домена , близких к . В состав β-цепи и каждой из двух γ-цепей входит активирующий мотив . Активирующий сигнальный каскад на FcεR1 запускается, когда ITAM в составе β- и γ-цепей фосфорилируются по остаткам тирозина .

Сигнальный путь , активирующийся при кросс-связывании FcεR1 с аллергеном при участии IgE, очень похож на тот, который запускается при активации лимфоцитов антигенами . С цитоплазматической частью β-цепи FcεR1 связана тирозинкиназа , и после кросс-связывания FcεR1 с аллергеном она фосфорилирует мотивы ITAM в β- и γ-цепях FcεR1. Другая тирозинкиназа, Syk , связывается с фосфорилированными ITAM в γ-цепях и активируется , фосфорилируя множество других белков и активируя их, тем самым увеличивая сигнал .
Среди белков, активируемых Syk, особенно важен белок , который в результате фосфорилирования приобретает способность к взаимодействию со многими белками. В частности, фосфолипаза C гамма (PLCγ) активируется в результате связывания с LAT и катализирует расщепление на инозитолтрифосфат (IP3) и диацилглицерин (DAG). IP3 повышает уровень ионов кальция в цитозоле , а DAG активирует протеинкиназу C (PKC). PKC фосфорилирует миозина , из-за чего базофильные гранулы приходят в движение и достигают контакта с клеточной мембраной . Далее гранула сливается с мембраной при участии белков SNARE , высвобождая наружу своё содержимое .
Активированные тучные клетки синтезируют и выделяют эйкозаноиды и цитокины. Среди эйкозаноидов в тучных клетках наиболее активно синтезируются лейкотриен C4 и . Образование эйкозаноидов контролирует цитозольный фермент фосфолипаза A 2 , который активируется при повышении концентрации кальция в цитозоле или фосфорилировании .
По спектру выделяемых цитокинов тучные клетки близки к T-хелперам 2 типа, или Th2-клеткам. Они продуцируют такие цитокины, как IL-3, IL-4, IL-5 , IL-6 , IL-10 , , GM-CSF , а также IL-1 , IL-8 , , IL-18 , , , TNF-α и гомеостатические цитокины IL-7 и IL-15 . Также они вырабатывают TGFβ , ряд хемокинов и интерфероны основных типов. Большинство цитокинов тучные клетки синтезируют под действием внешних стимуляторов, и лишь IL-4, TNF и GM-CSF они выделяют постоянно. Кроме того, активированные мастоциты продуцируют ряд ростовых факторов: фактор роста эндотелия сосудов (VEGF), фактор роста фибробластов (FGF) и фактор роста нервов (NGF) .
Функции
Тучные клетки принимают участие в развитии аллергических и анафилактических реакций. Высвобождение содержимого гранул при связывании Fc-участка антител IgE, связавших антиген, с рецепторами FcεRI на мастоцитах приводит к проявлению всех основных реакций гиперчувствительности немедленного типа. Дегрануляция не приводит к гибели клеток, и после выброса гранулы восстанавливаются. Также дегрануляция запускается при повышении внутриклеточной концентрации цАМФ и цитозольной концентрации ионов кальция. Благодаря наличию паттернраспознающих рецепторов TLR2 , TLR3 и TLR4 тучные клетки могут напрямую распознавать патогены и характерные для них молекулы . Кроме того, за счет специальных рецепторов на тучных клеток их могут активировать некоторые компоненты комплемента .
Гистамин, входящий в состав гранул тучных клеток, вызывает расширение посткапиллярных венул , активирует эндотелий и повышает . Выделение гистамина приводит к локальной эдеме (набуханию), покраснению, увеличению температуры и поступлению других иммунных клеток в очаг активации мастоцитов. Гистамин также деполяризует нервные окончания , что вызывает болевые ощущения .
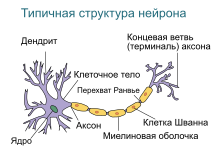
Тучные клетки имеются в головном мозге человека , где взаимодействуют с . В головном мозге мастоциты обнаруживаются в структурах, обеспечивающих передачу висцеральных сенсорных сигналов (например, болевых) или осуществляющих функции, а также в гематоэнцефалическом барьере. Они присутствуют в гипофиза , эпифизе , таламусе , гипоталамусе , области в стволе мозга , сосудистом сплетении , а также мозговых оболочках . В нервной системе тучные клетки выполняют те же основные функции, что и в остальных частях тела: они задействованы в аллергических реакциях, реакциях врождённого и приобретённого иммунитета , и воспалении . Кроме того, тучные являются главными , на которые воздействуют патогены через .
В пищеварительном тракте слизистые мастоциты находятся рядом с сенсорными нервными окончаниями . Когда они подвергаются дегрануляции, они высвобождают медиаторы, активирующие висцеральные афферентные нейроны и повышают экспрессию мембранных ноцицепторов в них, связываясь с соответствующими рецепторами на поверхности нейронов . В результате этого процесса могут развиться нейрогенное воспаление, и нарушения перистальтики кишечника . Активированные нейроны выделяют нейропептиды , такие как вещество P и , которые связываются с соответствующими рецепторами на тучных клетках и запускают их дегрануляцию, приводящую к выделению таких веществ, как β-гексозаминидаза, цитокины, хемокины, простагландин D2, лейкотриены и .
Развитие
Общий предок тучных клеток находится в костном мозге, а окончательная дифференцировка предшественников этих клеток происходит в селезёнке. Далее в кровоток выходят предшественники тучных клеток, у человека имеющие фенотип CD13 + CD33 + CD34 + CD38 + CD117 + . Из кровотока предшественники мастоцитов мигрируют в ткани (наиболее интенсивно — в слизистую кишечника), где их дифференцировка завершается. Главные ростовые факторы тучных клеток — SCF и IL-3, кофакторами выступают IL-4, IL-9, IL-10 и фактор роста нервов (NGF). В слизистых оболочках для развития тучных клеток необходим IL-33. Тучные клетки весьма долговечны (срок жизни исчисляется месяцами и годами) и в зрелой форме сохраняют способность к делению .
Эволюция
Тучные клетки имеются у представителей всех классов позвоночных животных . Рецепторы FcεRI тучные клетки приобрели, по-видимому, на поздних этапах эволюции , поскольку антитела IgE имеются только у млекопитающих . Триптаза и гистамин имеются в гранулах тучных клеток уже у костистых рыб , и именно у них тучные клетки оформились в том виде, в каком они присутствуют у высших позвоночных. Клетки, от которых, возможно, произошли мастоциты, были идентифицированы у асцидий . Эти клетки содержат гистамин и гепарин и выполняют защитные функции. Кроме того, структурно к тучным клеткам близки некоторые гемоциты членистоногих . Первые тучные клетки, вероятно, появились около 450—500 млн лет назад у последнего общего предка круглоротых , хрящевых рыб и высших позвоночных .
Клиническое значение

Выделяют группу заболеваний, известных как расстройства активации тучных клеток ( англ. mast cell activation disorders ). К ним относят нарушения со стороны иммунной системы, не связанные с заражением патогеном и имеющие схожие симптомы, связанные с несвоевременной активацией тучных клеток. Классификация расстройств активации тучных клеток и их диагностические критерии были предложены в 2010 году .
Тучные клетки лежат в основе развития аллергии и анафилаксии. Преимущественно с активацией тучных клеток связаны многие формы кожных аллергических реакций и аллергических реакций со стороны слизистых. Тучные клетки играют ключевую роль в развитии астмы , экземы , чесотки , аллергического ринита и аллергического конъюнктивита . Для устранения симптомов аллергии часто применяют антигистаминные препараты , блокирующие связывание гистамина с нервными окончаниями. Препараты на основе кромоглициевой кислоты блокируют кальциевые каналы , необходимые для дегрануляции тучных клеток, благодаря чему стабилизируют мастоциты и предотвращают выделение гистамина и других медиаторов. Антагонисты лейкотриенов, такие как монтелукаст и зафирлукаст , блокируют действие лейкотриенов и находят всё большее применение в устранении симптомов аллергии . При анафилаксии происходит резкое и мощное высвобождение содержимого гранул тучных клеток в организме, что может привести к смерти . Мастоциты связаны с развитием некоторых аутоиммунных заболеваний , таких как ревматоидный артрит и буллёзный пемфигоид .
Повышенное количество тучных клеток и их CD34+ клеток-предшественников приводят к развитию состояния, известного как мастоцитоз . Часто мастоцитоз связан с мутациями гена , кодирующего CD117 — рецептор SCF . Иногда из тучных клеток развиваются опухоли — , при которых в организме накапливается избыточное количество медиаторов, содержащихся в гранулах тучных клеток . Мастоцитомы часто встречаются у кошек и собак . С тучными клетками связаны некоторые другие неоплазии , в частности, чрезвычайно агрессивные и острый тучноклеточный лейкоз .
История изучения
Тучные клетки впервые описал Пауль Эрлих в 1878 году в своей докторской диссертации , где он также охарактеризовал их гранулы. Эрлих ошибочно решил, что тучные клетки питают окружающие ткани, поэтому назвал их Mastzellen (от нем. Mast — откармливать). Впоследствии было показано, что тучные клетки функционально относятся к иммунной системе .
Примечания
- . Memidex. Дата обращения: 19 февраля 2011. Архивировано из 6 ноября 2018 года.
- , с. 58.
- da Silva E. Z. , Jamur M. C. , Oliver C. (англ.) // The Journal Of Histochemistry And Cytochemistry : Official Journal Of The Histochemistry Society. — 2014. — October ( vol. 62 , no. 10 ). — P. 698—738 . — doi : . — .
- ↑ Polyzoidis S. , Koletsa T. , Panagiotidou S. , Ashkan K. , Theoharides T. C. (англ.) // Journal Of Neuroinflammation. — 2015. — 17 September ( vol. 12 ). — P. 170—170 . — doi : . — .
- ↑ , с. 120.
- ↑ Prussin C. , Metcalfe D. D. (англ.) // The Journal Of Allergy And Clinical Immunology. — 2003. — February ( vol. 111 , no. 2 Suppl ). — P. 486—494 . — doi : . — .
- ↑ , с. 61.
- , с. 60—61.
- ↑ , с. 60.
- Moon T. C. , Befus A. D. , Kulka M. (англ.) // Frontiers In Immunology. — 2014. — Vol. 5 . — P. 569—569 . — doi : . — .
- Ashmole I. , Bradding P. (англ.) // Clinical And Experimental Allergy : Journal Of The British Society For Allergy And Clinical Immunology. — 2013. — May ( vol. 43 , no. 5 ). — P. 491—502 . — doi : . — .
- , с. 122.
- Kinet J. P. (англ.) // Annual Review Of Immunology. — 1999. — Vol. 17 . — P. 931—972 . — doi : . — .
- ↑ , p. 423—424.
- Rivera J. , Cordero J. R. , Furumoto Y. , Luciano-Montalvo C. , Gonzalez-Espinosa C. , Kovarova M. , Odom S. , Parravicini V. (англ.) // Molecular Immunology. — 2002. — September ( vol. 38 , no. 16-18 ). — P. 1253—1258 . — doi : . — .
- , p. 424.
- Ren H. , Han R. , Chen X. , Liu X. , Wan J. , Wang L. , Yang X. , Wang J. (англ.) // Journal Of Cerebral Blood Flow And Metabolism : Official Journal Of The International Society Of Cerebral Blood Flow And Metabolism. — 2020. — September ( vol. 40 , no. 9 ). — P. 1752—1768 . — doi : . — .
- ↑ Carabotti M. , Scirocco A. , Maselli M. A. , Severi C. (англ.) // Annals Of Gastroenterology. — 2015. — April ( vol. 28 , no. 2 ). — P. 203—209 . — .
- ↑ Budzyński J. , Kłopocka M. (англ.) // World Journal Of Gastroenterology. — 2014. — 14 May ( vol. 20 , no. 18 ). — P. 5212—5225 . — doi : . — .
- ↑ Wouters M. M. , Vicario M. , Santos J. (англ.) // Gut. — 2016. — January ( vol. 65 , no. 1 ). — P. 155—168 . — doi : . — .
- , с. 59.
- Crivellato E. , Ribatti D. (англ.) // Biological Reviews Of The Cambridge Philosophical Society. — 2010. — May ( vol. 85 , no. 2 ). — P. 347—360 . — doi : . — .
- ↑ Frieri M. (англ.) // Clinical Reviews In Allergy & Immunology. — 2018. — June ( vol. 54 , no. 3 ). — P. 353—365 . — doi : . — .
- ↑ Akin C. , Valent P. , Metcalfe D. D. (англ.) // The Journal Of Allergy And Clinical Immunology. — 2010. — December ( vol. 126 , no. 6 ). — P. 1099—1104 . — doi : . — .
- , с. 123.
- Lee D. M. , Friend D. S. , Gurish M. F. , Benoist C. , Mathis D. , Brenner M. B. (англ.) // Science (New York, N.Y.). — 2002. — 6 September ( vol. 297 , no. 5587 ). — P. 1689—1692 . — doi : . — .
- Horny H. P. , Sotlar K. , Valent P. (англ.) // Pathobiology : Journal Of Immunopathology, Molecular And Cellular Biology. — 2007. — Vol. 74 , no. 2 . — P. 121—132 . — doi : . — .
- . The Merck Veterinary Manual (2006). Дата обращения: 8 июля 2007. 23 мая 2007 года.
- Chott A. , Guenther P. , Huebner A. , Selzer E. , Parwaresch R. M. , Horny H. P. , Valent P. (англ.) // The American Journal Of Surgical Pathology. — 2003. — July ( vol. 27 , no. 7 ). — P. 1013—1019 . — doi : . — .
- Lichtman M. A. , Segel G. B. (англ.) // Blood Cells, Molecules & Diseases. — 2005. — November ( vol. 35 , no. 3 ). — P. 370—383 . — doi : . — .
- Ehrlich P. Beiträge zur Theorie und Praxis der histologischen Färbung (нем.) . — Leipzig University, 1878.
- . Дата обращения: 16 августа 2010. Архивировано из 3 февраля 2010 года.
Литература
- Жункейра Л. К., Карнейро Ж. Гистология. — М. : ГЭОТАР-Медиа, 2009. — 576 с. — ISBN 978-5-9704-1352-4 .
- Ярилин А. А. Иммунология. — М. : ГЭОТАР-Медиа, 2010. — 752 с. — ISBN 978-5-9704-1319-7 .
- Abul K. Abbas, Andrew H. Lichtman, Shiv Pillai. . — Philadelphia: Elsevier Saunders, 2015. — ISBN 978-0-323-22275-4 .
- 2020-07-14
- 1