Interested Article - Гиалуроновая кислота

- 2020-10-04
- 1
Гиалуро́новая кислота́ , гиалурона́н , гиалурона́т (сокр. ГК) — линейный , несульфированный гликозаминогликан , входящий в состав соединительной , эпителиальной и нервной тканей . От других гликозаминогликанов, присутствующих в организме человека, гиалуронан отличается высокой молекулярной массой и тем, что он не сульфонирован и не подвергается модификации после синтеза в организме. Гиалуронан — единственный гликозаминогликан, находящийся в свободном состоянии в промежуточном веществе межклеточного пространства дермы , а также в соединительной ткани всех позвоночных .
Гиалуроновая кислота является одним из основных компонентов внеклеточного матрикса , содержится во многих ( слюне , синовиальной жидкости и др.). Принимает значительное участие в пролиферации и миграции клеток. Продуцируется некоторыми бактериями (напр. Streptococcus ). В теле человека весом 70 кг в среднем содержится около 15 граммов гиалуроновой кислоты, треть из которой преобразуется (расщепляется или синтезируется) каждый день .
Инъекции гиалуроновой кислоты — наиболее часто применяемые в косметологии процедуры .
Функции
Гиалуроновая кислота — важный компонент суставного хряща , в котором присутствует в виде оболочки каждой клетки ( хондроцита ). При связывании гиалуроновой кислоты с мономерами аггрекана в присутствии связующего белка, в хряще формируются крупные отрицательно заряженные агрегаты, поглощающие воду. Эти агрегаты отвечают за упругость хряща (устойчивость его к компрессии). Молекулярная масса (длина цепи) гиалуроновой кислоты в хряще уменьшается с возрастом организма, при этом общее её содержание увеличивается .
Структура
Структура гиалуроновой кислоты была установлена в 1930-х годах в лаборатории Карла Майера ( ).
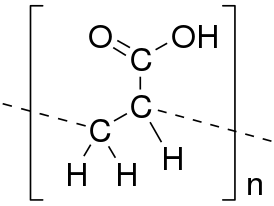
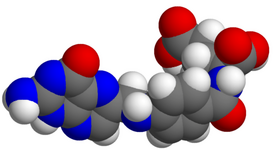
Молекула гиалуроновой кислоты представляет собой линейный полимер дисахаридного фрагмента гиалобиуроновой кислоты (основа полимера – дисахарид из пары D-глюкуронида-β-(1,3)-(N-ацетил)-глюкозамина, соединённых β(1→4)-гликозидной связью) . Иначе – это поли-(2-ацетамидо-2-дезокси-D-глюко)-D-глюкуроногликан, то есть полимер , состоящий из остатков D-глюкуроновой кислоты и D-N-ацетилглюкозамина , соединённых поочерёдно β-1,4- и β-1,3- гликозидными связями . [ источник не указан 187 дней ]
Молекула гиалуроновой кислоты может содержать до 25 000 дисахаридных звеньев. Природная гиалуроновая кислота имеет молекулярную массу от 5000 до 20 000 000 дальтон. Средняя молекулярная масса полимера, содержащегося в синовиальной жидкости у человека составляет 3 140 000 дальтон .
Молекула гиалуроновой кислоты является энергетически стабильной в частности благодаря стереохимии составляющих её дисахаридов . Объёмные заместители пиранозного кольца находятся в стерически выгодных положениях, в то время как меньшие по размеру атомы водорода занимают менее выгодные аксиальные позиции.
Гиалуронан не имеет изомеров, это вещество вне зависимости от источника (организма) происхождения имеет одинаковый состав и различается только молекулярной массой .
Размер (длина) молекул гиалуронана значительно превышает размеры молекул других гликозаминогликанов. В водном растворе средний продольный размер макромолекулы гиалуронана с молекулярной массой 2 500 000 Да превышает 10 мкм . Длина этой молекулы приблизительно равна диаметру эритроцита человека и значительно больше среднего размера бактерий .
Гиалуронан гидрофилен. Гидрофильные свойства молекуле гиалуроновой кислоты обусловлены наличием в ней карбоксильных, гидроксильных и ацетоамидных групп .
В тканях молекулы гиалуронана образуют сетчатую структуру и формируют межклеточный матрикс .
Биосинтез
Синтез молекул гиалуроновой кислоты осуществляется с помощью ферментов — гиалуронансинтазами (HA-synthase, HAS), семейством интегральных мембранных белков, которые синтезируют чётко определённые, однородные по длине цепи, характерные для молекул гиалуроната . В организмах позвоночных существует три типа HAS: HAS1, HAS2, HAS3; каждый из них способствует удлинению полимера ГК . Для создания капсулы гиалуроната должны присутствовать эти ферменты, поскольку они полимеризуют предшественники UDP-сахарá в молекулы ГК. Предшественники ГК синтезируются путём предварительного фосфорилирования глюкозы гексокиназой с образованием глюкозо-6-фосфата , который является основным прекурсом (предшественником) ГК . Затем используются два пути синтеза UDP-N-ацетилглюкозамина и UDP-глюкуроновой кислоты, которые оба вступают в реакцию с образованием молекул ГК. Глюкозо-6-фосфат превращается либо во фруктозо-6-фосфат с помощью фосфоглюкоизомеразы, либо в глюкозо-1-фосфат с помощью фосфоглюкомутазы, причём оба метаболита (Ф-6-Ф и Г-1-Ф) подвергаются различным реакциям .
Синтез UDP-глюкуроновой кислоты
Уридиндифосфат-глюкуроновая кислота (UDP-глюкуроновая кислота) образуется с помощью UDP-глюкозопирофосфорилазы, которая переносит молекулу UDP от UTP на глюкозо-1-фосфат, превращая в UDP-глюкозу, которая затем вступает в реакцию окисления UDP-глюкозодегидрогеназой (NAD + -зависимая), с образованием UDP-глюкуроновой кислоты .

Синтез UDP-N-ацетилглюкозамина
Дальнейший путь превращения фруктозо-6-фосфата протекает в сторону образования глюкозамина-6-фосфата, реакцию катализирует фермент амидотрансфераза (переносит NH 2 -группу от молекулы L-глутамина на фруктозо-6-фосфат). Затем мутаза вступает в реакцию с данным продуктом (изомеризация) с образованием глюкозамина-1-фосфата. Далее ацетилтрансфераза преобразует его в N-ацетилглюкозамин-1-фосфат (ацетилирование NH 2 -группы), и, наконец, пирофосфорилаза путём переноса UDP от UTP, превращает этот продукт в молекулы UDP-N-ацетилглюкозамина .

Объединение UDP-глюкуроновой кислоты и UDP-N-ацетилглюкозамина
Молекулы UDP-глюкуроновой кислоты и UDP-N-ацетилглюкозамина связываются вместе, с помощью гиалуронансинтазы, образуя гиалуроновую кислоту, таким образом завершая синтез .

Биодеградация
Гиалуроновая кислота деградируется семейством ферментов, называемых гиалуронидазами . В организме человека существуют по меньшей мере семь типов гиалуронидазоподобных ферментов, некоторые из которых являются супрессорами опухолеобразования. Продукты разложения гиалуроновой кислоты ( олигосахариды и крайне низкомолекулярные гиалуронаты) проявляют проангиогенные свойства. Кроме того, недавние исследования показали, что фрагменты гиалуроновой кислоты, в отличие от исходного высокомолеколекулярного полисахарида, способны индуцировать воспалительный ответ в макрофагах и дендритных клетках при повреждениях тканей и отторжении трансплантированной кожи. [ источник не указан 187 дней ]
Применение
Гиалуроновая кислота — наиболее часто используемый в косметологии инъекционный препарат .
Также гиалуроновая кислота используется в качестве вспомогательной среды для переноса эмбрионов при вспомогательных репродуктивных технологиях, в качестве жидкости для обработки язв ног и пролежней, при лечении (как перорально, так и инъекционно) заболеваний суставов. Все эти методы применения гиалуроновой кислоты объединяет низкое качество как исследований эффективности, так и побочных эффектов. Большинство исследований, показавших эффективность, произведены на малых группах, положительные эффекты отмечены не во всех исследованиях и снижаются в тех из них, где уменьшается вероятность систематической ошибки .
Существует множество исследований применения гиалуроновой кислоты при различных болезнях суставов, но все они отличаются малой выборкой и слабым контролем побочных эффектов, особенно плохо обстоит дело с наблюдением за потенциально возможными долговременными побочными эффектами. Несмотря на то, что по большей части исследования лечения дисплазии , остеоартрозов и прочих заболеваний суставов с помощью гиалуроновой кислоты показывают успешные данные, ни одно на 2023 год исследование не является высококачественным и заслуживающим абсолютного доверия (и, кроме того, исследования могут быть сознательно ангажированными).
По данным систематического обзора и метаанализа , опубликованного в 2012 году в Annals of Internal Medicine , внутрисуставные инъекции гиалуроновой кислоты приносят небольшую, клинически несущественную пользу и обусловливают значительный риск потенциальных побочных эффектов . Согласно кокрановскому обзору 2015 года, не существует качественных исследований эффективности гиалуроновой кислоты при остеоартрите голеностопного сустава: имеющиеся клинические испытания применения гиалуроновой кислоты при этом заболевании низкокачественные (с малым числом участников) . В среднем испытуемые оценивали улучшение физического состояния и уменьшение боли как на 12% большее, чем при эффекте плацебо. В связи с этим «инъекции гиалуроновой кислоты могут быть условно рекомендованы после выявленной неудачи использования простых анальгетиков».
Исследования перорального использования гиалуроновой кислоты в качестве профилактики и лечения болезней суставов у человека и домашних животных на 2023 год ещё меньше по размеру выборки и качеству исследования (в отличие от больших исследований аналогов- гликозамингликанов : хондроитинсульфатов и глюкозамина сульфатов, по которым можно судить об их неэффективности, несмотря на десятилетия их традиционного использования)
Также гиалуроновая кислота применяется в препаратах искусственной слезы .
Происхождение названия
Название «гиалуроновая кислота» этому веществу было дано в 1934 году ( нем. Karl Meyer ) и Дж. Палмером (J. W. Palmer), которые впервые выделили его из стекловидного тела глаза . Название происходит от греч. hyalos — стекловидный и уроновая кислота . [ источник не указан 187 дней ]
Сопряжённое основание для гиалуроновой кислоты носит название гиалуронат . Поскольку молекула полимера в организме обычно существует в промежуточной форме, многие авторы считают более корректным использование термина гиалуронан . [ источник не указан 187 дней ]
См. также
Примечания
- ↑ .
- Stern R. Hyaluronan catabolism: a new metabolic pathway (англ.) // : journal. — 2004. — August ( vol. 83 , no. 7 ). — P. 317—325 . — .
- Holmes M W A., Bayliss M T., Muir H. Hyaluronic acid in human articular cartilage. Age-related changes in content and size (англ.) // : journal. — 1988. — Vol. 250 . — P. 435—441 .
- Saari H et al. (1993) Differential effects of reactive oxygen species on native synovial fluid and purified human umbilical cord hyaluronate. Inflammation 17:403-415.
- ↑ Sze, Jun Hui; Brownlie, Jeremy C.; Love, Christopher A. (June 2016). . 3 Biotech . 6 (1): 67. doi : . ISSN . PMC . PMID .
- Itano, Naoki (2002). . Proceedings of the National Academy of Sciences . Proc Natl Acad Sci USA. 99 (6): 3609—3614. Bibcode : . doi : . PMC . PMID .
- ↑ Moreno-Camacho, Carlos A.; Montoya-Torres, Jairo R.; Jaegler, Anicia; Gondran, Natacha (2019-09-10). . Journal of Cleaner Production (англ.) . 231 : 600—618. doi : . ISSN . S2CID .
- . medgel.ru. Дата обращения: 24 ноября 2017.
- (англ.) . www.cochrane.org . Дата обращения: 14 сентября 2023.
- ↑ Rutjes A. W. , Jüni P. , da Costa B. R. , Trelle S. , Nüesch E. , Reichenbach S. (англ.) // Annals Of Internal Medicine. — 2012. — 7 August ( vol. 157 , no. 3 ). — P. 180—191 . — doi : . — .
- Devorah Heymann, Liat Vidal, Yuval Or, Zeev Shoham. // The Cochrane Database of Systematic Reviews. — 2020-09-02. — Т. 9 , вып. 9 . — С. CD007421 . — ISSN . — doi : .
- Witteveen, A. G. H. : [ 21 апреля 2021 ] = Hyaluronic acid and other conservative treatment options for osteoarthritis of the ankle : [пер. с англ. ] / A. G. H. Witteveen, C. J. Hofstad, G. M. M. J. Kerkhoffs // Cochrane Database of Systematic Reviews. — 2015. — No. 10. Art. No. CD010643 (17 октября). — doi : .
- Jasvinder A Singh, Shahrzad Noorbaloochi, Roderick MacDonald, Lara J Maxwell. // The Cochrane Database of Systematic Reviews. — 2015-01-28. — Т. 2015 , вып. 1 . — С. CD005614 . — ISSN . — doi : .
- Allen D Sawitzke, Helen Shi, Martha F Finco, Dorothy D Dunlop, Crystal L Harris, Nora G Singer, John D Bradley, David Silver, Christopher G Jackson, Nancy E Lane, Chester V Oddis, Fred Wolfe, Jeffrey Lisse, Daniel E Furst, Clifton O Bingham, Domenic J Reda, Roland W Moskowitz, H James Williams, Daniel O Clegg. // Annals of the rheumatic diseases. — 2010-8. — Т. 69 , вып. 8 . — С. 1459–1464 . — ISSN . — doi : .
- Нагорский, П. Г. : [ 12 сентября 2014 ] // Новое в офтальмологии : журн. — 2012. — № 3.
- K. Meyer and J. W. Palmer. (англ.) // J. Biol. Chem. : journal. — 1934. — Vol. 107 . — P. 629—634 . от 27 декабря 2007 на Wayback Machine
Литература
- Patil, K. P., Kamalja, K. K., & Chaudhari, B. L. (2011). Optimization of medium components for hyaluronic acid production by Streptococcus zooepidemicus MTCC 3523 using a statistical approach. Carbohydrate Polymers, 86(4), 1573–1577.
- Rampratap, P., Lasorsa, A., Perrone, B., van der Wel, P. C., & Walvoort, M. (2023). Production of isotopically enriched high molecular weight hyaluronic acid and characterization by solid-state NMR. bioRxiv, 2023-03.
- Zhang, Z., Tian, X., Lu, J. Y., Boit, K., Ablaeva, J., Zakusilo, F. T., ... & Gorbunova, V. (2023). Increased hyaluronan by naked mole-rat HAS2 extends lifespan in mice. bioRxiv, 2023-05.
- Galvez-Martin, P., Soto-Fernandez, C., Romero-Rueda, J., Cabañas, J., Torrent, A., Castells, G., & Martinez-Puig, D. (2023). A novel hyaluronic acid matrix ingredient with regenerative, anti-aging and antioxidant capacity. International journal of molecular sciences, 24(5), 4774. PMID PMC doi :
- Galdi, F., Pedone, C., McGee, C. A., George, M., Rice, A. B., Hussain, S. S., ... & Garantziotis, S. (2021). Inhaled high molecular weight hyaluronan ameliorates respiratory failure in acute COPD exacerbation: a pilot study. Respiratory Research, 22(1), 1-11. PMID PMC doi :
- Капулер, О. : [ англ. ] / О. Капулер, А. Галеева, Б. Сельская … [ et al. ] // Врач : журн. — 2015. — № 2. — С. 25–27.
- 2020-10-04
- 1